Impureza-8 Relacionada ao Salmeterol
- Número CAT DCTI-C-211
- Número CAS NA
- Fórmula Molecular C26H38O2
- Peso molecular 382.59
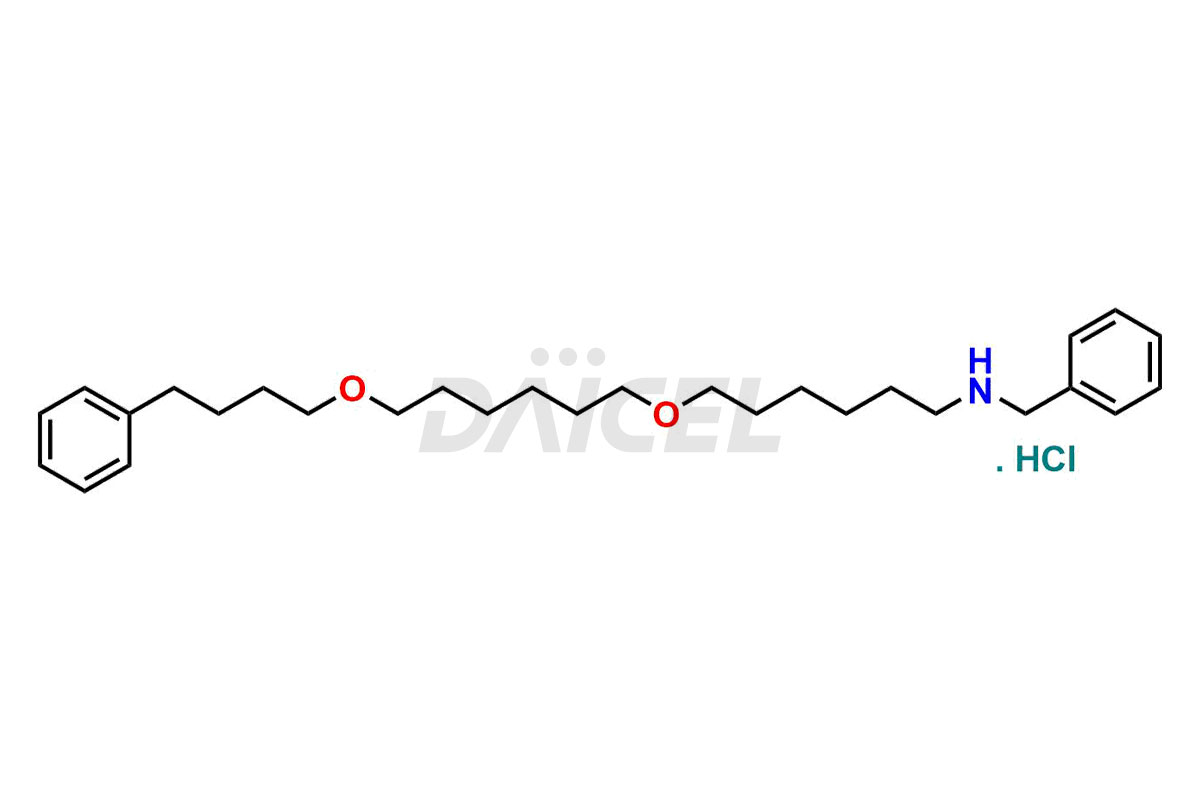
Impureza-9 Relacionada ao Salmeterol
- Número CAT DCTI-C-212
- Número CAS NA
- Fórmula Molecular C29H46ClNO2 (sal HCl) C29H45NO2 (base livre)
- Peso molecular 476.14 (sal HCl) 439.68 (base livre)
CARREGUE MAIS
Você visualizou todos os 29 produtos