Важность циклических пептидов и роль примесей
Циклические пептидные препараты и их значение
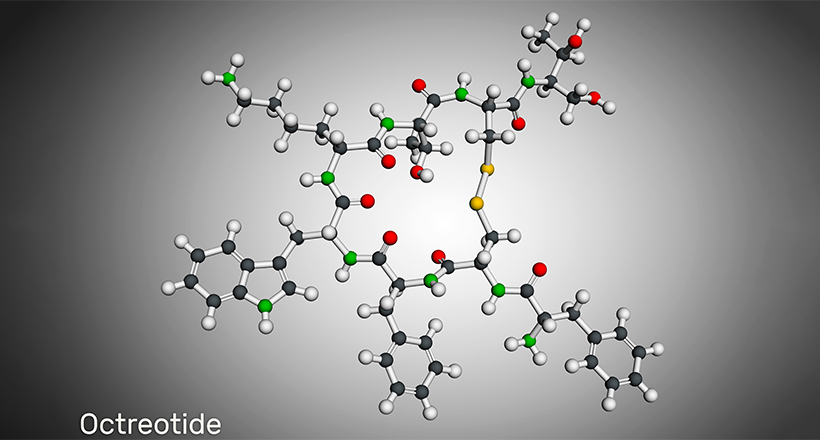
Циклические пептиды представляют собой класс молекул, которые привлекли значительное внимание при разработке лекарственных средств благодаря их уникальным свойствам, включая высокую стабильность, целевую специфичность, повышенную эффективность и клеточную проницаемость. Циклические пептиды представляют собой полипептидные цепи, имеющие циклическую кольцевую структуру, состоящую из 5-14 аминокислот с молекулярной массой примерно от 500 до 2000 Да. Кольцевая структура может быть образована путем связывания одного конца пептида и другого амидной связью или другими химически стабильными связями, такими как лактонная, эфирная, тиоэфирная, дисульфидная и т.д.
Циклизация пептидных последовательностей помогает более эффективно связываться с соответствующими рецепторами. Циклическая структура пептидов обеспечивает большую площадь поверхности для взаимодействия с целевым сайтом. Циклические пептидные препараты невосприимчивы к ферментативному гидролизу, поскольку не имеют свободных амино- и карбоксильных концов, что повышает их стабильность. Обычно циклические пептиды проявляют лучшую биологическую активность по сравнению со своими линейными аналогами благодаря конформационной структуре, что обеспечивает усиление связывания с молекулами-мишенями или селективность рецептора.
Некоторые циклические пептидные препараты включают Daptomycin, Телаванцин, Далбаванцин, Ланреотид, Октреотид, Linaclotide, Plecanatide, Ромидепсин, вазопрессин, Окситоцини Кальцитонин. Многие циклические пептидные препараты получены из природных источников, таких как циклоспорин А, бактенецин, лактоциклин и другие. Однако в настоящее время широкое распространение получают биоинженерные синтетические циклические пептидные препараты.
Как синтезировать циклические пептиды?
Синтез циклических пептидов включает твердофазный синтез пептидов (SPPS). В этом методе синтез пептидов происходит линейно, иммобилизованных на гранулах смолы с дисульфидным линкером или другими химически стабильными связями, такими как лактон, эфир и тиоэфир. После образования линейного пептида возможные защитные группы отщепляются, и пептиды высвобождаются путем добавления основания. Кроме того, депротонирование N-концевой тиоловой группы затрагивает дисульфидный линкер между пептидом и смолой при внутримолекулярной циклизации, давая желаемый циклический пептид.
В целом, синтез циклических пептидов требует тщательного контроля защитных групп, связывающих реагентов и условий реакции для обеспечения высоких выходов и чистоты.
Методы синтеза циклических пептидов
Для получения циклических пептидных соединений используются различные методы: • комбинаторная химия • синтез de novo. • циклизация, опосредованная химиоселективным лигированием
В зависимости от циклизации, методы синтеза циклических пептидов: голова к хвосту, боковая цепь к боковой цепи, голова к боковой цепи и боковая цепь к хвосту. Циклизация аминокислот боковой цепи происходит с образованием дисульфидного мостика между цистеином. Кроме того, циклизация от основной цепи к основной цепи осуществляется путем образования амидной связи между N-концевыми и С-концевыми аминокислотными остатками.
Кроме того, существуют и другие циклические пептиды, такие как бициклические/трициклические пептиды и сшитые циклические пептиды. Бициклические пептиды являются эффективными ингибиторами ферментов, а сшитые пептиды облегчают проникновение пептидов в клетки и используют сшивающие агенты для улучшения физико-химических свойств.
Примеси в циклических пептидных препаратах
Примеси могут возникать в результате синтеза циклических пептидов. Связанными с API примесями являются укорочения, модификации функциональных групп, вставки или делеции аминокислот, окисление или восстановление функциональных групп, агрегаты и неполное снятие защиты. Хроматографические среды, используемые при очистке, и растворители также могут способствовать образованию примесей в препаратах циклических пептидов. Продукты деградации возникают из-за изменений в лекарственном препарате при хранении в течение длительного времени или воздействия света, температуры, воды или реакции на вспомогательные вещества. Для обеспечения безопасности и эффективности циклических пептидных препаратов важно контролировать и минимизировать количество примесей в процессах синтеза и очистки.
Общие пептидные примеси, такие как N-Ac-примесь, дезамидирование по остаткам Gln, Asn, дезамидирование по С-концу, примесь трисульфида, цианоаланин @ остаток Asn, дез-Gly и эндо-Gly концевых аминокислот, являются обычными в циклических пептидах. слишком. Деградация и другие укороченные пептиды также являются основным классом примесей в этих циклических пептидах.
Помимо примесей описанного выше типа, в циклических пептидах часто образуются другие примеси, такие как параллельные и антипараллельные димеры.
- Seq: Cys(1)-Tyr-Phe-Gln-Asn-Cys(6)-Pro-Arg-Gly-CONH2 (серная связь между цистеинами)
- Параллельные димеры: 1,1', 6,6'
- Антипараллельные димеры: 1,6',1',6
- Seq: H-Asn-Asp-Glu-Cys(4)-Glu-Leu-Cys(7)-Val-Asn-Val-Ala-Cys(12)-Thr-Gly-Cys(15)-Leu-OH(4-12), (7-15)-bis(disulfide)
- Параллельные димеры: 4,4', 7,7', 12,12', 15,15';
- Антипараллельные димеры: 4,7',4',7, 12,15', 12',15; или 4,12',4',12,7,15',7',15 или 4,15',4',15, 7,12',7',12
- Seq: H-Cys(1)-Cys(2)-Glu-Tyr-Cys(5)-Cys(6)-Asn-Pro-Ala-Cys(10)-Thr-Gly-Cys(13)-Tyr- ОН (3 дисульфидных мостика между 1-6, 2-10 и 5-13 цистеинами)