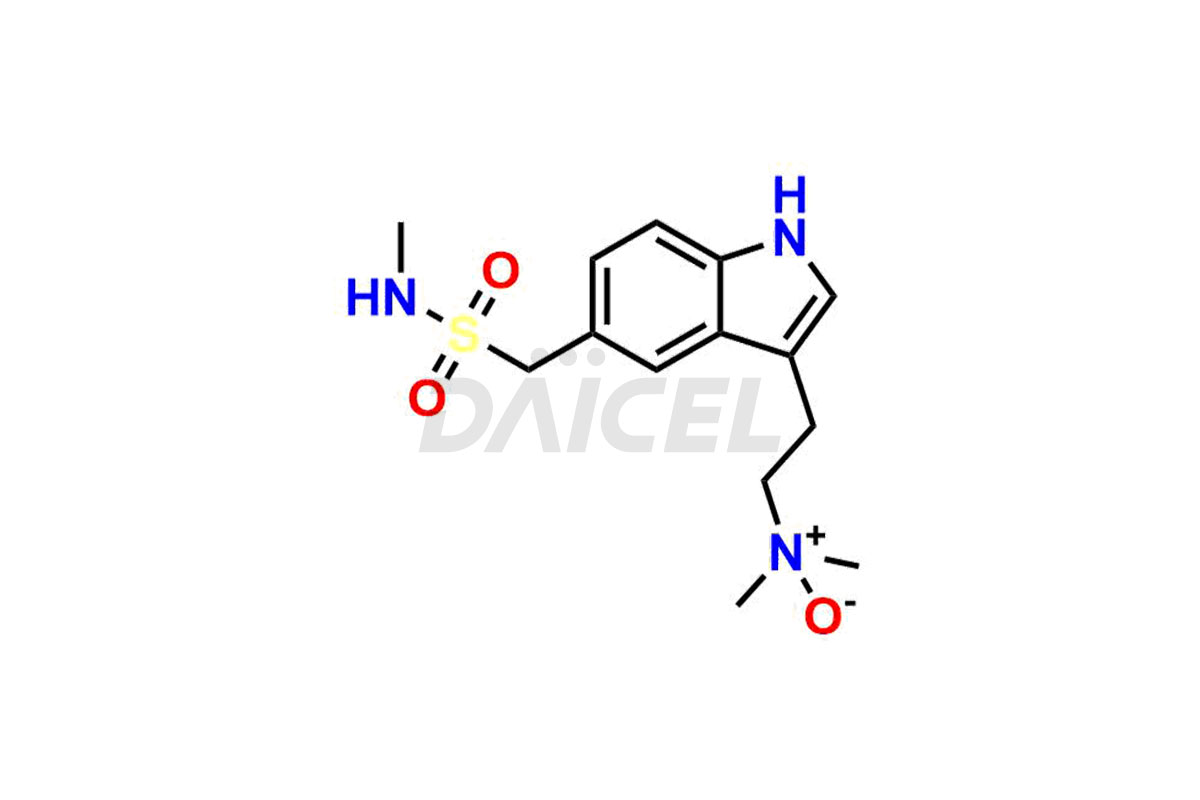
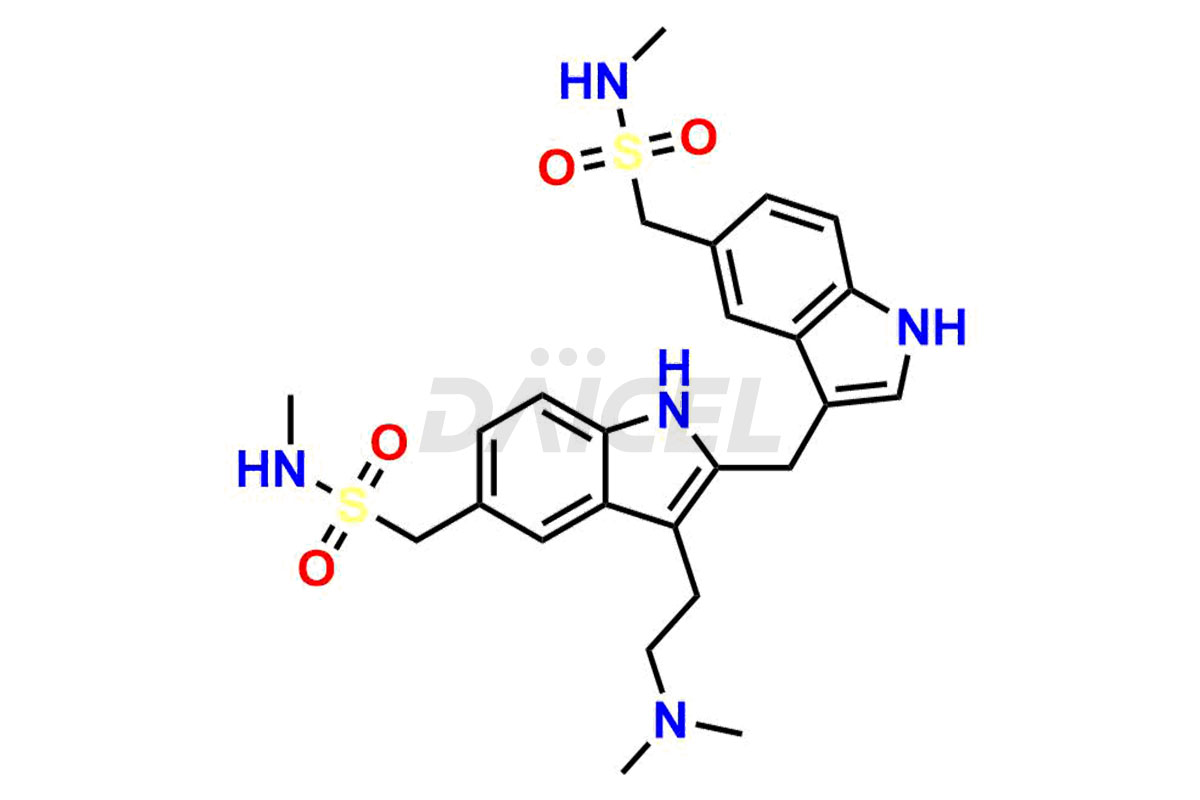
Sumatriptan
Referências
- Oxford, Alexander William, derivado de indol, Glaxo Group Ltd., Reino Unido, US5037845A, 6 de agosto de 1991
- Oxford, J.; Lant, MS, Desenvolvimento e validação de um ensaio cromatográfico-espectrométrico de massa líquido para a determinação de sumatriptano no plasma, Journal of Chromatography, Biomedical Applications, Volume: 496, Issue: 1, Pages: 137-46, 1989
- Dunne, Moira; Andrew, Peter, Ensaio totalmente automatizado para a determinação de sumatriptano em soro humano usando extração em fase sólida e cromatografia líquida de alta eficiência com detecção eletroquímica, Journal of Pharmaceutical and Biomedical Analysis, Volume: 14, Edição: 6, Páginas: 721-726 , 1996
Perguntas Frequentes
Como são detectadas e quantificadas as impurezas do Sumatriptano?
As impurezas no sumatriptano são detectadas e quantificadas usando várias técnicas analíticas, como cromatografia líquida de alto desempenho de fase reversa (RP-HPLC).
Por que é essencial controlar as impurezas do Sumatriptano?
Controlar a presença de impurezas no Sumatriptano é crucial para garantir que o medicamento seja de alta qualidade, seguro e eficaz. Além disso, podem prejudicar vários aspectos do desempenho do medicamento, tais como a sua potência, estabilidade e prazo de validade global.
Qual solvente auxilia na análise de impurezas de Sumatriptano?
Água ou DMSO é o solvente usado na análise de muitas impurezas do Sumatriptano.
Quais são as condições de temperatura necessárias para armazenar as impurezas do Sumatriptano?
As impurezas de sumatriptano são armazenadas em temperatura ambiente controlada entre 2-8 ⁰C ou conforme indicado no Certificado de Análise (CoA).
Nota: Os produtos protegidos por patentes válidas de um fabricante não são colocados à venda em países com proteção de patente. A venda de tais produtos constitui uma violação de patente e sua responsabilidade corre por conta e risco do comprador.