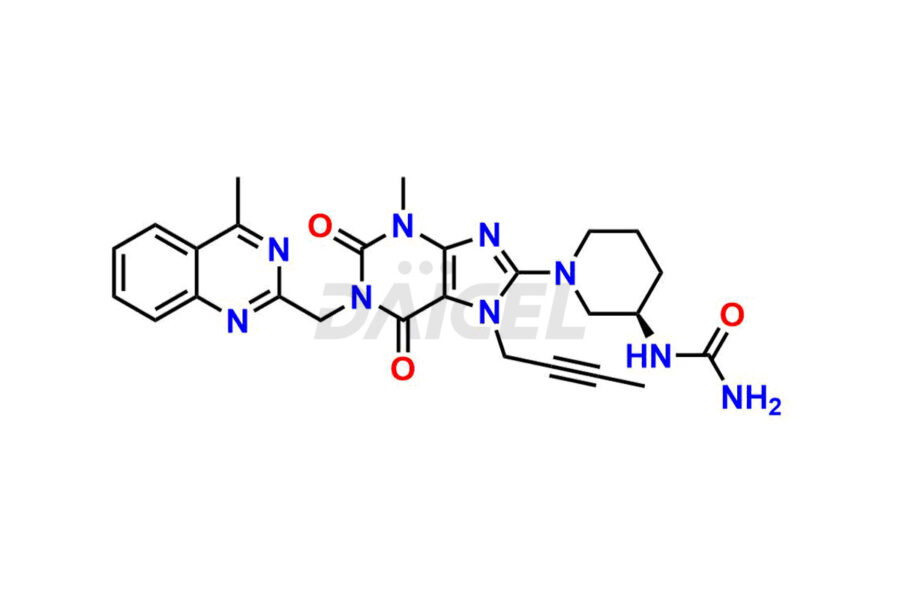
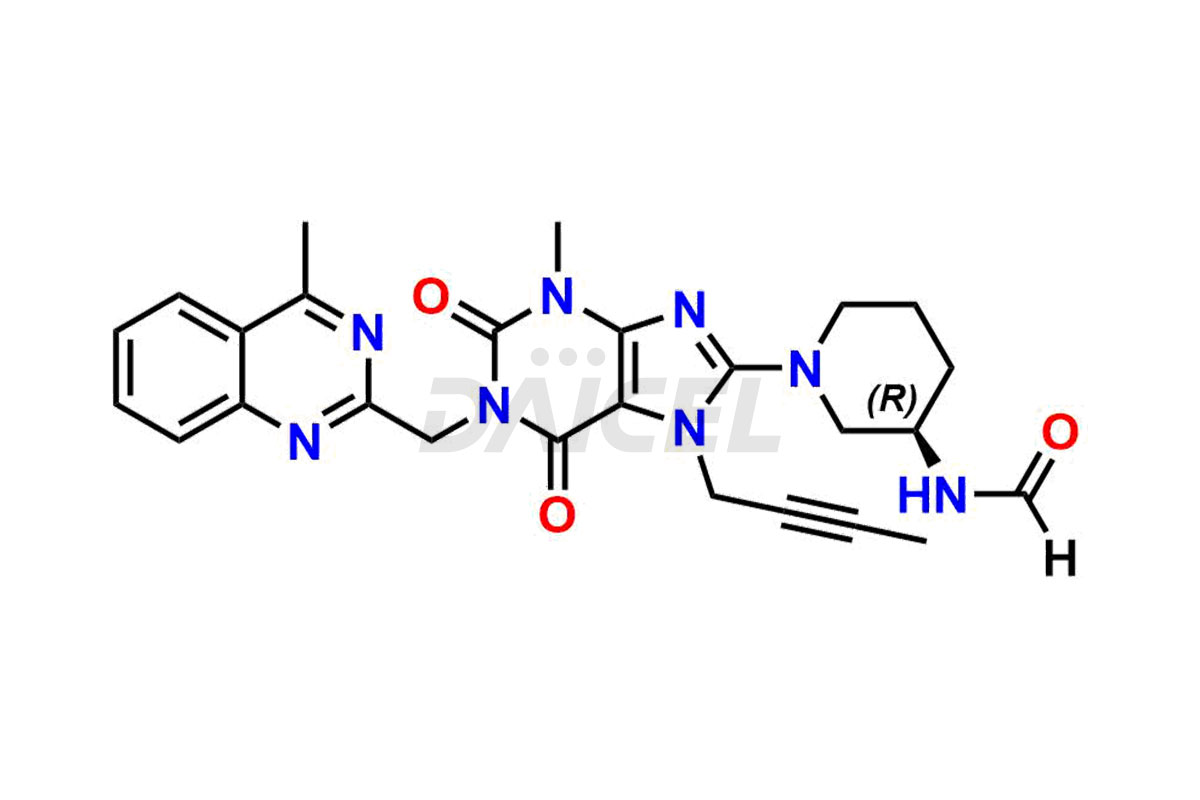
Linagliptina
Referências
- Himmelsbach, Frank; Langkopf, Elke; Eckhardt, Matias; Marcos, Michael; Maier, Roland; Lotz, Ralf Richard Hermann; Tadayyon, Mohammad,8-[3-amino-piperidin-1-il]-xantinas, a preparação das mesmas e seu uso como composições farmacêuticas, Boehringer Ingelheim Pharma GmbH & Co. K.-G., Alemanha, US7407955B2, 5 de agosto, 2008
- El-Bagary, Ramzia Ismail; Elkady, Ehab Farouk; Ayoub, Bassam Mahfouz, Determinação espectrofluorométrica de linagliptina a granel e em forma farmacêutica, European Journal of Chemistry, Volume: 5, Edição: 2, Páginas: 380-382, 3 pp., 2014
Perguntas Frequentes
Existem diretrizes ou requisitos específicos para relatar impurezas de Linagliptina?
As diretrizes regulatórias descrevem a documentação e os relatórios necessários sobre impurezas de Linagliptina para garantir transparência e responsabilidade.
As impurezas da Linagliptina são testadas quanto ao seu potencial genotóxico?
Os testes de genotoxicidade são normalmente realizados para avaliar o potencial das impurezas da Linagliptina em causar danos ou mutações no DNA.
As impurezas da Linagliptina podem resultar de processos de fabricação inadequados?
Processos de fabricação inadequados, como manuseio inadequado ou contaminação, podem contribuir para a formação de impurezas na Linagliptina.
Qual é a temperatura de armazenamento recomendada para impurezas de Linagliptina?
As impurezas de linagliptina devem ser armazenadas em temperatura ambiente controlada, geralmente entre 2-8 °C.
Nota: Os produtos protegidos por patentes válidas de um fabricante não são colocados à venda em países com proteção de patente. A venda de tais produtos constitui uma violação de patente e sua responsabilidade corre por conta e risco do comprador.