Informação Geral
Bortezomibe Impurezas e Bortezomibe
Daicel Pharma sintetiza impurezas de Bortezomibe de alta qualidade, incluindo impureza de ácido de Bortezomibe, impureza de amida de Bortezomibe, dímero de Bortezomibe e enantiômero de Bortezomibe. Essas impurezas são essenciais para avaliar a qualidade, estabilidade e segurança de um insumo farmacêutico ativo, o Bortezomibe. Além disso, a Daicel Pharma oferece uma síntese personalizada de impurezas de Bortezomibe para entrega global para atender às necessidades específicas de nossos clientes.
Bortezomibe [CAS: 179324-69-7] é um agente antineoplásico e inibidor de proteassoma que trata linfomas e mieloma múltiplo refratário. É um derivado modificado do ácido dipeptidil borônico que trata o mieloma múltiplo.
Bortezomibe: uso e disponibilidade comercial
O bortezomibe é um agente antineoplásico aprovado pela FDA para o tratamento do mieloma múltiplo. Também trata o linfoma de células do manto em pacientes submetidos a pelo menos um tratamento prévio de primeira linha. Velcade é a marca sob a qual o Bortezomibe está disponível.
Estrutura e mecanismo de ação do bortezomibe
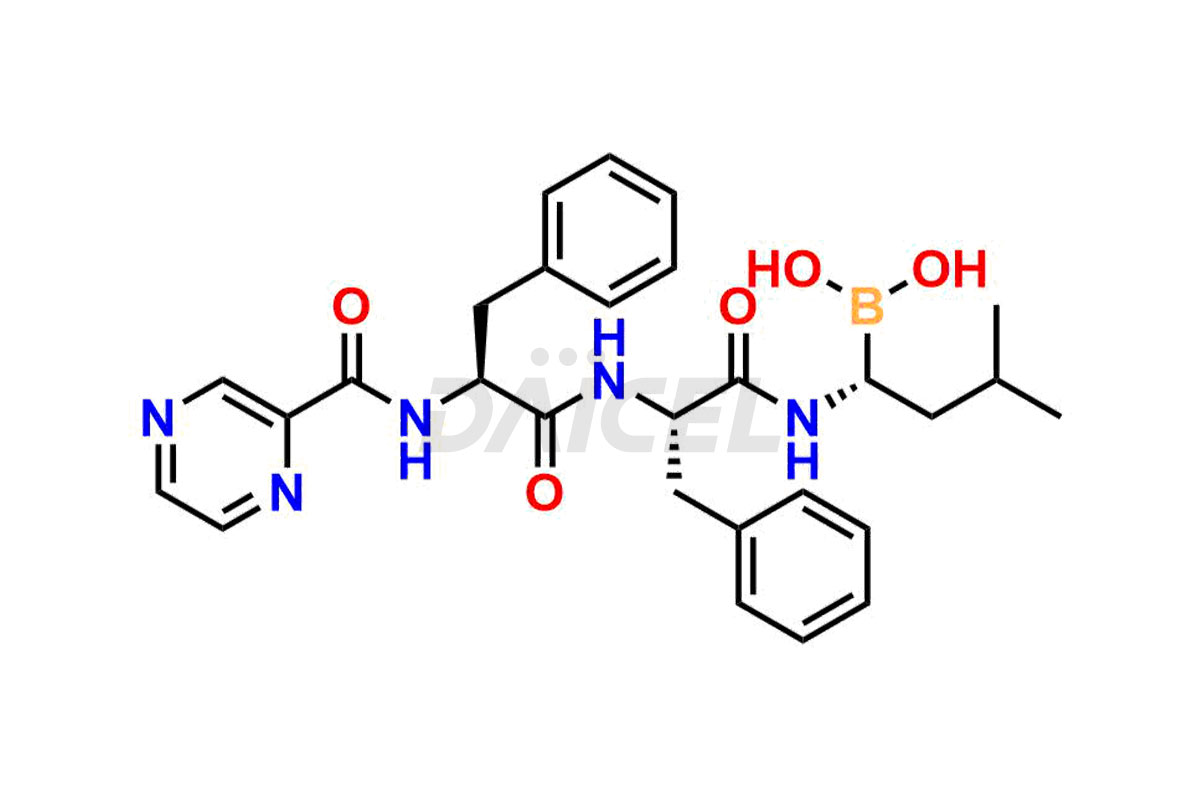
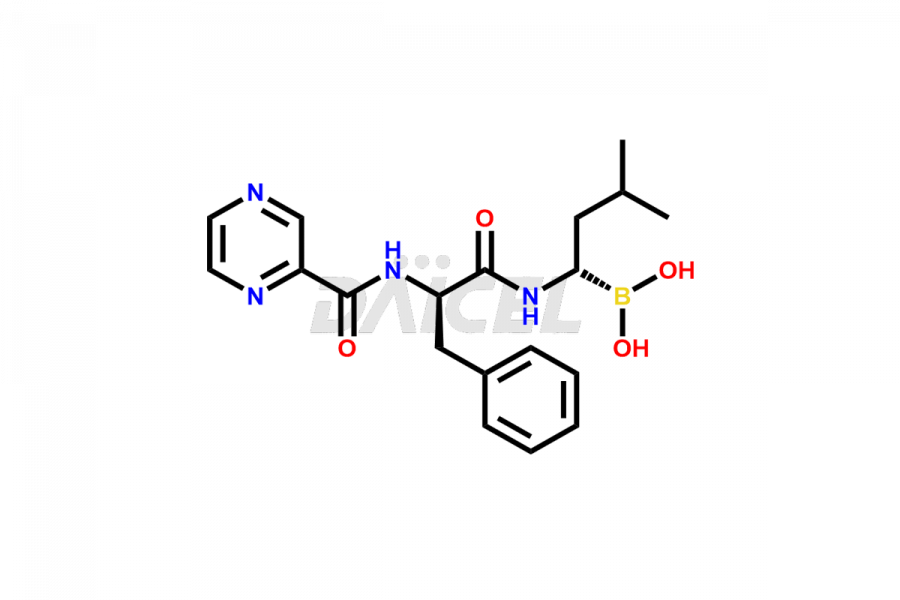
O nome químico do Bortezomibe é ácido [(1R)-3-metil-1-[[(2S)-1-oxo-3-fenil-2-[(pirazinilcarbonil)amino]propil]amino]butil]-borônico. Sua fórmula química é C19H25BN4O4, e seu peso molecular é de aproximadamente 384.2 g/mol.
O bortezomibe inibe o proteassoma 26S em células de mamíferos, o que previne a proteólise. Ele perturba os mecanismos homeostáticos que levam à morte celular e retarda o crescimento do tumor.
Impurezas e Síntese de Bortezomibe
As impurezas que se formam durante a fabricação1 processo ou armazenamento de Bortezomibe incluem produtos de degradação e impurezas relacionadas ao processo, resíduos de solventes e metais residuais. Eles podem afetar a segurança, eficácia e qualidade do medicamento. Assim, é necessário controlá-los através da implementação de medidas adequadas, como a utilização de matérias-primas de alta qualidade, a otimização do processo de fabricação, o emprego de condições de armazenamento adequadas e a realização de testes rigorosos de controle de qualidade para garantir a pureza e segurança do medicamento.
A Daicel Pharma fornece um Certificado de Análise (CoA) para padrões de impureza de Bortezomibe, incluindo impureza de ácido de Bortezomibe, impureza de amida de Bortezomibe, dímero de Bortezomibe e enantiômero de Bortezomibe. O CoA é gerado a partir de uma instalação analítica compatível com cGMP e inclui dados de caracterização abrangentes, como RMN de 1H, RMN de 13C, IR, MASSA e pureza de HPLC2. Também podemos fornecer dados de caracterização adicionais como 13C-DEPT e CHN mediante solicitação. A Daicel Pharma é capaz de criar impurezas ou produtos de degradação desconhecidos do Bortezomibe. Cada entrega possui um relatório completo de caracterização.