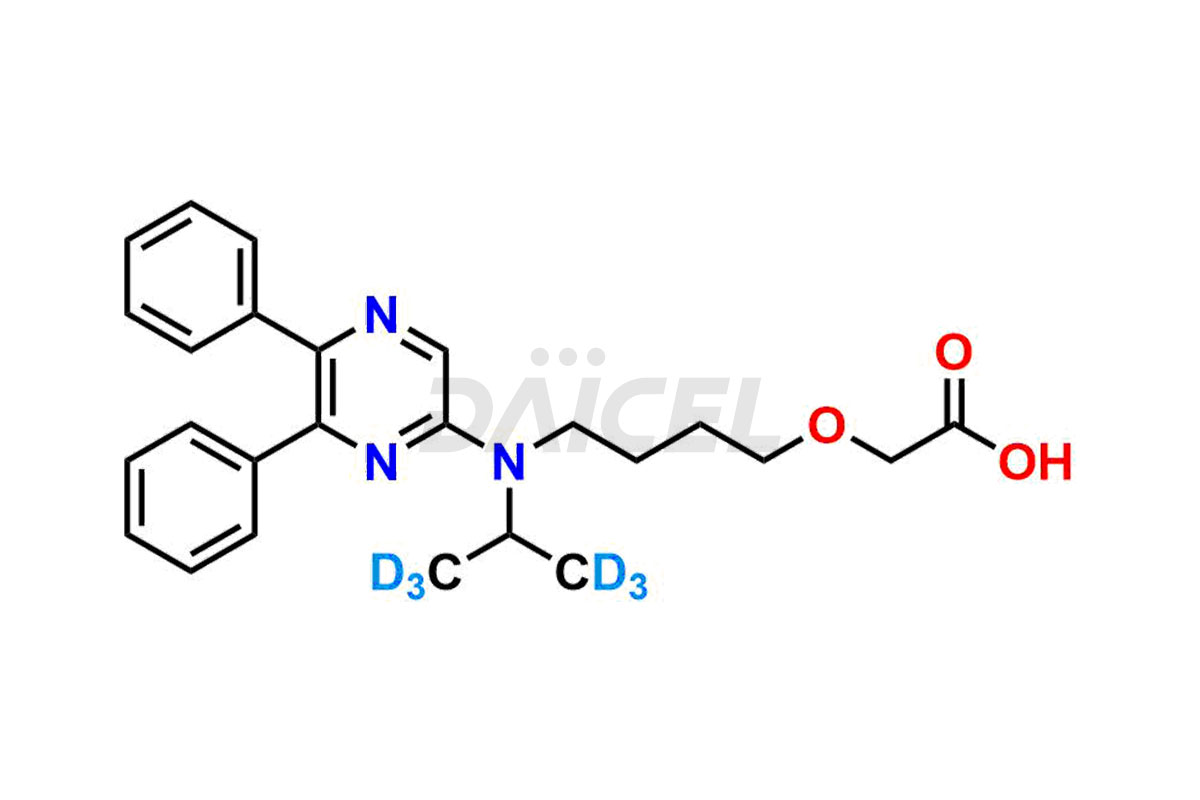
Selexipag
Referenties
- Asaki, Tetsuo; Hamamoto, Taisuke; Kuwano, Keiichi, heterocyclische samengestelde derivaten en medicijnen, Nippon Shinyaku Co., Ltd., Japan, EP1400518B1, 17 januari 2007
- Bonde, Prajakta G.; Bachhav, RS; Kalegaonkar, Somnath, Ontwikkeling en validatie van RP-HPLC-methode voor de schatting van selexipag in bulk en zijn tabletdoseringsvorm, World Journal of Pharmacy and Pharmaceutical Sciences, Volume: 11, Issue: 8, Pagina's: 2166-2175, 2022
Veelgestelde Vragen / FAQ
Waarom is de aanwezigheid van onzuiverheden een punt van zorg in Selexipag?
De aanwezigheid van onzuiverheden in Selexipag kan de kwaliteit, veiligheid en werkzaamheid aanzienlijk beïnvloeden. Afhankelijk van het type en de concentratie van onzuiverheden kunnen ze de farmacologische activiteit en stabiliteit van het geneesmiddel negatief beïnvloeden en uiteindelijk potentiële risico's voor de gezondheid van de patiënt vormen. Het is daarom cruciaal om onzuiverheden zorgvuldig te beheren en te beheersen om de optimale prestaties en veiligheid van het medicijn als farmaceutisch product te garanderen.
Hoe worden de onzuiverheden gedetecteerd en gekwantificeerd in Selexipag?
Selexipag-onzuiverheden worden beoordeeld met behulp van analytische technieken zoals de nieuwe high-performance liquid chromatography (RP-HPLC)-methode.
Welke oplosmiddelen helpen bij de analyse van Selexipag-onzuiverheden?
Methanol is het oplosmiddel dat wordt gebruikt in analytische technieken om onzuiverheden van Selexipag te scheiden en te detecteren.
Wat zijn de temperatuuromstandigheden die nodig zijn om Selexipag-onzuiverheden op te slaan?
Selexipag-onzuiverheden moeten worden bewaard bij een gecontroleerde kamertemperatuur tussen 2-8°C of zoals aangegeven op het analysecertificaat (CoA).
Let op: Producten die beschermd zijn door geldige patenten van een fabrikant worden niet te koop aangeboden in landen met patentbescherming. De verkoop van dergelijke producten vormt een inbreuk op het octrooi en de aansprakelijkheid ervan is voor risico van de koper.