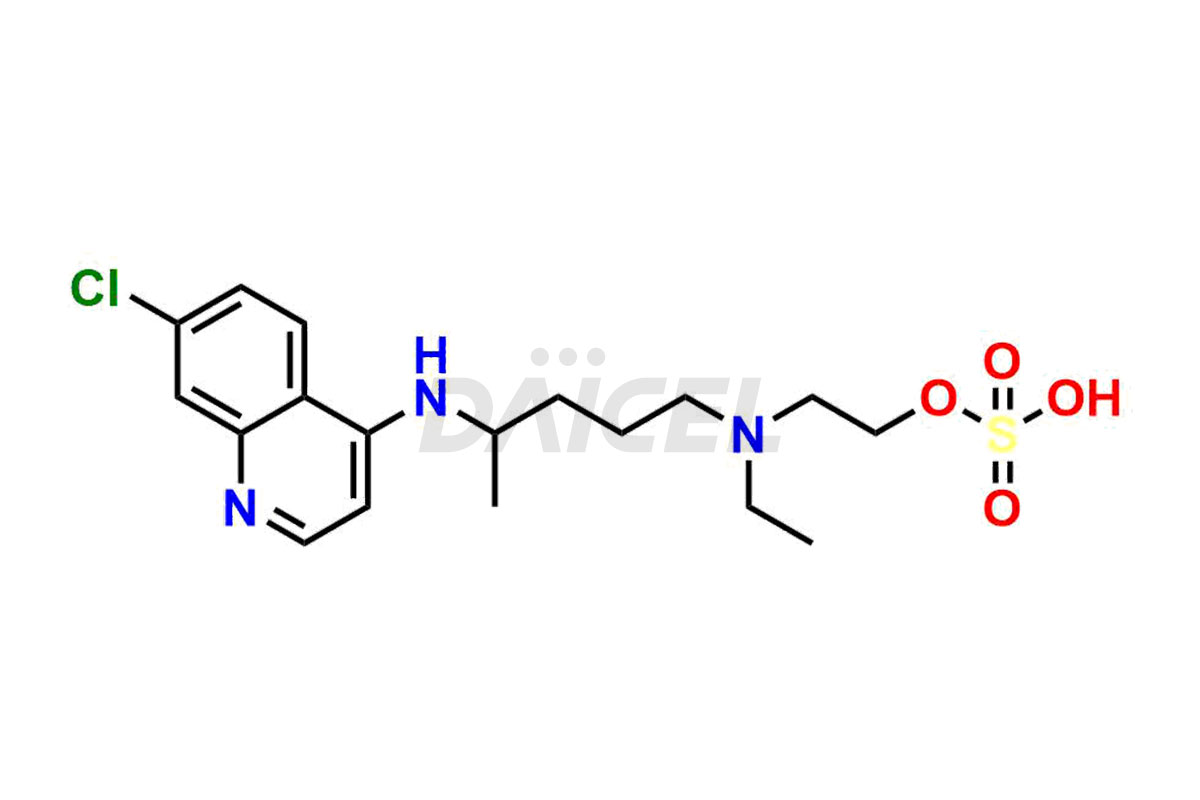
Hydroxychloroquine Sulfaat EP Onzuiverheid B
- CAT-nummer: DCTI-C-1068
- CAS-nummer 103152-84-7
- Moleculaire Formule C18H26ClN3O4S
- moleculair gewicht 415.93
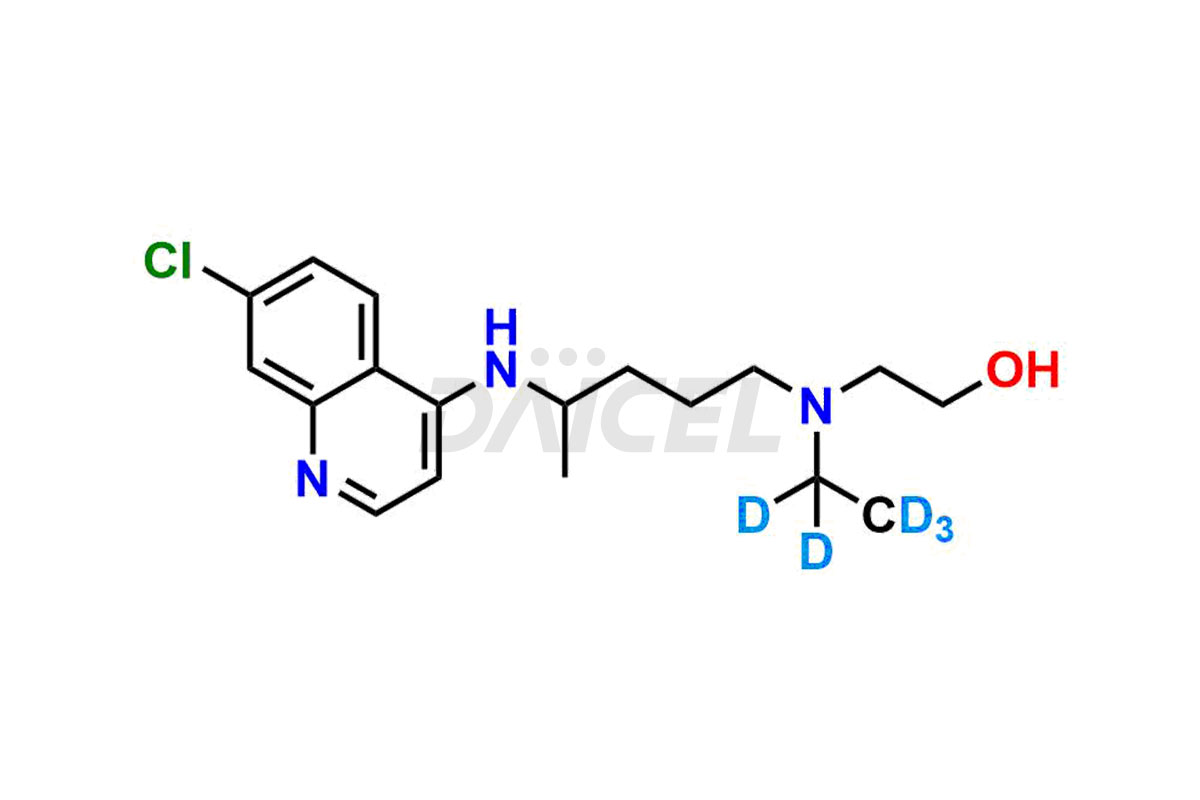
Hydroxychloroquine-D5
- CAT-nummer: DCTI-A-038
- CAS-nummer 118-42-3 (zonder label)
- Moleculaire Formule C18H21D5ClN3O
- moleculair gewicht 340.91
LADEN MEER
Je hebt alle 11 producten bekeken