Algemene informatie
bortezomib Onzuiverheden en Bortezomib
Daicel Pharma synthetiseert hoogwaardige Bortezomib-onzuiverheden, waaronder Bortezomib-zuur-onzuiverheid, Bortezomib-amide-onzuiverheid, Bortezomib-dimeer en Bortezomib-enantiomeer. Deze onzuiverheden zijn essentieel voor het evalueren van de kwaliteit, stabiliteit en veiligheid van een actief farmaceutisch ingrediënt, Bortezomib. Bovendien biedt Daicel Pharma een op maat gemaakte synthese van Bortezomib-onzuiverheden voor wereldwijde levering om aan de specifieke behoeften van onze klanten te voldoen.
bortezomib [CAS: 179324-69-7] is een antineoplastisch middel en proteasoomremmer die lymfomen en refractair multipel myeloom behandelt. Het is een gemodificeerd dipeptidylboorzuurderivaat dat multipel myeloom behandelt.
Bortezomib: gebruik en commerciële beschikbaarheid
Bortezomib is een door de FDA goedgekeurd antineoplastisch middel dat multipel myeloom behandelt. Het behandelt ook mantelcellymfoom bij patiënten die ten minste één eerdere eerstelijnsbehandeling hebben ondergaan. Velcade is de merknaam waaronder Bortezomib verkrijgbaar is.
Bortezomib Structuur en werkingsmechanisme
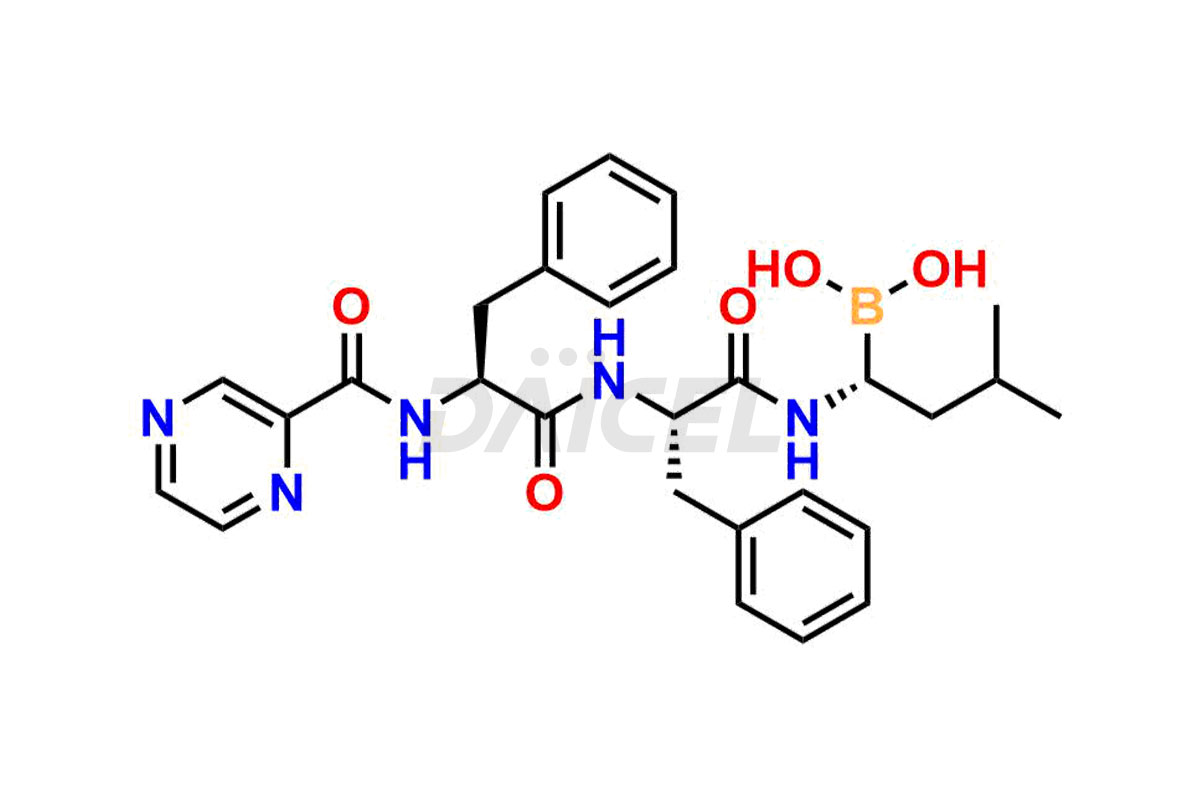
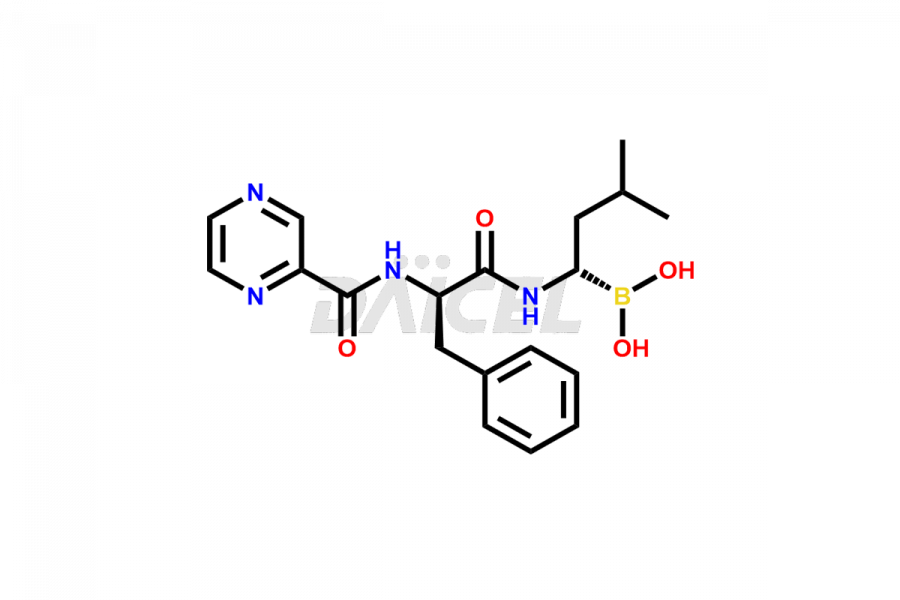
De chemische naam van Bortezomib is [(1R)-3-methyl-1-[[(2S)-1-oxo-3-fenyl-2-[(pyrazinylcarbonyl)amino]propyl]amino]butyl]boorzuur. De chemische formule is C19H25BN4O4, en het molecuulgewicht is ongeveer 384.2 g/mol.
Bortezomib remt het 26S-proteasoom in zoogdiercellen, wat proteolyse voorkomt. Het verstoort homeostatische mechanismen die leiden tot celdood en vertraagt de tumorgroei.
Bortezomib onzuiverheden en synthese
De onzuiverheden die ontstaan tijdens de productie1 proces of opslag van Bortezomib omvatten afbraakproducten en procesgerelateerde onzuiverheden, oplosmiddelresiduen en resterende metalen. Ze kunnen de veiligheid, werkzaamheid en kwaliteit van het geneesmiddel beïnvloeden. Het is dus noodzakelijk om ze te beheersen door adequate maatregelen te nemen, zoals het gebruik van hoogwaardige uitgangsmaterialen, het optimaliseren van het productieproces, het toepassen van geschikte opslagomstandigheden en het uitvoeren van strenge kwaliteitscontroletests om de zuiverheid en veiligheid van het geneesmiddel te waarborgen.
Daicel Pharma levert een analysecertificaat (CoA) voor Bortezomib-onzuiverheidsstandaarden, waaronder Bortezomib-zuur-onzuiverheid, Bortezomib-amide-onzuiverheid, Bortezomib-dimeer en Bortezomib-enantiomeer. Het CoA wordt gegenereerd vanuit een cGMP-conforme analytische faciliteit en bevat uitgebreide karakteriseringsgegevens zoals 1H NMR, 13C NMR, IR, MASS en HPLC-zuiverheid2. Op verzoek kunnen we ook aanvullende karakteriseringsgegevens geven, zoals 13C-DEPT en CHN. Daicel Pharma is in staat onbekende onzuiverheden of afbraakproducten van Bortezomib aan te maken. Elke levering heeft een volledig karakteriseringsrapport.