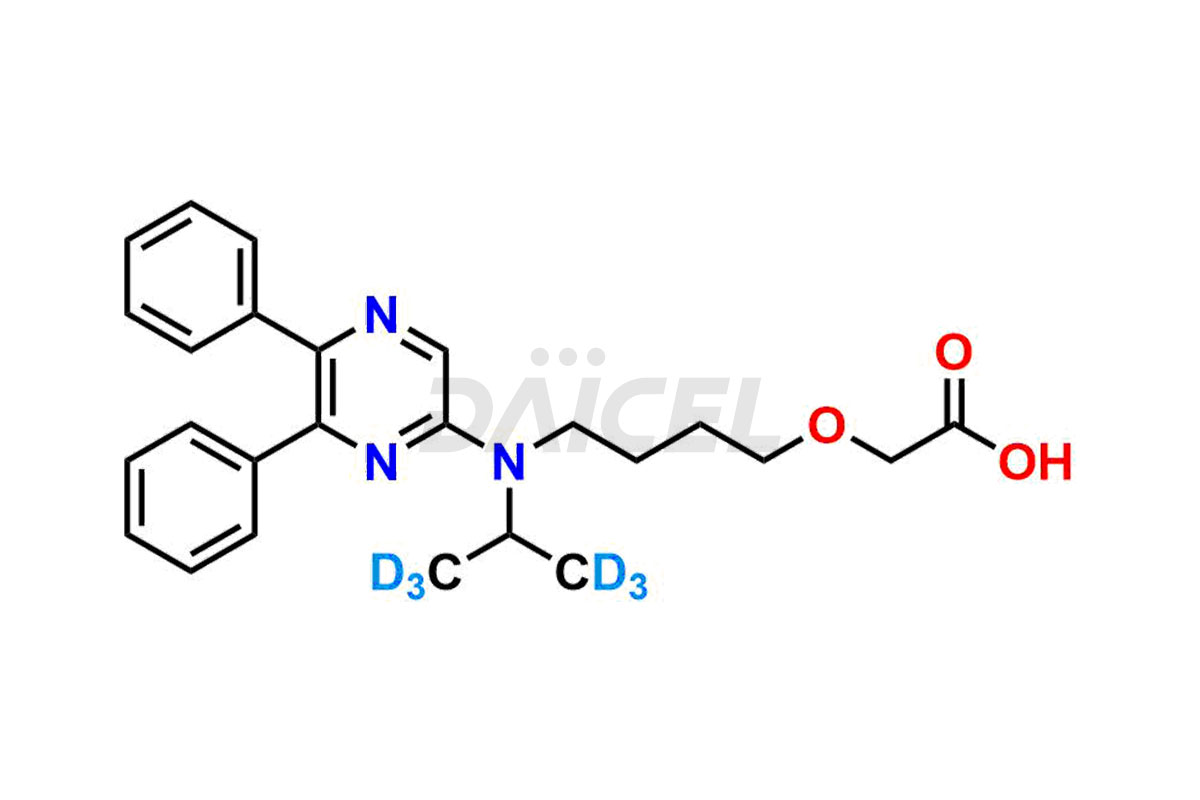
Selexipag
Riferimenti
- Asaki, Tetsuo; Hamamoto, Taisuke; Kuwano, Keiichi, Derivati composti eterociclici e medicinali, Nippon Shinyaku Co., Ltd., Giappone, EP1400518B1, 17 gennaio 2007
- Bonde, Prajakta G.; Bachhav, RS; Kalegaonkar, Somnath, Sviluppo e validazione del metodo RP-HPLC per la stima di selexipag in massa e della sua forma di dosaggio in compresse, World Journal of Pharmacy and Pharmaceutical Sciences, Volume: 11, Numero: 8, Pagine: 2166-2175, 2022
Domande frequenti
Perché la presenza di impurità è motivo di preoccupazione in Selexipag?
La presenza di impurità in Selexipag può influenzarne significativamente la qualità, la sicurezza e l'efficacia. A seconda del tipo e della concentrazione delle impurità, queste possono influenzare negativamente l'attività farmacologica e la stabilità del farmaco e, in definitiva, comportare potenziali rischi per la salute del paziente. È quindi fondamentale gestire e controllare attentamente le impurità per garantire prestazioni ottimali e sicurezza del farmaco come prodotto farmaceutico.
Come vengono rilevate e quantificate le impurità in Selexipag?
Le impurezze di Selexipag vengono valutate utilizzando tecniche analitiche come il nuovo metodo della cromatografia liquida ad alte prestazioni (RP-HPLC).
Quali solventi aiutano nell'analisi delle impurità di Selexipag?
Il metanolo è il solvente utilizzato nelle tecniche analitiche per separare e rilevare le impurità di Selexipag.
Quali sono le condizioni di temperatura richieste per conservare Selexipag Impurities?
Le impurità di Selexipag devono essere conservate a temperatura ambiente controllata compresa tra 2 e 8°C o come indicato sul Certificato di analisi (CoA).
Nota: i prodotti protetti da brevetti validi di un produttore non sono offerti in vendita nei paesi che dispongono di protezione brevettuale. La vendita di tali prodotti costituisce una violazione di brevetto e la relativa responsabilità è a rischio dell'acquirente.