Cefixima EP Impurità F
- Numero CAT DCTI-C-104
- Numero CAS 79368-95-9
- Formula molecolare C18H19N5O7S2
- Peso molecolare 481.5
Cefixime Impurità-A
- NUMERO DI GATTO DCTI-C-2216
- NUMERO CAS 1614255-90-1
- FORMULA MOLECOLARE C16H17N5O8S2
- PESO MOLECOLARE 471.46
Daicel Pharma sintetizza impurità di Cefixime di alta qualità come Cefixime EP Impurity F e Cefixime Impurity-A, che sono cruciali nell'analisi della qualità, stabilità e sicurezza biologica del principio farmaceutico attivo Cefixime. Inoltre, Daicel Pharma offre sintesi personalizzate di impurità di cefixima e le consegna a livello globale.
Cefixime [CAS: 79350-37-1] è un antibiotico derivato semisinteticamente da un fungo chiamato Cephalosporium acremonium. È un antibiotico cefalosporinico di terza generazione con un ampio spettro di attività contro diversi tipi di batteri.
La cefixima è un antibiotico ad ampio spettro efficace contro varie infezioni causate da microrganismi sensibili. Queste infezioni comprendono bronchite acuta ed esacerbazioni acute di bronchite cronica causate da Streptococcus pneumoniae e Haemophilus influenzae (ceppi beta-lattamasi positivi e negativi). Inoltre, tratta la gonorrea non complicata causata da Neisseria gonorrhoeae (ceppi produttori di penicillinasi e non penicillinasi). Inoltre, aiuta nel trattamento dell'otite media causata da Haemophilus influenzae (ceppi beta-lattamasi positivi e negativi), Moraxella catarrhalis (per lo più beta-lattamasi positivi) e S. pyogenes. Inoltre, tratta le infezioni non complicate del tratto urinario causate da Escherichia coli e Proteus mirabilis. Il farmaco è disponibile sotto forma di compressa orale con il marchio Suprax.
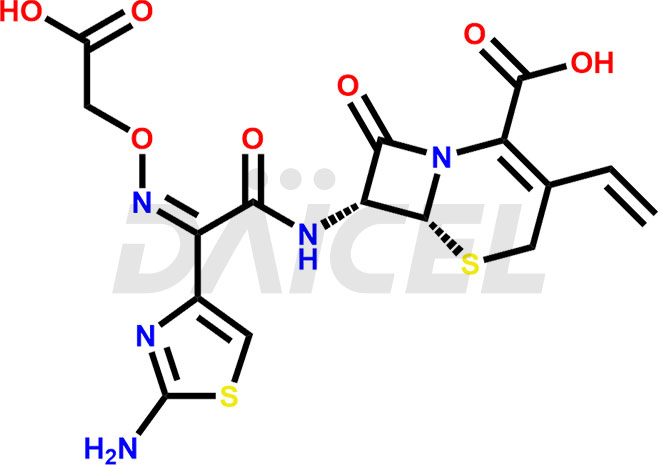
Il nome chimico della cefixima è (6R,7R)-7-[[(2Z)-2-(2-Ammino-4-tiazolil)-2-[(carbossimetossi)immino]acetil]ammino]-3-etenil-8 acido -osso-5-tia-1-azabiciclo[4.2.0]ott-2-ene-2-carbossilico. La sua formula chimica è C16H15N5O7S2, e il suo peso molecolare è di circa 453.5 g/mol.
Come altre cefalosporine, la cefixima inibisce la sintesi della parete cellulare dei batteri. È altamente stabile in presenza di enzimi beta-lattamasi.
Le impurità sono sostanze che sono involontariamente presenti nei prodotti farmaceutici e possono influenzarne la qualità, l'efficacia e la sicurezza. Cefixima1, un antibiotico ampiamente utilizzato, non fa eccezione e può contenere impurità che derivano da varie fonti. Queste impurità includono composti correlati come intermedi, sottoprodotti della sintesi della cefixima e prodotti di degradazione che si formano durante lo stoccaggio o in condizioni sfavorevoli. Pertanto, i produttori devono sviluppare e convalidare metodi analitici per rilevare e quantificare accuratamente le impurità presenti nella cefixima. I produttori possono ridurre al minimo la formazione di impurità e migliorare la qualità della cefixima implementando strategie di controllo e ottimizzazione del processo, come l'utilizzo di materiali di partenza di alta qualità, l'ottimizzazione delle condizioni di reazione e l'utilizzo di tecniche di purificazione appropriate. In definitiva, garantire la purezza della cefixima è essenziale per garantirne la sicurezza e l’efficacia per i pazienti.
Daicel offre un certificato di analisi (CoA) rilasciato da una struttura analitica conforme a cGMP per gli standard di impurità di Cefixime, Cefixime EP Impurity F e Cefixime Impurity-A. Il CoA include dati di caratterizzazione completi, come 1H NMR, 13C NMR, IR, MASS e purezza HPLC2. Forniamo anche 13C-DEPT e CHN su richiesta. Forniamo un rapporto completo di caratterizzazione alla consegna. Daicel ha la tecnologia e l'esperienza per preparare qualsiasi impurità sconosciuta o prodotto di degradazione della Cefixima.
Le impurità della cefixima possono ridurre la durata di conservazione del farmaco accelerandone la degradazione e riducendone la stabilità.
L'acqua viene utilizzata come solvente nell'analisi delle impurità della Cefixima.
Le impurità di cefixima devono essere conservate a una temperatura ambiente controllata compresa tra 2 e 8 ⁰C o come indicato sul Certificato di analisi (CoA).
Nota: i prodotti protetti da brevetti validi di un produttore non sono offerti in vendita nei paesi che dispongono di protezione brevettuale. La vendita di tali prodotti costituisce una violazione di brevetto e la relativa responsabilità è a rischio dell'acquirente.