Informazione generale
bortezomib Impurezze e Bortezomib
Daicel Pharma sintetizza impurità di Bortezomib di alta qualità, tra cui l'impurità acida di Bortezomib, l'impurità di Bortezomib ammidica, il dimero di Bortezomib e l'enantiomero di Bortezomib. Queste impurezze sono essenziali per valutare la qualità, la stabilità e la sicurezza di un ingrediente farmaceutico attivo, Bortezomib. Inoltre, Daicel Pharma offre una sintesi personalizzata delle impurità di Bortezomib da distribuire a livello globale per soddisfare le esigenze specifiche dei nostri clienti.
bortezomib [CAS: 179324-69-7] è un agente antineoplastico e un inibitore del proteasoma che tratta i linfomi e il mieloma multiplo refrattario. È un derivato modificato dell'acido dipeptidilboronico che tratta il mieloma multiplo.
Bortezomib: uso e disponibilità commerciale
Bortezomib è un agente antineoplastico approvato dalla FDA per il trattamento del mieloma multiplo. Tratta anche il linfoma mantellare nei pazienti sottoposti ad almeno un precedente trattamento di prima linea. Velcade è il marchio con cui è disponibile Bortezomib.
Struttura e meccanismo d'azione di Bortezomib
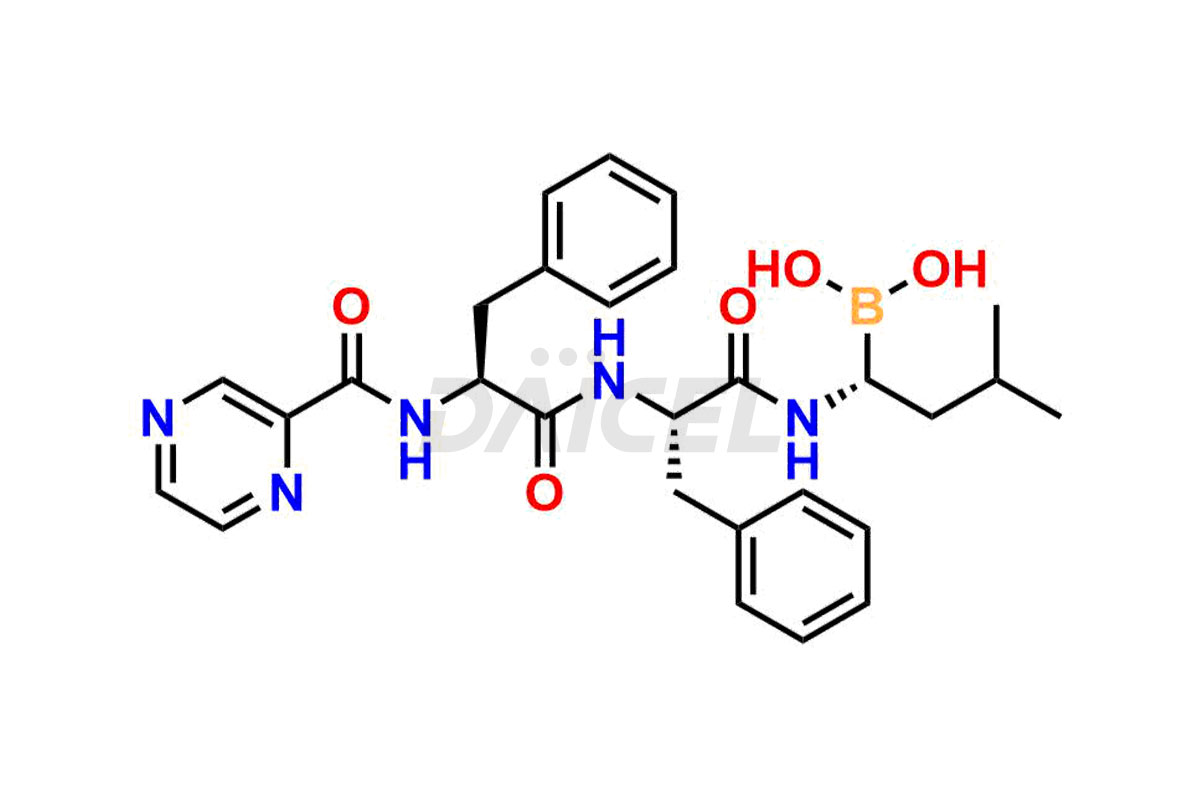
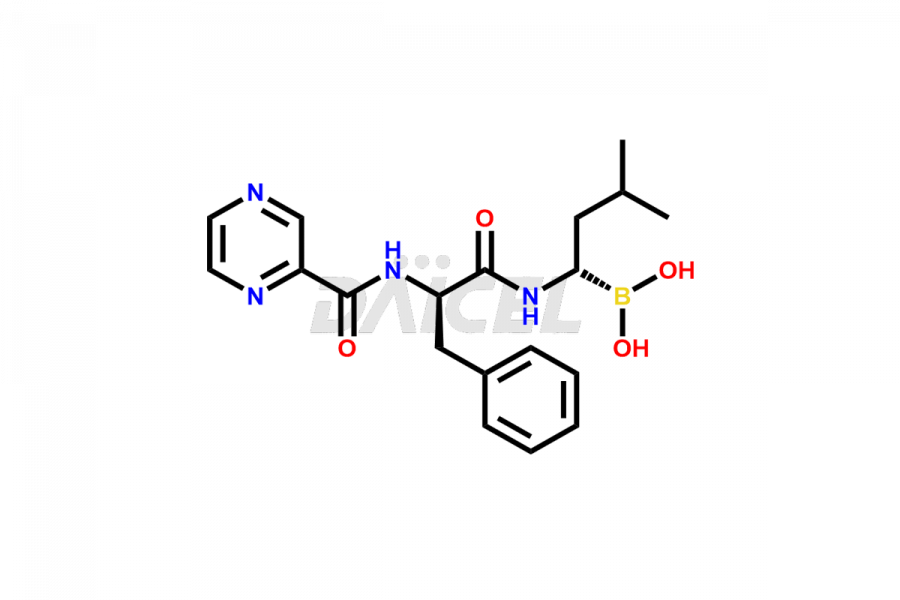
Il nome chimico di Bortezomib è acido [(1R)-3-metil-1-[[(2S)-1-osso-3-fenil-2-[(pirazinilcarbonil)ammino]propil]ammino]butil]-boronico. La sua formula chimica è C19H25BN4O4, e il suo peso molecolare è di circa 384.2 g/mol.
Bortezomib inibisce il proteasoma 26S nelle cellule di mammifero, prevenendo la proteolisi. Interrompe i meccanismi omeostatici che portano alla morte cellulare e ritarda la crescita del tumore.
Impurezze e sintesi di Bortezomib
Le impurità che si formano durante la lavorazione1 processo o stoccaggio di Bortezomib includono prodotti di degradazione e impurità legate al processo, residui di solventi e metalli residui. Possono influenzare la sicurezza, l’efficacia e la qualità del farmaco. Pertanto, è necessario controllarli implementando misure adeguate come l’utilizzo di materiali di partenza di alta qualità, l’ottimizzazione del processo di produzione, l’impiego di condizioni di conservazione adeguate e lo svolgimento di rigorosi test di controllo qualità per garantire la purezza e la sicurezza del prodotto farmaceutico.
Daicel Pharma fornisce un certificato di analisi (CoA) per gli standard di impurità di Bortezomib, tra cui l'impurezza acida di Bortezomib, l'impurità di Bortezomib amide, il dimero di Bortezomib e l'enantiomero di Bortezomib. Il CoA viene generato da una struttura analitica conforme a cGMP e include dati di caratterizzazione completi come 1H NMR, 13C NMR, IR, MASS e purezza HPLC2. Su richiesta possiamo anche fornire dati di caratterizzazione aggiuntivi come 13C-DEPT e CHN. Daicel Pharma è in grado di creare impurità sconosciute o prodotti di degradazione del Bortezomib. Ogni consegna ha un rapporto di caratterizzazione completo.