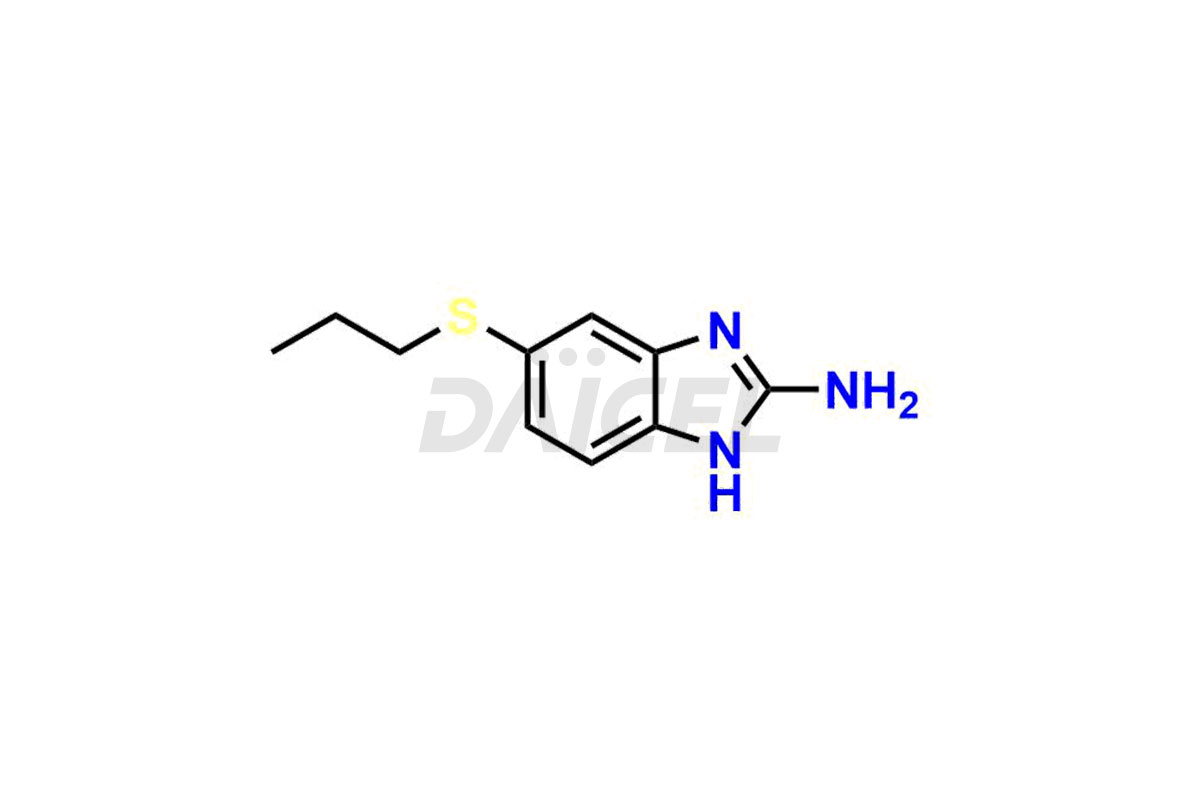
Amino Albendazolo (Albendazolo EP Impurità A)
- Numero CAT DCTI-C-290
- Numero CAS 80983-36-4
- Formula molecolare C10H13N3S
- Peso molecolare 207.3
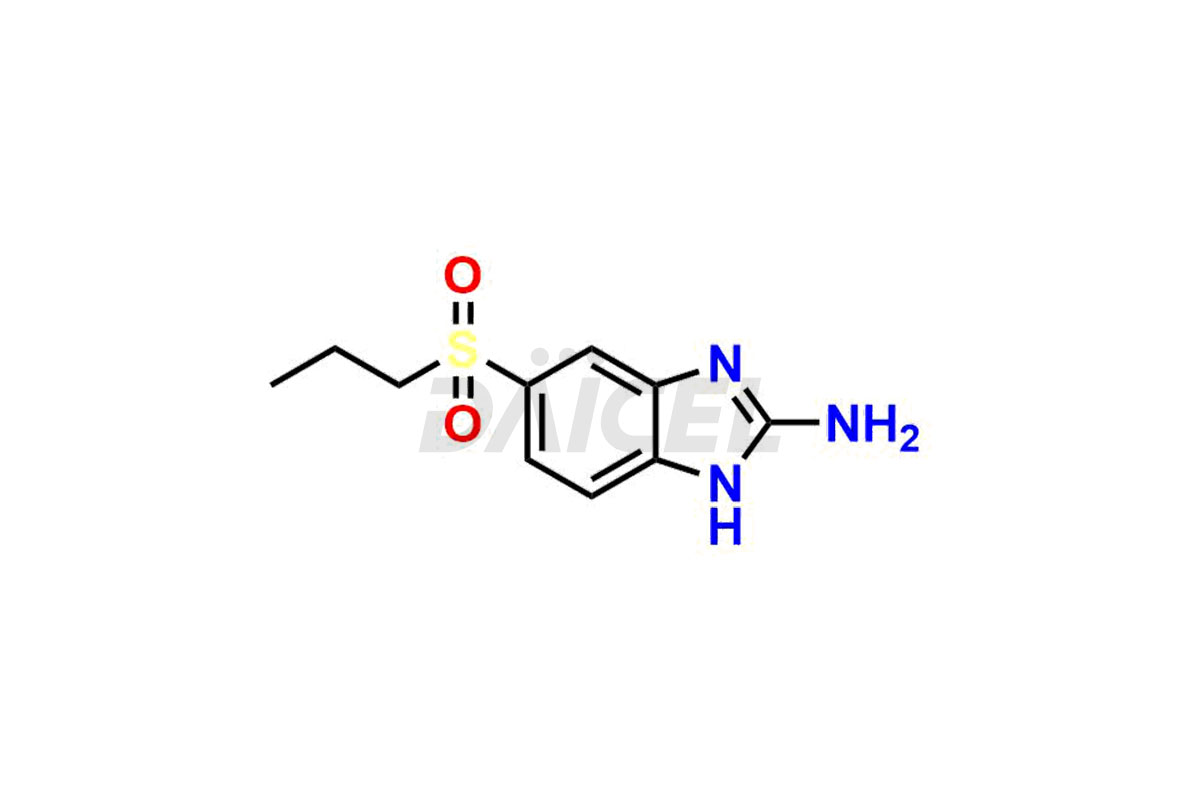
Amino Albendazolo Sulfone (Albendazolo EP Impurità D)
- Numero CAT DCTI-C-289
- Numero CAS 80983-34-2
- Formula molecolare C10H13N3O2S
- Peso molecolare 239.29
Caricare più
Hai visualizzato tutti i 11 prodotti