Abacavir
Informazione generale
Impurità di abacavir e abacavir
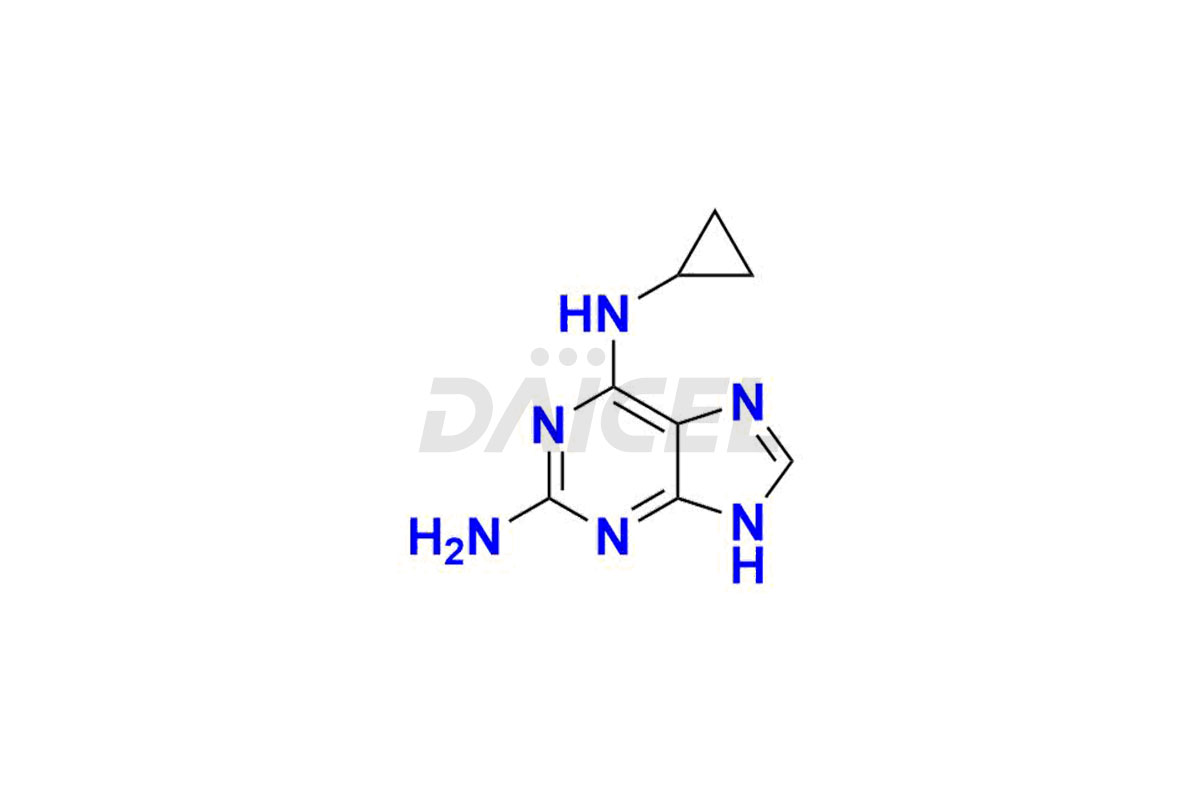
Daicel Pharma sintetizza l'impurità di abacavir di alta qualità, N6-ciclopropil-9H-purin-2,6-diammina, che è cruciale nell'analisi della qualità, della stabilità e della sicurezza biologica dell'ingrediente farmaceutico attivo Abacavir. Inoltre, Daicel Pharma offre sintesi personalizzate delle impurità di abacavir e le consegna a livello globale.
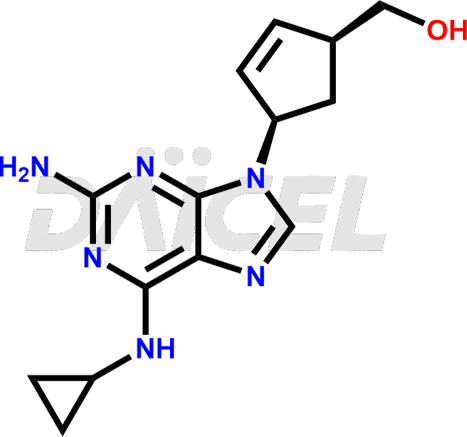
Abacavir [CAS: 136470-78-5] è un analogo nucleosidico carbociclico sintetico che tratta l'infezione da HIV negli adulti, nei bambini e nei neonati. Si combina con altri farmaci per l'HIV, in particolare solfato e altri farmaci antiretrovirali. Abacavir funziona come un inibitore nucleosidico della trascrittasi inversa (NRTI), che aiuta a combattere l'HIV inibendo l'attività dell'enzima trascrittasi inversa dell'HIV-1 necessario affinché il virus si replichi.
Abacavir: uso e disponibilità commerciale
Abacavir è un farmaco approvato dalla FDA per il trattamento dell’infezione da HIV-1. Viene utilizzato in combinazione con altri farmaci antiretrovirali, come abacavir/lamivudina/zidovudina, abacavir/dolutegravir/lamivudina e abacavir/lamivudina. Abacavir è classificato come un inibitore nucleosidico della trascrittasi inversa (NRTI) e può essere somministrato per via orale sotto forma di compressa o soluzione. I nomi commerciali di Abacavir includono Epzicom (combinazione di Abacavir-Lamivudina), Triumeq (combinazione di Abacavir-Lamivudina-Dolutegravir), Trizivir (combinazione di Abacavir-Lamivudina-Zidovudina) e Ziagen.
Struttura e meccanismo d'azione di abacavir 
Il nome chimico di Abacavir è (1S,4R)-4-[2-Ammino-6-(ciclopropilammino)-9H-purin-9-il]-2-ciclopentene-1-metanolo. La sua formula chimica è C14H18N6O, e il suo peso molecolare è di circa 286.33 g/mol.
Abacavir viene convertito nel suo metabolita attivo, Carbovir trifosfato. È un analogo della deossiguanosina-5¢-trifosfato (dGTP). Inibisce l'attività della trascrittasi inversa (RT) dell'HIV-1.
Impurità e sintesi di abacavir
Le impurità di abacavir possono essere classificate in base ai materiali di partenza, al processo di reazione o alla degradazione della sostanza farmaceutica. Le impurità formate possono derivare dal processo sintetico1, fasi di purificazione o condizioni di conservazione. Possono influenzare la qualità, la sicurezza e l’efficacia del farmaco. Il monitoraggio e l'analisi regolari aiutano a garantire che i livelli di impurità rimangano entro limiti accettabili e non rappresentino un rischio per i pazienti.
Daicel fornisce un certificato di analisi (CoA) per lo standard di impurità di abacavir, N6-ciclopropil-9H-purin-2,6-diammina. Il CoA viene emesso da una struttura analitica conforme a cGMP e contiene dati di caratterizzazione completi, come 1H NMR, 13C NMR, IR, MASS e purezza HPLC2. Ulteriori dati di caratterizzazione, come 13C-DEPT e CHN, possono essere forniti su richiesta. Daicel può anche preparare qualsiasi impurità sconosciuta o prodotto di degradazione di Abacavir. Forniamo un rapporto completo di caratterizzazione alla consegna.
Riferimenti
- Daluge, Susan Mary, Therapeutic nucleosides, Wellcome Foundation Ltd., Regno Unito, US5034394A, 23 luglio 1991
- Veldkamp, AI; Sparidani, RW; Hoetelmans, RMW; Beijnen, JH, Determinazione quantitativa di abacavir (1592U89), un nuovo inibitore nucleosidico della trascrittasi inversa, nel plasma umano mediante cromatografia liquida isocratica a fase inversa ad alte prestazioni con rilevamento ultravioletto, Journal of Chromatography B: Biomedical Sciences and Applications, Volume: 736, Numero: 1 + 2, Pagine: 123-128, 1999
Domande frequenti
Qual è la fonte delle impurità di abacavir?
La fonte delle impurità di abacavir può includere materie prime, solventi, reagenti e prodotti di degradazione formati durante la produzione o la conservazione del prodotto farmaceutico.
Come vengono rilevate e quantificate le impurità presenti in Abacavir?
Le impurità di abacavir vengono rilevate e quantificate utilizzando tecniche cromatografiche e spettroscopiche, come HPLC, UPLC e LC-MS.
Come vengono monitorate le impurità di abacavir?
Le impurità di abacavir vengono monitorate attraverso test regolari della sostanza farmaceutica e del prodotto durante la produzione e per tutta la sua durata di conservazione.
Quali sono le condizioni di temperatura richieste per conservare le impurità di abacavir?
Le impurezze di abacavir vengono conservate a una temperatura ambiente controllata compresa tra 2 e 8 ⁰C o come indicato sul Certificato di Analisi (CoA).
Nota: i prodotti protetti da brevetti validi di un produttore non sono offerti in vendita nei paesi che dispongono di protezione brevettuale. La vendita di tali prodotti costituisce una violazione di brevetto e la relativa responsabilità è a rischio dell'acquirente.