Charger plus
Vous avez vu 9 sur 64 articles
Daicel Pharma synthétise des impuretés de ténofovir de haute qualité comme le (S)-ténofovir monohydrate, la 9-(2-hydroxypropyl)adénine, le diéthyl-p-toluène sulfonyloxyméthylphosphonate, l'hydroxy méthyle ténofovir disoproxil, et plus encore, qui sont cruciaux dans l'analyse de la qualité, la stabilité et la sécurité biologique de l'ingrédient pharmaceutique actif Ténofovir. De plus, Daicel Pharma propose une synthèse personnalisée des impuretés du ténofovir et les livre dans le monde entier.
Le ténofovir [CAS : 147127/20/6] est un médicament qui traite le VIH en association avec d'autres médicaments. De plus, il traite l’infection par le virus de l’hépatite B (VHB). C'est un analogue nucléotidique acyclique de l'adénosine.
Le ténofovir traite plusieurs infections virales comme le VIH, le virus de l'herpès simplex-2 et le virus de l'hépatite B. Il est disponible par voie orale sous deux formes, le ténofovir alafénamide et le ténofovir disoproxil. Le ténofovir est un médicament de première intention contre le syndrome d'immunodéficience acquise et l'infection chronique par l'hépatite B. C'est un ingrédient actif de nombreux médicaments, tels que Viread, Truvada, Atripla, Biktarvy, Cimduo, Complera, etc.
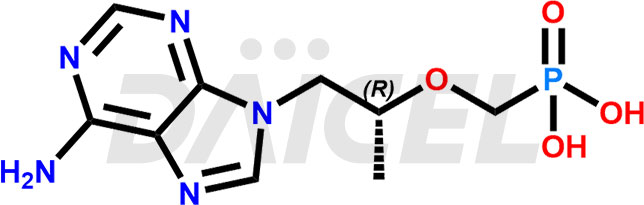
Le nom chimique du ténofovir est l'acide ([[(2R)-1-(6-Amino-9H-purin-9-yl)propan-2-yl]oxy]méthyl)phosphonique. Sa formule chimique est C9H14N5O4P, et son poids moléculaire est d'environ 287.21 g/mol.
Le ténofovir diphosphate inhibe l'activité de la transcriptase inverse du VIH en entrant en compétition avec la désoxyadénosine 5'-triphosphate et en l'incorporant dans l'ADN.
Des impuretés peuvent apparaître pendant la production1,2 du Ténofovir qui peut être nocif et nécessiter une surveillance et un contrôle stricts. Ces impuretés sont influencées par des facteurs, des conditions de réaction, des conditions de stockage et la qualité des matières premières utilisées lors de la fabrication. Ainsi, il est essentiel de veiller à ce que des mesures de contrôle de qualité appropriées soient en place tout au long du processus de production pour garantir la pureté et la sécurité du produit final.
Daicel fournit un certificat d'analyse (CoA) pour les normes d'impuretés du ténofovir, notamment le (S)-ténofovir monohydrate, la 9-(2-hydroxypropyl)adénine, le diéthyl-p-toluène sulfonyloxyméthylphosphonate, l'hydroxyméthylténofovir disoproxil, et plus encore. Le CoA est émis par une installation d'analyse conforme aux BPF et contient des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.3. Des données de caractérisation supplémentaires, telles que 13C-DEPT et CHN, peuvent être fournies sur demande. Daicel peut également préparer toute impureté ou produit de dégradation inconnu du ténofovir. Nous remettons un rapport de caractérisation complet à la livraison.
Les impuretés généralement trouvées dans le ténofovir comprennent des substances apparentées, telles que des impuretés liées au processus et des produits de dégradation.
Les impuretés du ténofovir sont analysées par chromatographie liquide à haute performance (HPLC), qui sépare les impuretés de la substance médicamenteuse et quantifie leurs concentrations.
Les impuretés du ténofovir sont éliminées grâce à diverses méthodes de purification, telles que la cristallisation et la chromatographie sur colonne. La mesure dans laquelle l'élimination des impuretés dépend de leurs propriétés chimiques et de leur concentration.
Les impuretés du ténofovir sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.