Le tamoxifène
Renseignements généraux
Impuretés du tamoxifène et tamoxifène
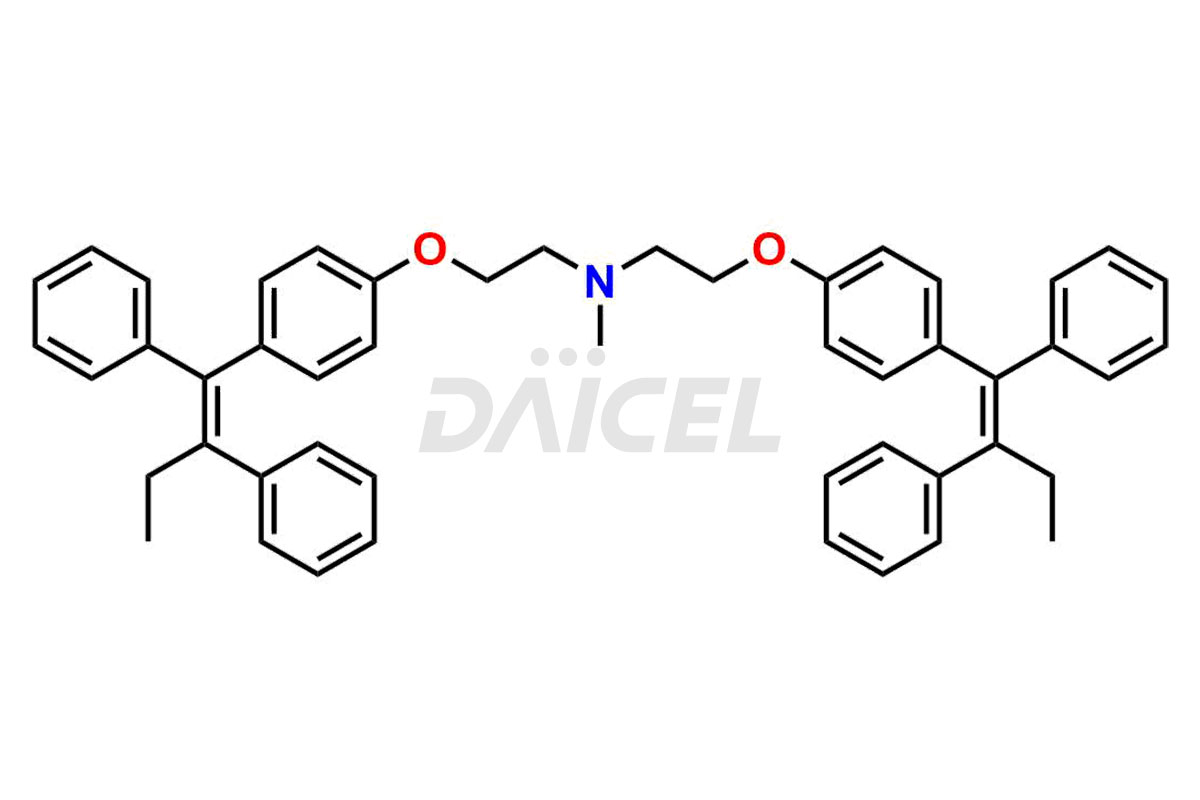
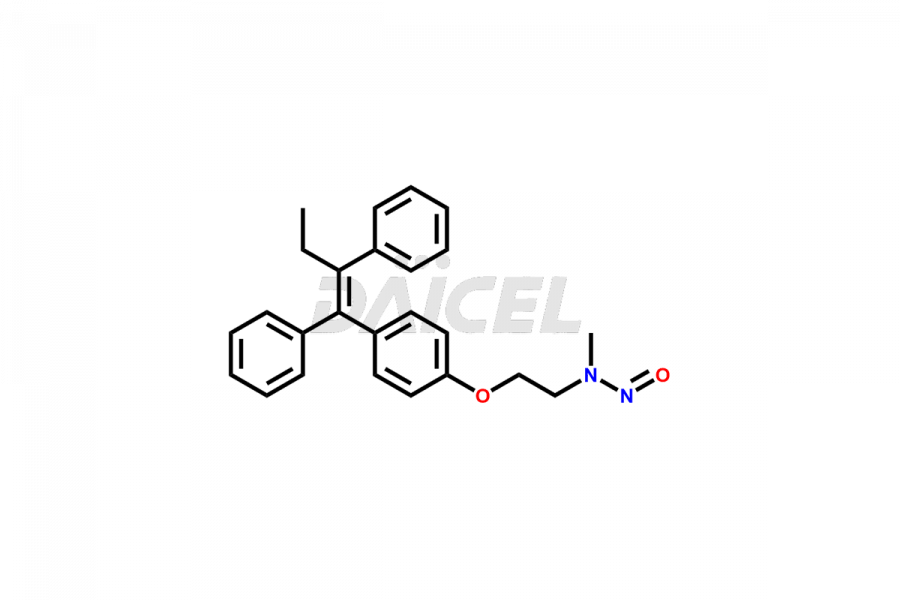
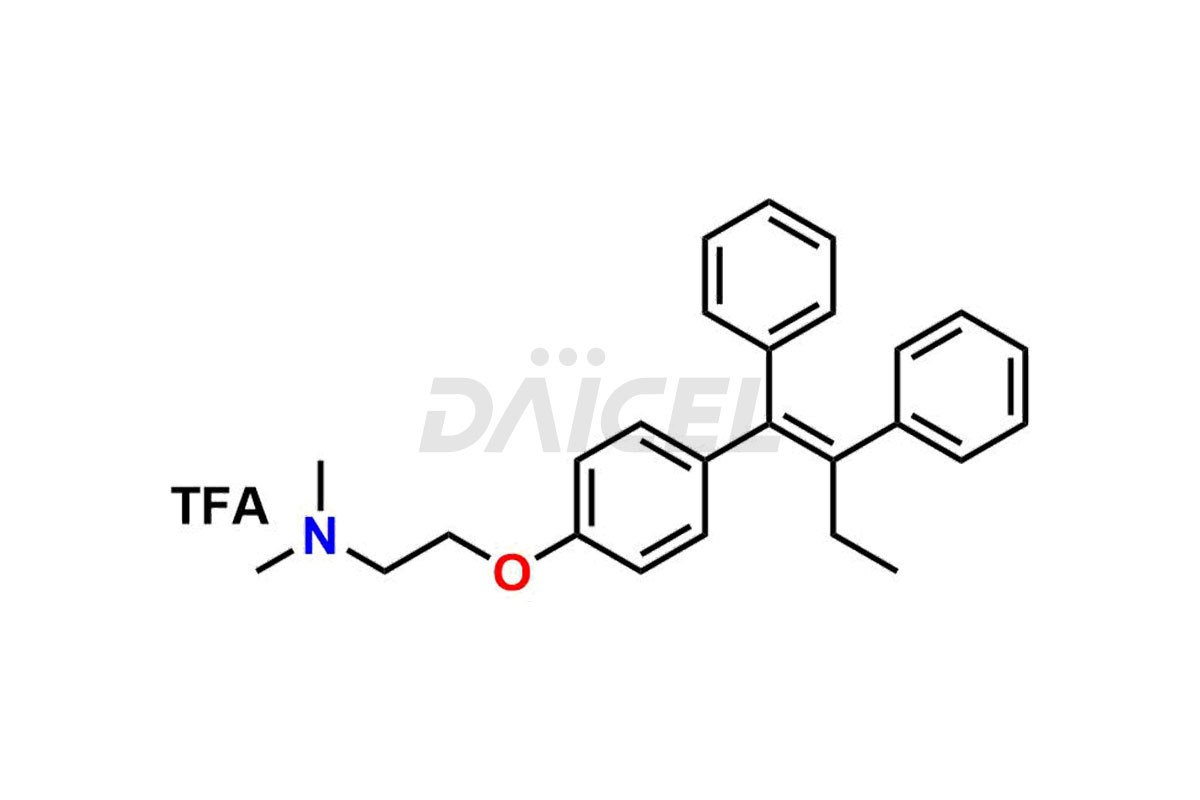
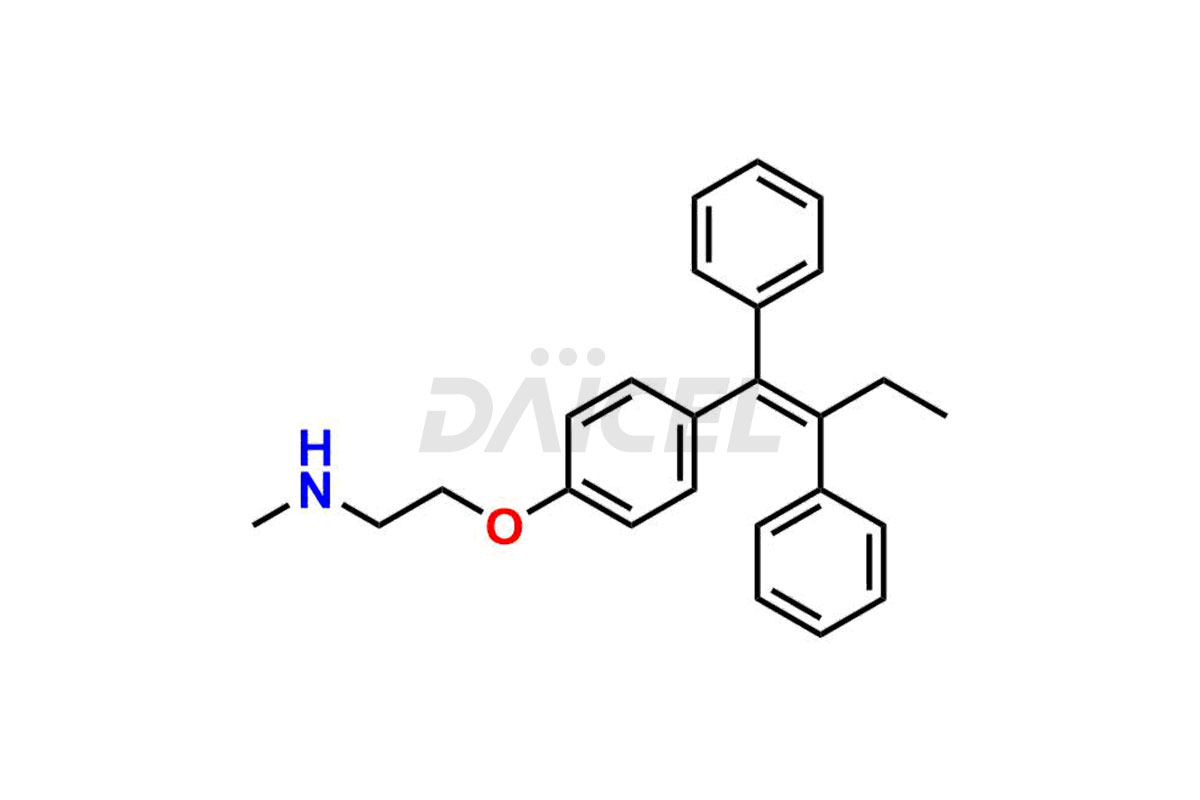
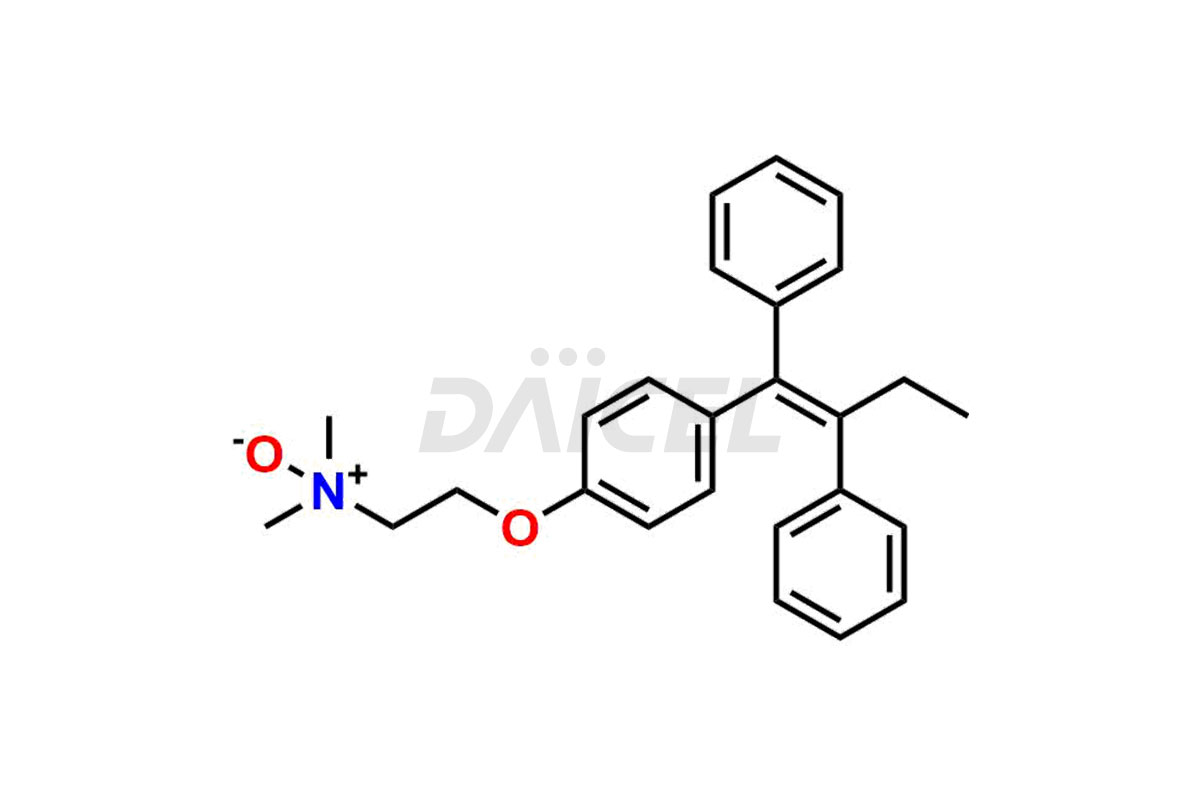
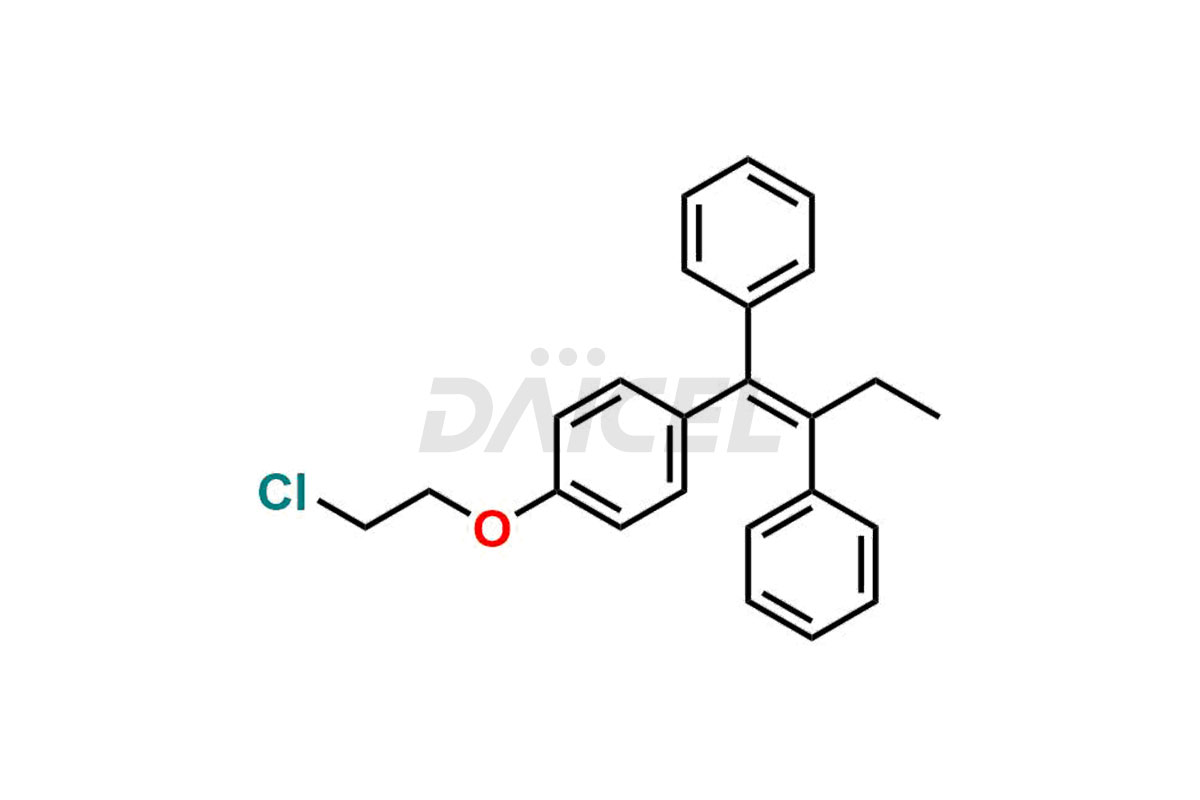
Daicel Pharma fournit une large sélection d'impuretés uniques de tamoxifène, notamment le bis-tamoxifène, l'impureté A du tamoxifène, l'impureté D du tamoxifène, l'impureté F du tamoxifène, le N-oxyde de tamoxifène et la chloroléfine Z. Ces impuretés sont essentielles à l’évaluation de la qualité, de la stabilité et de la sécurité biologique de l’ingrédient pharmaceutique actif tamoxifène. De plus, Daicel Pharma peut synthétiser les impuretés du tamoxifène en fonction des exigences spécifiques des clients, garantissant ainsi une livraison fiable dans le monde entier.
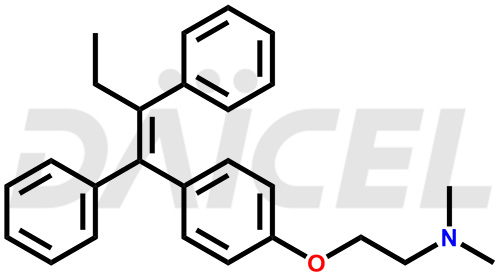
Le tamoxifène [CAS : 10540/29/1] est un dérivé du triphényléthylène qui traite le cancer du sein chez les adultes atteints de tumeurs positives aux récepteurs des œstrogènes. Il s’agit également d’un traitement adjuvant pour le cancer du sein à récepteurs d’œstrogènes positifs à un stade précoce chez l’adulte.
Tamoxifène : utilisation et disponibilité commerciale
Le tamoxifène, un œstrogène faible non stéroïdien, traite le cancer du sein à tous les stades chez des patientes spécifiques. Il est destiné au traitement palliatif des femmes préménopausées atteintes d'une maladie à récepteurs d'œstrogènes positifs (ER-positifs). Le tamoxifène réduit également le risque de cancer du sein invasif après une intervention chirurgicale et une radiothérapie chez les femmes adultes diagnostiquées avec un carcinome canalaire in situ.
Le tamoxifène est disponible sous Nolvadex et Soltamox, qui contiennent l'ingrédient actif, le tamoxifène.
Structure et mécanisme d'action du tamoxifène 
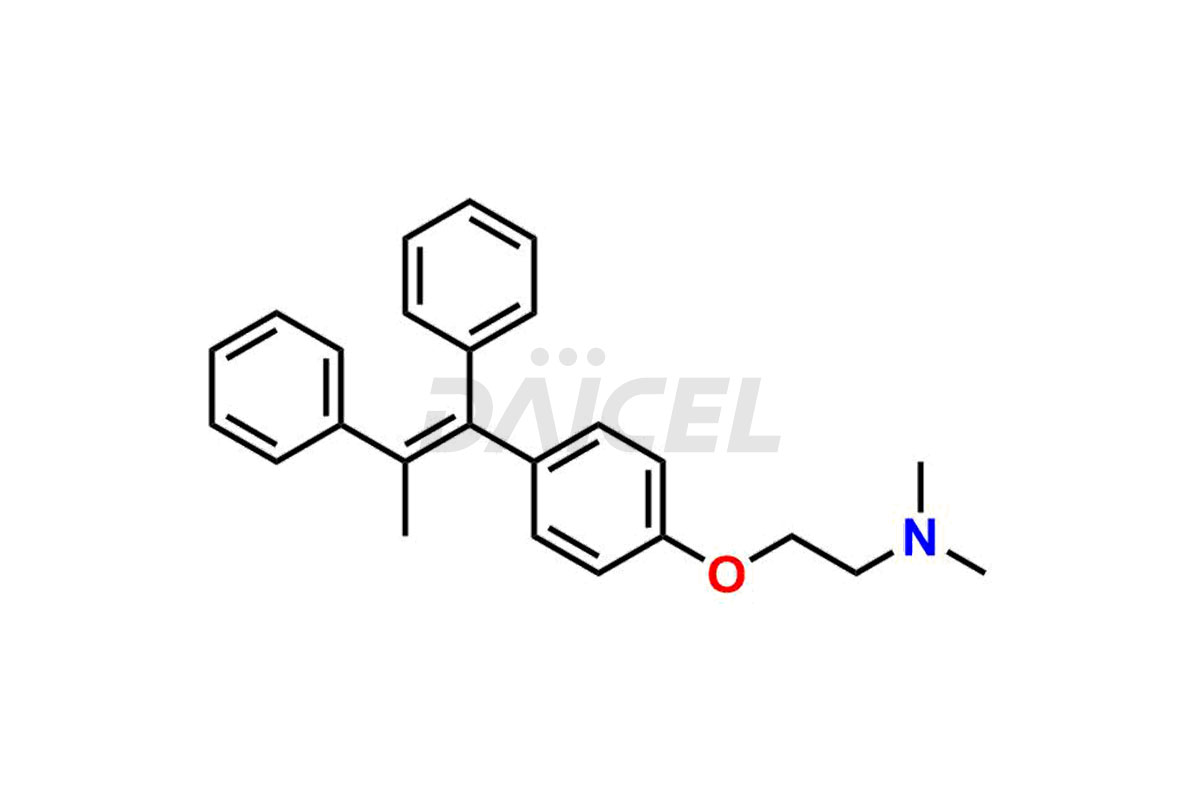
Le nom chimique du tamoxifène est 2-[4-[(1Z)-1,2-Diphényl-1-butén-1-yl]phénoxy]-N,N-diméthyléthanamine. Sa formule chimique est C26H29NON, et son poids moléculaire est d'environ 371.5 g/mol.
Les effets anti-œstrogéniques du tamoxifène entrent en compétition avec les œstrogènes pour les sites de liaison dans les tissus mammaires.
Impuretés et synthèse du tamoxifène
Lors de la synthèse1 et le stockage du tamoxifène, diverses impuretés telles que des substances apparentées, des produits de dégradation et des solvants résiduels peuvent se former. Il est essentiel de surveiller et de contrôler avec diligence ces impuretés pour garantir la sécurité, l’efficacité et la qualité globale du médicament.
Daicel Pharma fournit un certificat d'analyse (CoA) complet pour les normes d'impuretés du tamoxifène, notamment le bis-tamoxifène, l'impureté A du tamoxifène, l'impureté D du tamoxifène, l'impureté F du tamoxifène, le N-oxyde de tamoxifène et la chloroléfine Z. Ces impuretés sont produites strictement selon les bonnes pratiques de fabrication (cGMP) actuelles. Le CoA comprend des données de caractérisation détaillées, telles que la pureté RMN 1H, RMN 13C, IR, MASS et HPLC, offrant une compréhension approfondie du profil des impuretés. Sur demande, Daicel peut également fournir des données 13C-DEPT pour une caractérisation plus approfondie.
De plus, Daicel Pharma possède l'expertise technique nécessaire pour synthétiser toute impureté inconnue ou produit de dégradation du tamoxifène.
Bibliographie
FAQ
Bibliographie
- Brittain, David Robert, Procédé de fabrication de 1,1,2-Triphénylalk-1-Enes, Imperial Chemical Industries Ltd., GB1354939A, 30 mai 1974
- Daniel, CP; Gaskell, SJ; Évêque, G. ; Nicholson, RI, Détermination du tamoxifène et d'un métabolite hydroxylé dans le plasma de patientes atteintes d'un cancer du sein avancé par chromatographie en phase gazeuse-spectrométrie de masse, Journal of Endocrinology, Volume : 83, Numéro : 3, Pages : 401-8, 1979
Foire aux Questions
Comment les impuretés du Tamoxifène sont-elles détectées et quantifiées ?
Les méthodes analytiques telles que la chromatographie liquide haute performance (HPLC) peuvent détecter les impuretés présentes dans le tamoxifène.
Les impuretés du tamoxifène peuvent-elles affecter la sécurité des patients ?
La présence d'impuretés dans le tamoxifène peut affecter la sécurité des patients. Le type et le niveau de ces impuretés peuvent entraîner des effets indésirables ou diminuer l’efficacité du médicament.
Quels solvants aident à l’analyse des impuretés du tamoxifène ?
Le méthanol est utilisé pour obtenir une solubilité et une séparation optimales des impuretés du tamoxifène.
Quelles sont les conditions de température requises pour stocker les impuretés du tamoxifène ?
Les impuretés du tamoxifène sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.