Le sofosbuvir
Renseignements généraux
Impuretés du sofosbuvir et sofosbuvir
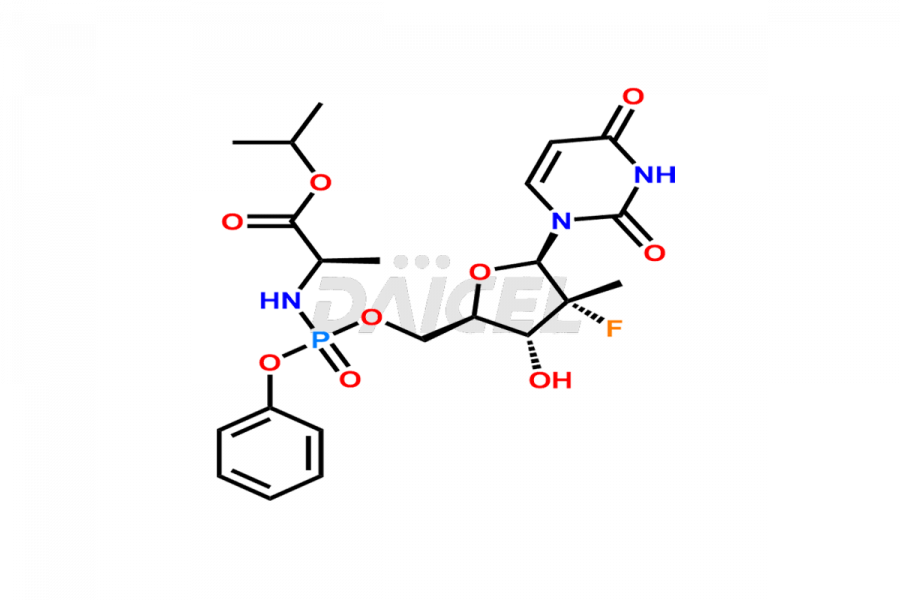
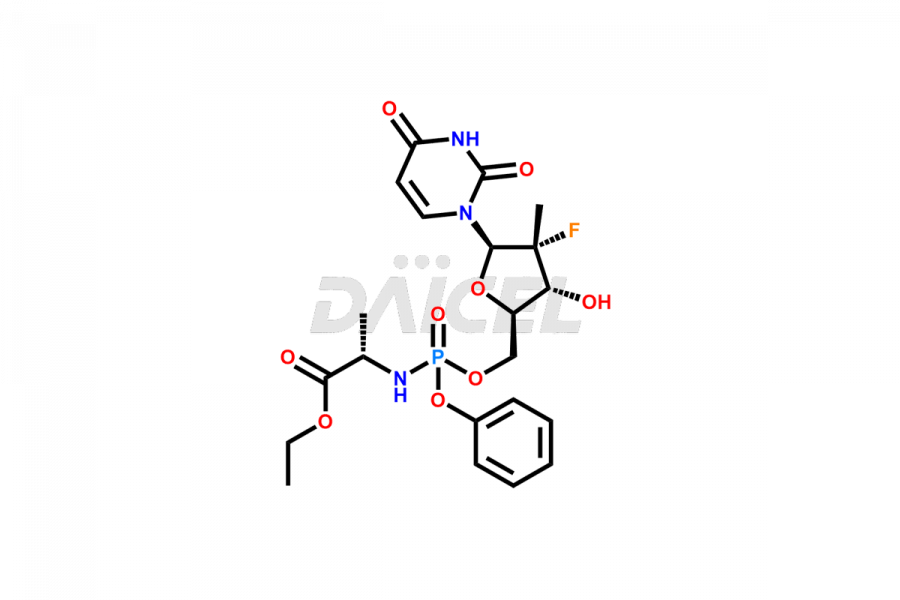
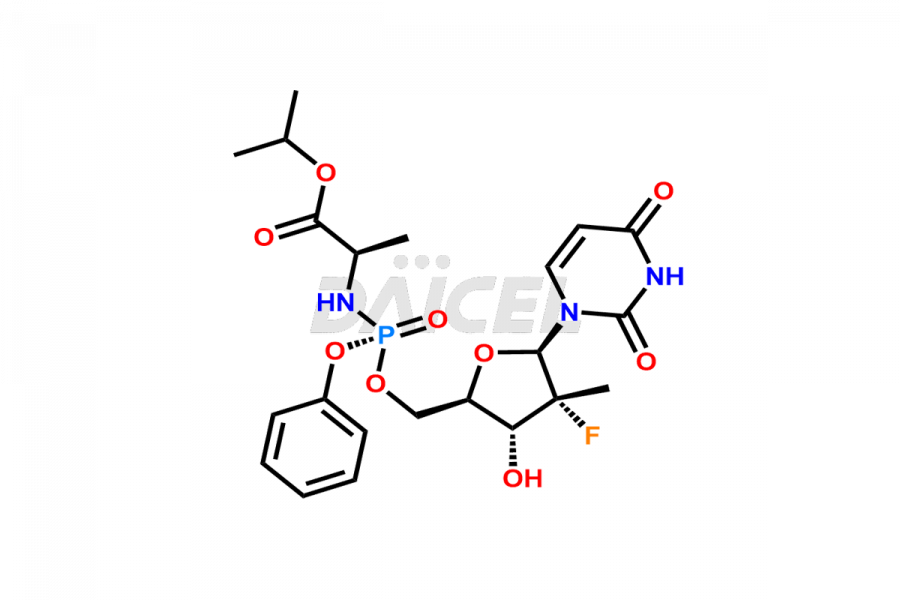
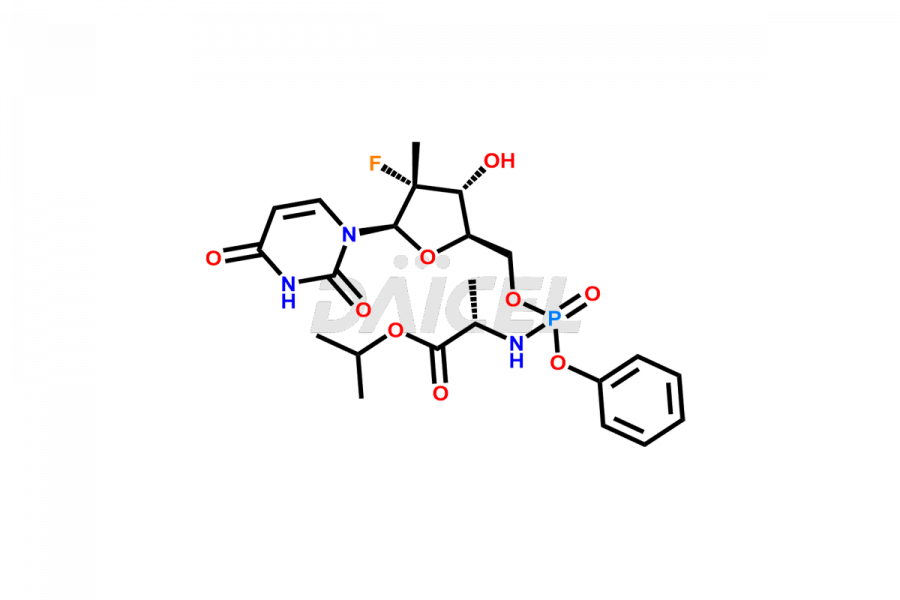
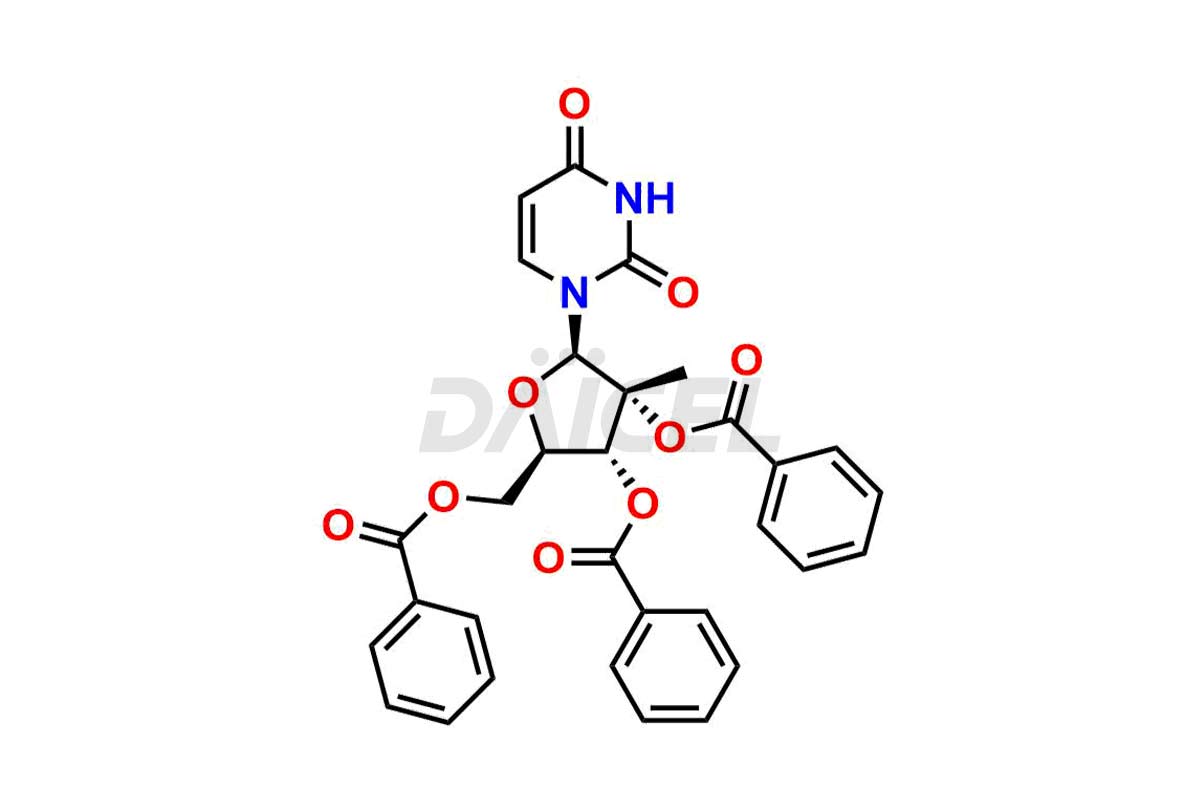
Daicel Pharma propose une gamme complète d'impuretés exclusives de Sofosbuvir telles que le D-Alanine Sofosbuvir, le Sofosbuvir (R)-Phosphate, le Sofosbuvir D-alaninate R, l'isomère S, l'isomère Sofosbuvir 3, l'impureté Sofosbuvir, et plus encore. Ces impuretés sont essentielles pour déterminer la qualité, la stabilité et la sécurité biologique de l'ingrédient pharmaceutique actif Sofosbuvir. De plus, Daicel Pharma peut synthétiser les impuretés du Sofosbuvir selon les spécifications précises du client tout en garantissant une livraison dans le monde entier.
Le sofosbuvir [CAS : 1190307/88/0] est un analogue nucléosidique administré par voie orale prescrit avec d'autres médicaments antiviraux. Il traite l'infection chronique par le virus de l'hépatite C (VHC) chez les patients atteints des génotypes 1,2, 3,4, 5, 6 du VHC. Il est également efficace dans le traitement des patients co-infectés par le VHC. et le VIH.
Sofosbuvir : utilisation et disponibilité commerciale
Le sofosbuvir est un médicament antiviral largement utilisé pour traiter les infections chroniques par le virus de l’hépatite C (VHC). Il se combine avec d’autres médicaments antiviraux pour former un schéma thérapeutique complet. Le sofosbuvir est administré par voie orale, ce qui le rend pratique pour les patients. Il s’est avéré très efficace pour obtenir une réponse virologique durable, améliorant ainsi les résultats pour les patients.
Le sofosbuvir est disponible sous Sovaldi, qui contient l’ingrédient actif Sofosbuvir.
Structure et mécanisme d'action du sofosbuvir 
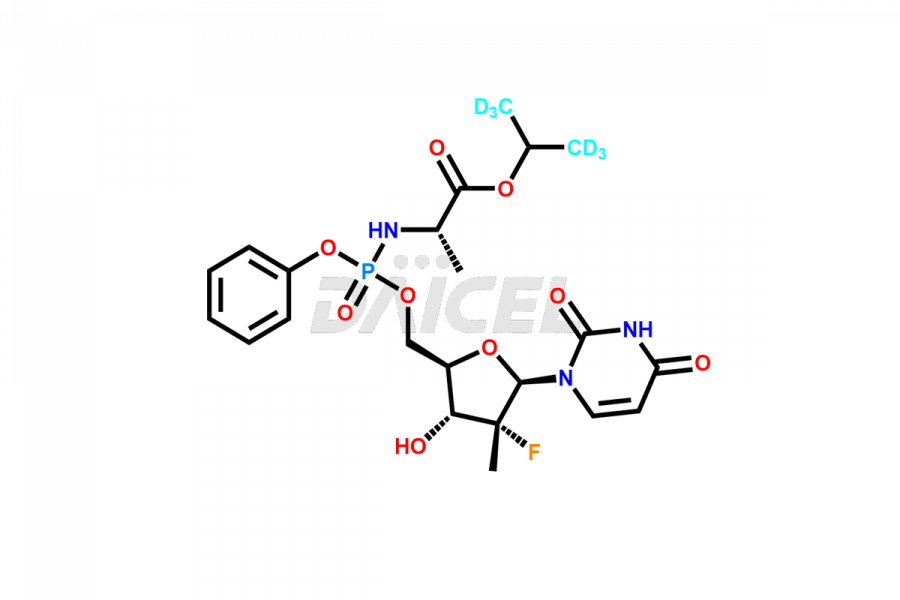
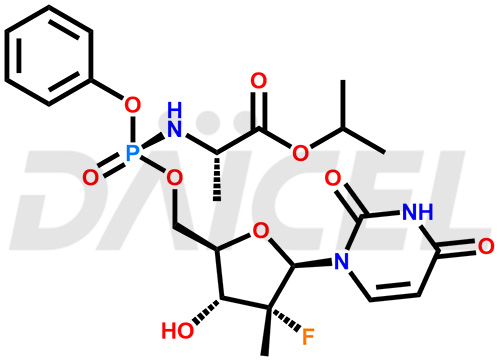
Le nom chimique du Sofosbuvir est N-[[P(S),2′R]-2′-désoxy-2′-fluoro-2′-méthyl-P-phényl-5′-uridylyl]- L-Alanine 1- ester de méthyléthyle. Sa formule chimique est C22H29FN3O9P, et son poids moléculaire est d'environ 529.5 g/mol.
Le sofosbuvir empêche l’ARN polymérase ARN-dépendante NS5B du VHC qui provoque la réplication virale.
Impuretés et synthèse du sofosbuvir
Lors de la synthèse1 et le stockage du Sofosbuvir, des impuretés peuvent apparaître, notamment des substances associées, des produits de dégradation et des solvants résiduels. Il est essentiel de surveiller et de contrôler attentivement ces impuretés pour garantir la sécurité, l'efficacité et la qualité globale du médicament.
Daicel Pharma propose un certificat d'analyse (CoA) complet pour les normes d'impuretés du sofosbuvir telles que le D-Alanine Sofosbuvir, le Sofosbuvir (R)-Phosphate, le Sofosbuvir D-alaninate R, l'isomère S, l'isomère Sofosbuvir 3, l'impureté Sofosbuvir, et plus encore. Ces impuretés se forment conformément aux bonnes pratiques de fabrication (cGMP) en vigueur. Le CoA comprend des données de caractérisation détaillées, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2, fournissant une compréhension approfondie du profil des impuretés. Sur demande, Daicel peut également fournir des données 13C-DEPT pour une caractérisation plus approfondie.
De plus, Daicel Pharma possède l'expertise technique nécessaire pour synthétiser toute impureté inconnue ou produit de dégradation du Sofosbuvir. Nous proposons également des composés labellisés. Pour la recherche bioanalytique et les études de biodisponibilité/bioéquivalence (BA/BE), Daicel Pharma fournit le Sofosbuvir-D6, un étalon de Sofosbuvir marqué deutéré de haute pureté.
Bibliographie
FAQ
Bibliographie
Foire aux Questions
Comment les impuretés du Sofosbuvir sont-elles détectées et quantifiées ?
Les méthodes analytiques telles que la chromatographie liquide haute performance en phase inverse (RP-HPLC) peuvent détecter les impuretés dans le sofosbuvir.
Les impuretés du Sofosbuvir peuvent-elles affecter la sécurité des patients ?
Les impuretés contenues dans le Sofosbuvir peuvent avoir un impact sur la sécurité des patients. Selon leur nature et leur concentration, les contaminants peuvent provoquer des effets indésirables ou réduire l’efficacité du médicament.
Quels solvants aident à l’analyse des impuretés du Sofosbuvir ?
L'acétonitrile aide à obtenir une solubilité et une séparation optimales des impuretés du Sofosbuvir.
Quelles sont les conditions de température nécessaires pour stocker les impuretés du Sofosbuvir ?
Les impuretés du sofosbuvir sont conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.