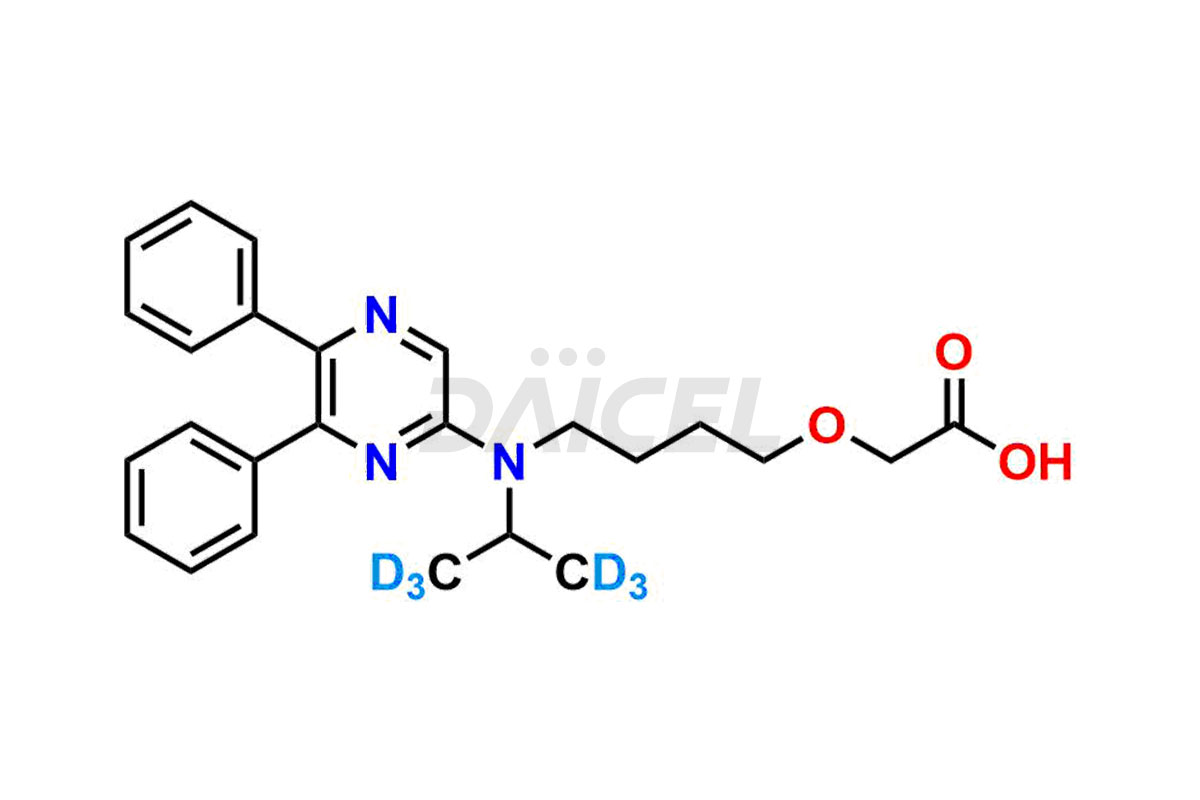
Sélexipag
Bibliographie
- Asaki, Tetsuo ; Hamamoto, Taisuke ; Kuwano, Keiichi, Dérivés de composés hétérocycliques et médicaments, Nippon Shinyaku Co., Ltd., Japon, EP1400518B1, 17 janvier 2007
- Bonde, Prajakta G. ; Bachhav, RS; Kalegaonkar, Somnath, Développement et validation de la méthode RP-HPLC pour l'estimation du sélexipag en vrac et de sa forme posologique en comprimé, World Journal of Pharmacy and Pharmaceutical Sciences, Volume : 11, Numéro : 8, Pages : 2166-2175, 2022
Foire aux Questions
Pourquoi la présence d’impuretés est-elle préoccupante dans Selexipag ?
La présence d'impuretés dans Selexipag peut affecter considérablement sa qualité, sa sécurité et son efficacité. Selon le type et la concentration des impuretés, elles peuvent nuire à l'activité pharmacologique et à la stabilité du médicament et, à terme, présenter des risques potentiels pour la santé des patients. Il est donc crucial de gérer et de contrôler soigneusement les impuretés pour garantir les performances et la sécurité optimales du médicament en tant que produit pharmaceutique.
Comment les impuretés sont-elles détectées et quantifiées dans Selexipag ?
Les impuretés de Selexipag sont évaluées à l'aide de techniques analytiques telles que la nouvelle méthode de chromatographie liquide haute performance (RP-HPLC).
Quels solvants aident à l’analyse des impuretés Selexipag ?
Le méthanol est le solvant utilisé dans les techniques analytiques pour séparer et détecter les impuretés du Selexipag.
Quelles sont les conditions de température requises pour stocker les impuretés Selexipag ?
Les impuretés Selexipag doivent être conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.