Charger plus
Vous avez vu 9 sur 13 articles
Daicel Pharma synthétise plus de douze impuretés du Ruxolitinib de haute qualité, telles que l'isomère R du Ruxolitinib, le métabolite du Ruxolitinib M18, l'oxyde de triphénylphosphine du Ruxolitinib, l'impureté Ruxolitinib Acrylopyrimidine, et plus encore. Ils sont cruciaux pour déterminer la qualité, la stabilité et la sécurité biologique du principe pharmaceutique actif, le ruxolitinib. De plus, Daicel Pharma propose une synthèse personnalisée des impuretés du Ruxolitinib et les livre dans le monde entier.
Ruxolitinib [CAS : 941678-49-5] est un médicament utilisé pour traiter la myélofibrose à risque intermédiaire ou élevé. Il inhibe les enzymes kinases associées à Janus (JAK) et a des effets antinéoplasiques et immunomodulateurs potentiels. Il est disponible sous forme de sel de phosphate.
Le ruxolitinib est un médicament qui appartient à la classe de médicaments appelés inhibiteurs de kinase activés par Janus (JAK). Il inhibe sélectivement les protéines kinases JAK1 et JAK2. Le ruxolitinib est approuvé par la FDA pour le traitement de la myélofibrose à haut risque, des patients atteints de polycythémie vraie intolérants ou résistants à l'hydroxyurée et de la maladie aiguë du greffon contre l'hôte réfractaire aux stéroïdes. Il est disponible sous différentes concentrations de comprimés sous la marque JAKAFI et sous forme de crème topique sous le nom OPZELURA. En 2021, la FDA a approuvé une formulation de crème de Ruxolitinib pour le traitement de la dermatite atopique légère à modérée, ce qui en fait le premier inhibiteur topique de JAK approuvé pour une utilisation sur le marché américain.
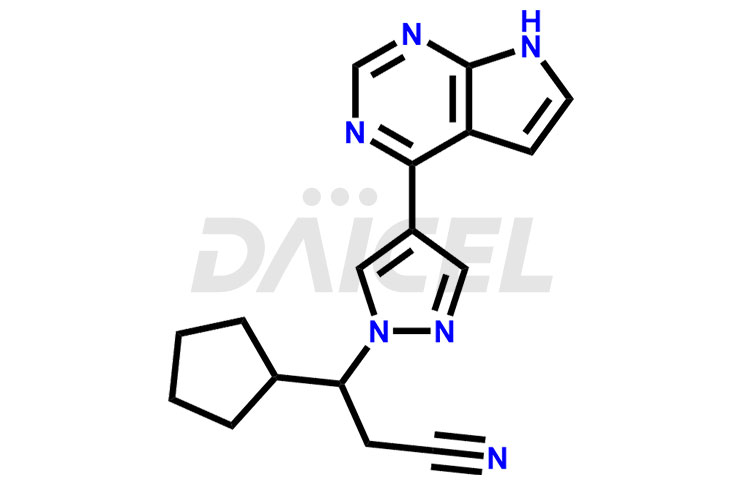
Son nom chimique est (R)-3-[4-(7H-Pyrrolo[2,3-d]pyrimidin-4-yl)-1H-pyrazol-1-yl]-3-cyclopentylpropanenitrile. La formule chimique du ruxolitinib est C17H18N6, et son poids moléculaire est d'environ 306.4 g/mol.
Le ruxolitinib appartient à la classe des médicaments inhibiteurs de JAK qui inhibent les protéines kinases JAK1 et JAK2. Le médicament affecte la signalisation de plusieurs cytokines et facteurs de croissance responsables de l'hématopoïèse et de la fonction immunitaire.
Lors de la synthèse1 du Ruxolitinib, plusieurs impuretés peuvent se former, notamment des diastéréomères, des régioisomères, des épimères et des dégradants. Ces impuretés doivent être étroitement surveillées et contrôlées lors de la synthèse du ruxolitinib pour garantir la sécurité et l'efficacité du médicament.
Daicel propose un certificat d'analyse (CoA) d'un centre d'analyse conforme aux BPF c pour plus de douze normes d'impuretés du Ruxolitinib, y compris l'isomère R du Ruxolitinib, le métabolite du Ruxolitinib M18, l'oxyde de triphénylphosphine du Ruxolitinib, l'impureté de l'acrylopyrimidine du Ruxolitinib, etc. Le CoA comprend des données de caractérisation complètes. , tels que RMN 1H, RMN 13C, IR, MASS2et la pureté HPLC. Nous fournissons également du 13C-DEPT et du CHN sur demande. Nous remettons également un rapport de caractérisation complet à la livraison.
Daicel dispose de la technologie et de l’expertise nécessaires pour préparer toute impureté ou produit de dégradation inconnu du Ruxolitinib. La société fournit également des composés marqués pour quantifier l’efficacité du Ruxolitinib générique. Daicel propose des étalons de ruxolitinib hautement purs marqués par des isotopes pour la recherche bioanalytique et les études BA/BE. Daicel fournit la pureté isotopique du composé marqué, le Ruxolitinib-D9, dans le CoA.
Les facteurs influençant la synthèse des impuretés du Ruxolitinib comprennent le choix des matières premières, les conditions de réaction, le choix du solvant, la température et les catalyseurs.
Les impuretés de dégradation du ruxolitinib peuvent inclure des impuretés formées en raison de la dégradation chimique ou physique du médicament, telle que l'hydrolyse, l'oxydation et la photodégradation.
Des techniques analytiques telles que la chromatographie liquide haute performance (HPLC), la chromatographie liquide-spectrométrie de masse (LC-MS), etc., permettent d'identifier et de quantifier les impuretés du Ruxolitinib.
Les impuretés du ruxolitinib sont isolées et purifiées à l'aide de techniques de chromatographie sur colonne, de recristallisation et de HPLC préparative.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.