Charger plus
Vous avez vu 9 sur 24 articles
Daicel Pharma fournit la synthèse des standards d'impuretés du Rivaroxaban tels que le 5-chloro-N-méthylthiophène-2-carboxamide, l'impureté B du Rivaroxaban, le métabolite 5 du Rivaroxaban, l'impureté H du Rivaroxaban EP, l'impureté F du Rivaroxaban EP, l'impureté B du Rivaroxaban EP, l'impureté 5 du RVX III, et plus encore . Ces impuretés sont cruciales pour la qualité, l’efficacité, la sécurité et la stabilité du Rivaroxaban. De plus, Daicel propose une synthèse personnalisée des impuretés du Rivaroxaban et les livre globalement selon les exigences du client.
Le rivaroxaban [CAS : 366789/02/8] est un amide d'acide monocarboxylique et est un anticoagulant. Le rivaroxaban est le premier inhibiteur direct du facteur Xa à action orale. Il prévient les accidents vasculaires cérébraux et les embolies veineuses.
Le rivaroxaban prévient les événements thromboemboliques veineux (TEV) chez les patients ayant subi une arthroplastie totale de la hanche ou du genou ; pour prévenir les accidents vasculaires cérébraux et l'embolie systémique chez les patients atteints de fibrillation auriculaire non valvulaire ; pour traiter la thrombose veineuse profonde (TVP) et l'embolie pulmonaire (EP) ; et pour réduire le risque de TVP et/ou d'EP récurrentes. Ce médicament est disponible sous le nom commercial de Xarelto.
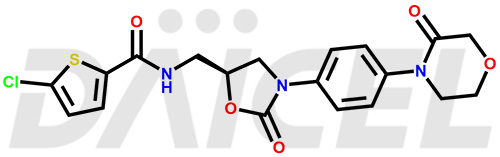
Le nom chimique du Rivaroxaban est 5-Chloro-N-[[(5S)-2-oxo-3-[4-(3-oxo-4-morpholinyl)phényl]-5-oxazolidinyl]méthyl]-2-thiophènecarboxamide. Sa formule chimique est C19H18CIN3O5S, et son poids moléculaire est d'environ 435.9 g/mol.
Le rivaroxaban bloque sélectivement le site actif du facteur Xa et contribue au processus de coagulation sanguine.
Le rivaroxaban est un médicament anticoagulant utilisé pour prévenir la formation de caillots sanguins. Comme de nombreux composés pharmaceutiques, il peut contenir des impuretés pouvant avoir un impact sur sa qualité et son efficacité. Ils peuvent inclure des composés apparentés, liés au processus et des impuretés génotoxiques potentielles. La synthèse1 du Rivaroxaban implique un processus complexe en plusieurs étapes, comprenant la réaction de divers intermédiaires avec des réactifs, suivie d'étapes de purification pour isoler l'ingrédient pharmaceutique actif.
Daicel Pharma fournit un certificat d'analyse (CoA) des normes d'impuretés du Rivaroxaban telles que le 5-chloro-N-méthylthiophène-2-carboxamide, l'impureté B du Rivaroxaban, le métabolite 5 du Rivaroxaban, l'impureté H du Rivaroxaban EP, l'impureté F du Rivaroxaban EP, l'impureté B du Rivaroxaban EP. , RVX III Impureté 5, et plus encore. Notre CoA provient d'une installation d'analyse conforme aux BPF et comprend des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC. Sur demande, nous fournissons des données de caractérisation supplémentaires, telles que 13C-DEPT. Daicel Pharma peut fournir des impuretés ou des produits de dégradation inconnus du Rivaroxaban.
Des recherches comparatives et un contrôle qualité rigoureux garantissent que les versions génériques sont équivalentes en termes de pureté, de sécurité et d'efficacité.
Lors des tests de contrôle qualité, les impuretés du Rivaroxaban utilisent des techniques analytiques telles que les méthodes HPLC pour identifier et quantifier les impuretés présentes dans le Rivaroxaban.
En raison des différentes procédures de synthèse, le niveau d'impuretés du Rivaroxaban peut varier.
Les impuretés du rivaroxaban doivent être conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.