Rilpivirine
Renseignements généraux
Impuretés de la rilpivirine et rilpivirine
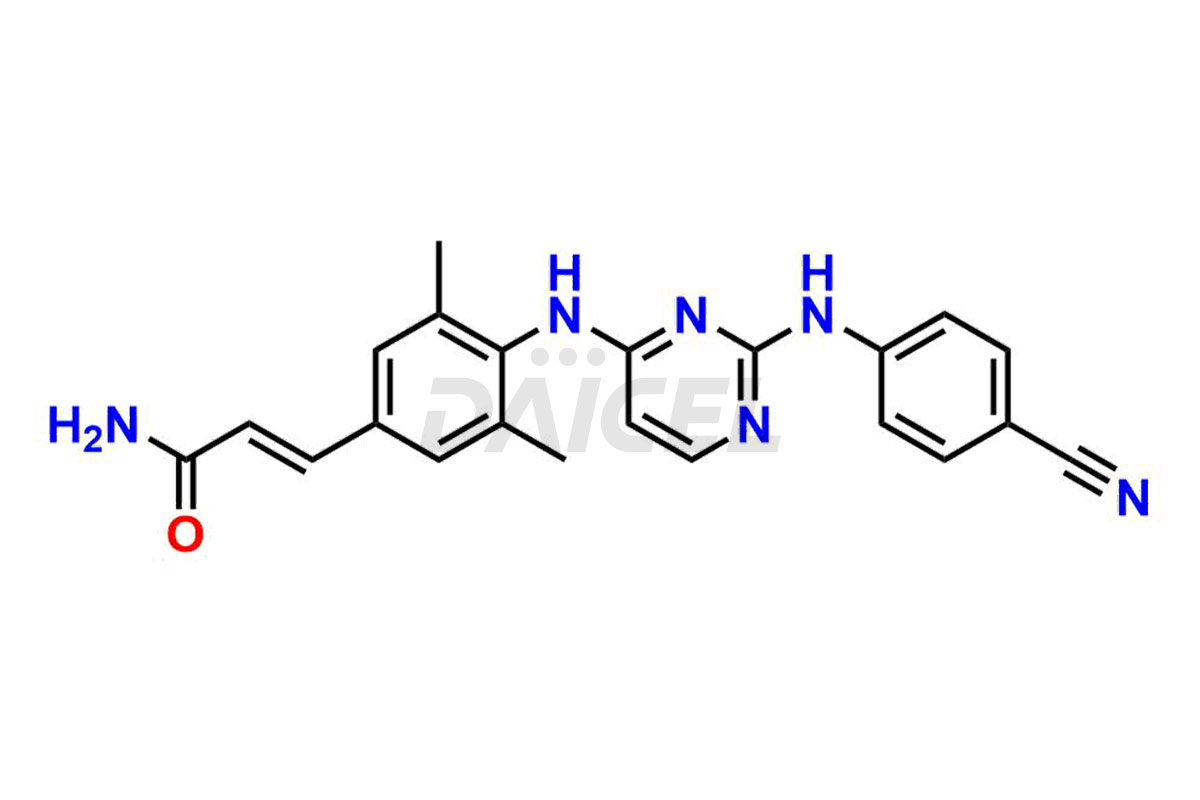
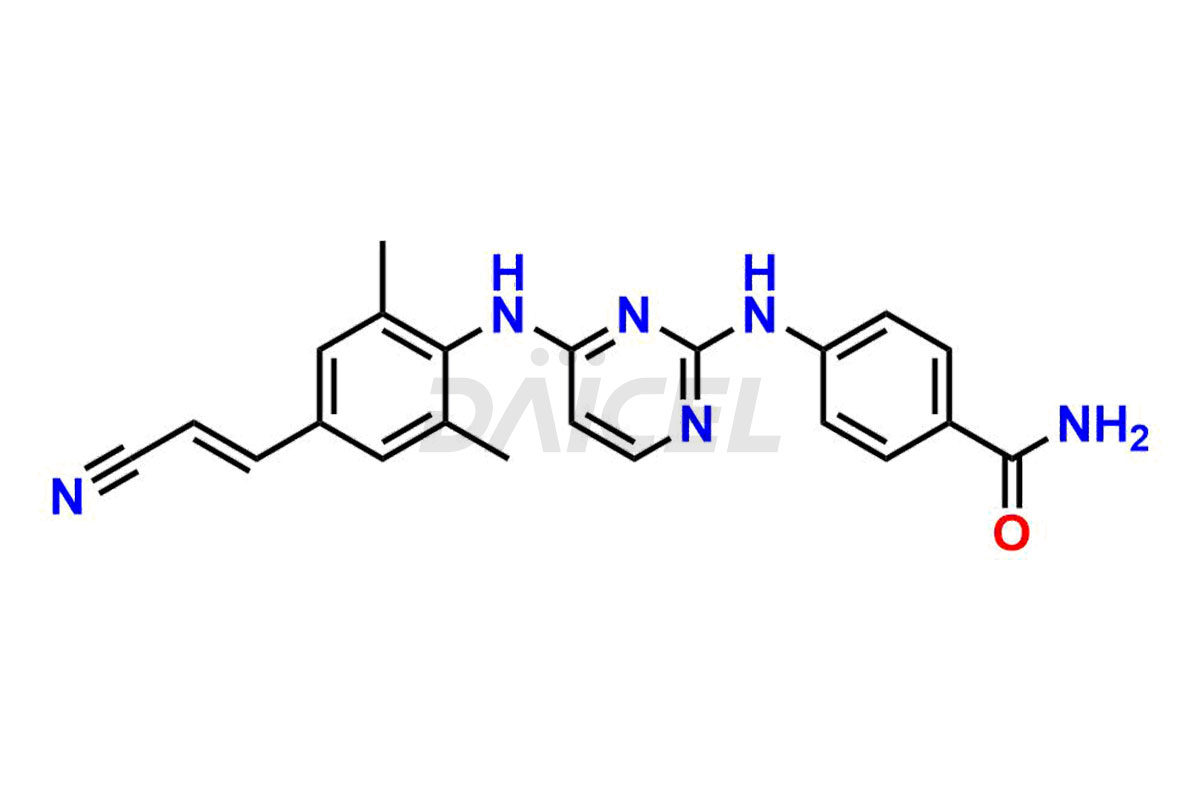
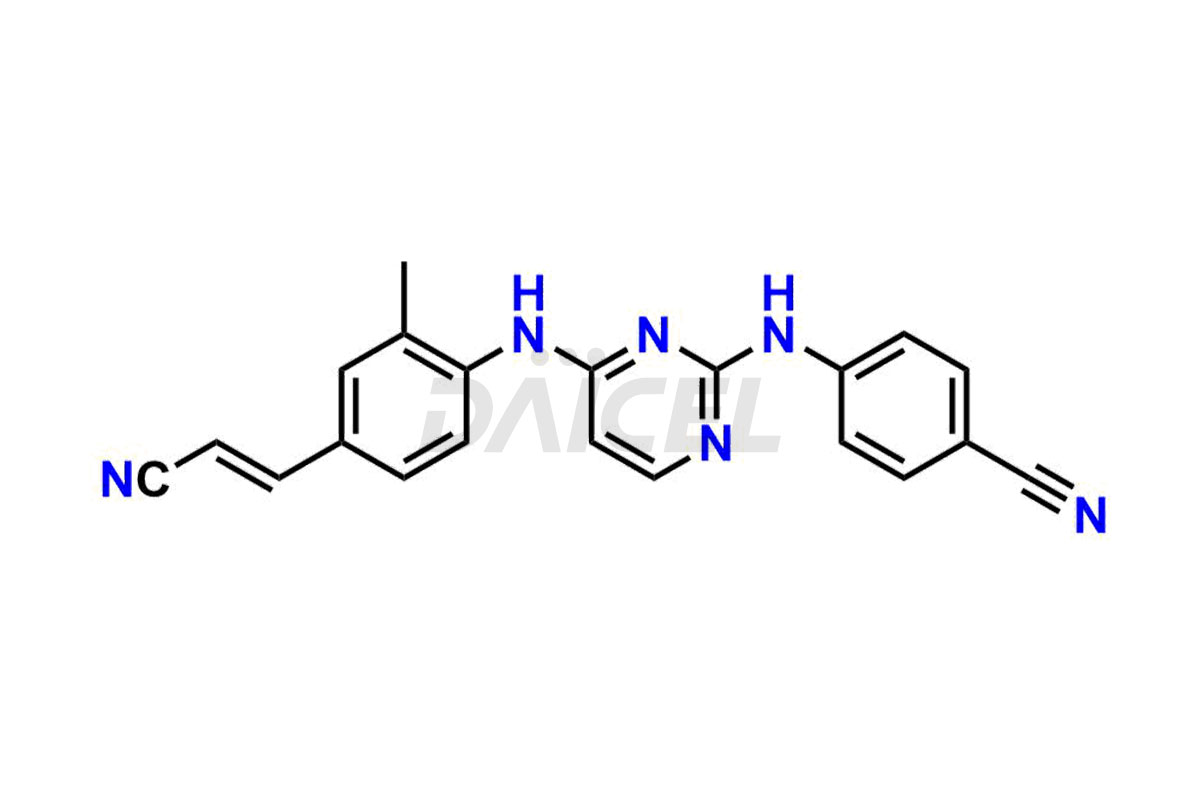
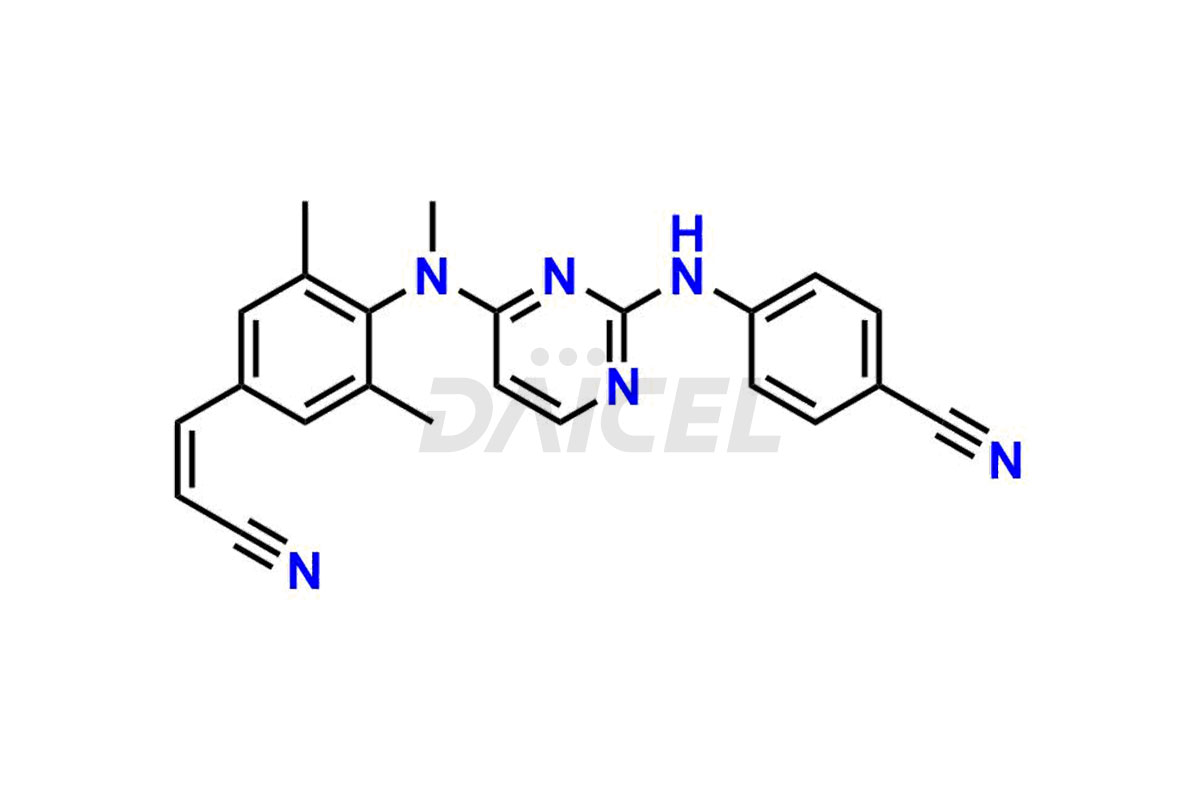
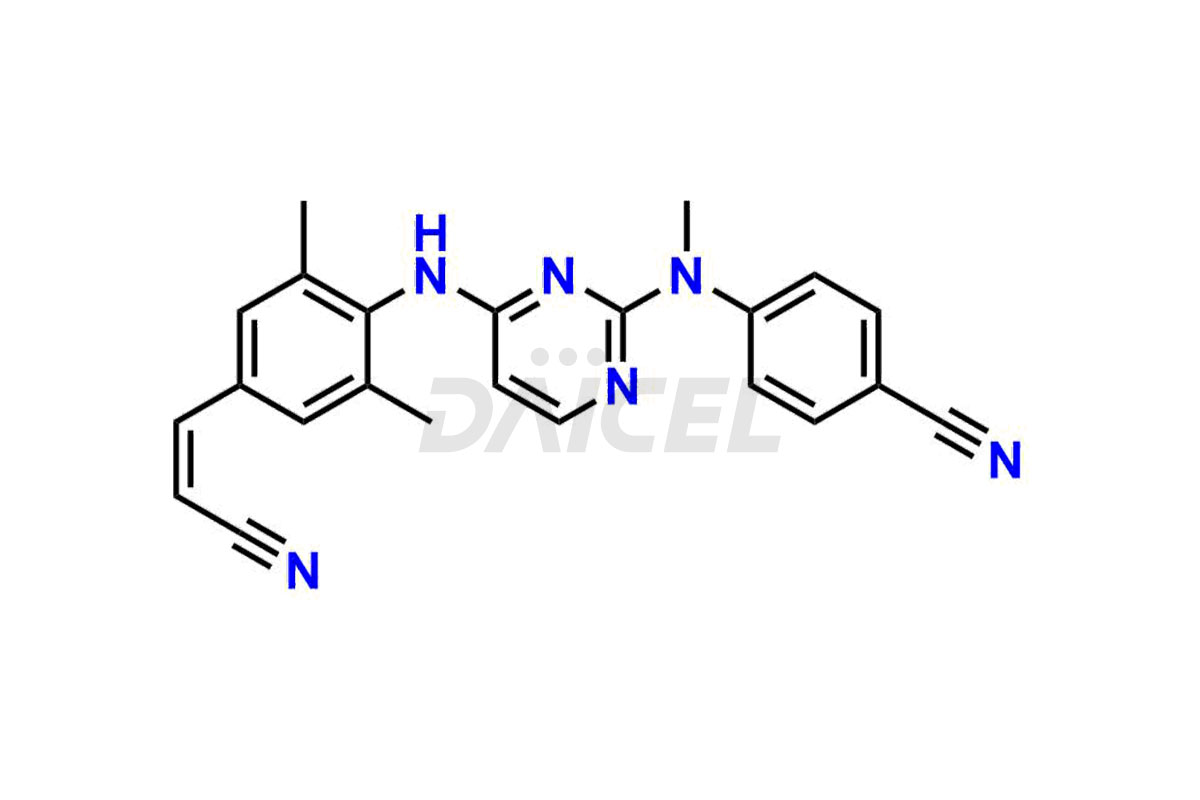
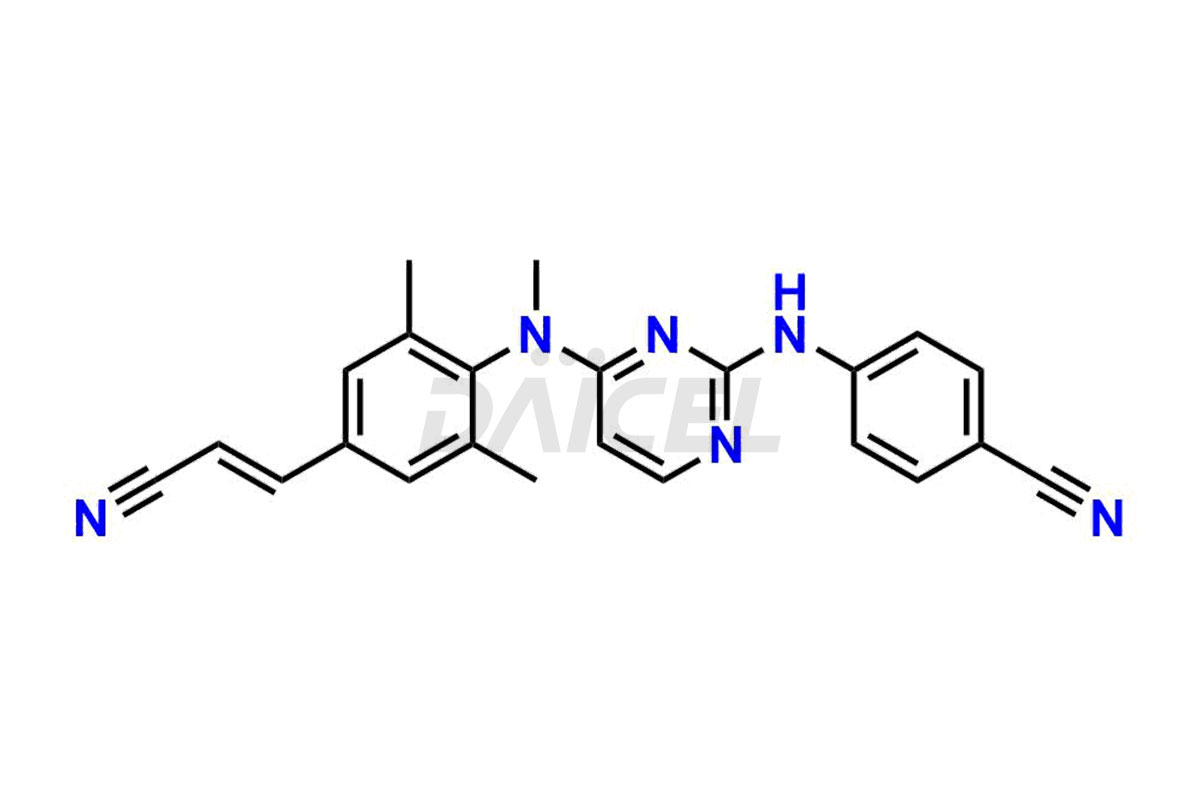
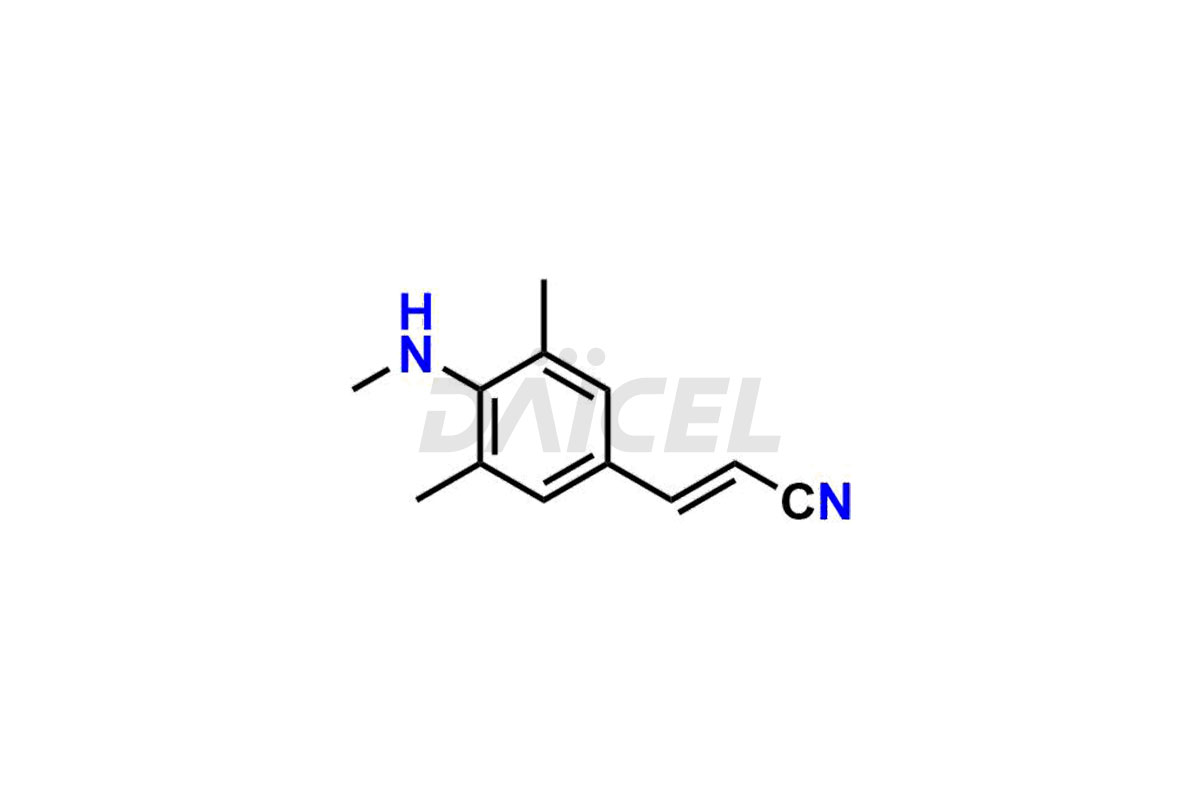
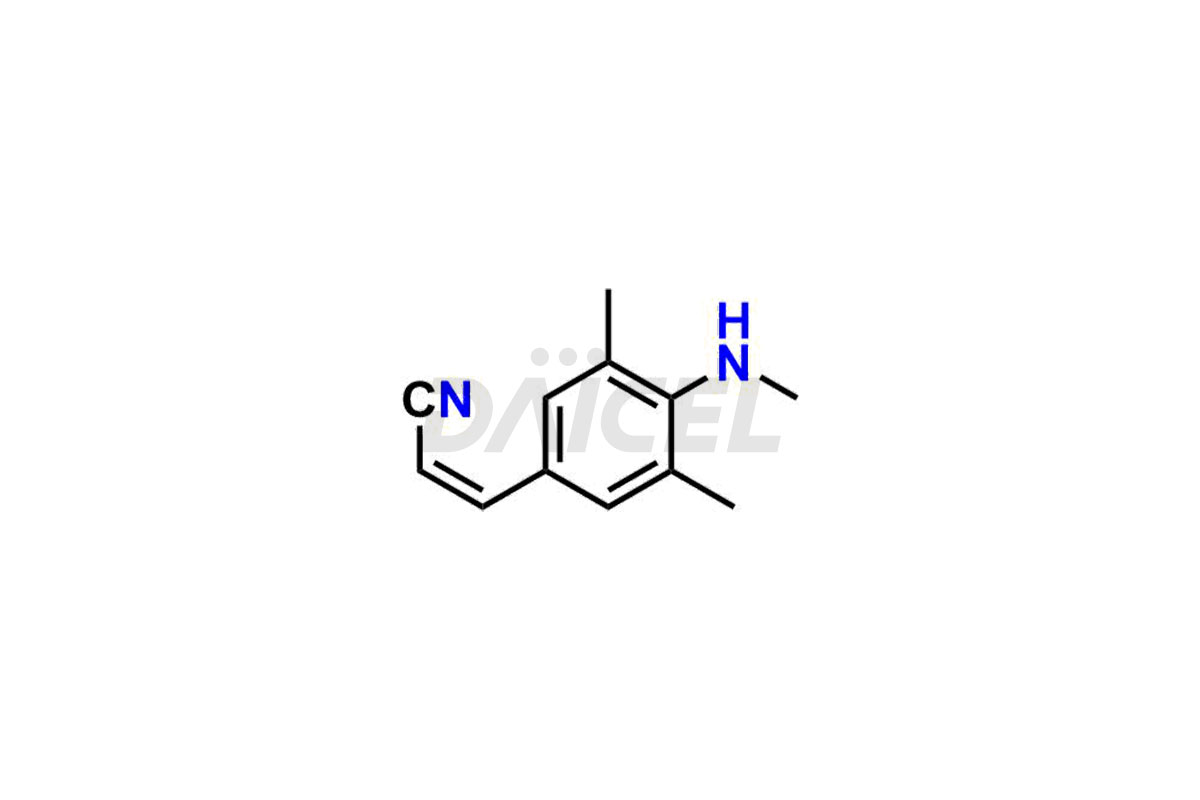
Daicel Pharma propose des standards d'impuretés de Rilpivirine qui sont l'impureté de Rilpivirine 2, l'impureté de Rilpivirine 3, l'impureté de Rilpivirine 4, l'impureté de Rilpivirine 6, l'impureté d'Amide de Rilpivirine-1, l'impureté d'Amide de Rilpivirine-2, l'impureté de Rilpivirine Desméthyl, l'impureté de Rilpivirine 6 – Isomère Z et l'impureté d'ester méthylique de Rilpivirine . Ces impuretés sont essentielles à la qualité, à l’efficacité, à la sécurité et à la stabilité de la Rilpivirine. De plus, Daicel propose une synthèse personnalisée des impuretés de la Rilpivirine et les livre dans le monde entier.
Rilpivirine [CAS : 500287-72-9] est une aminopyrimidine qui traite l'infection par le VIH.
Rilpivirine : utilisation et disponibilité commerciale
La rilpivirine associée à des agents antirétroviraux traite les infections par le VIH-1 chez les patients naïfs de traitement antirétroviral. Ce médicament est disponible sur le marché sous la marque Edurant.
Structure et mécanisme d'action de la rilpivirine 
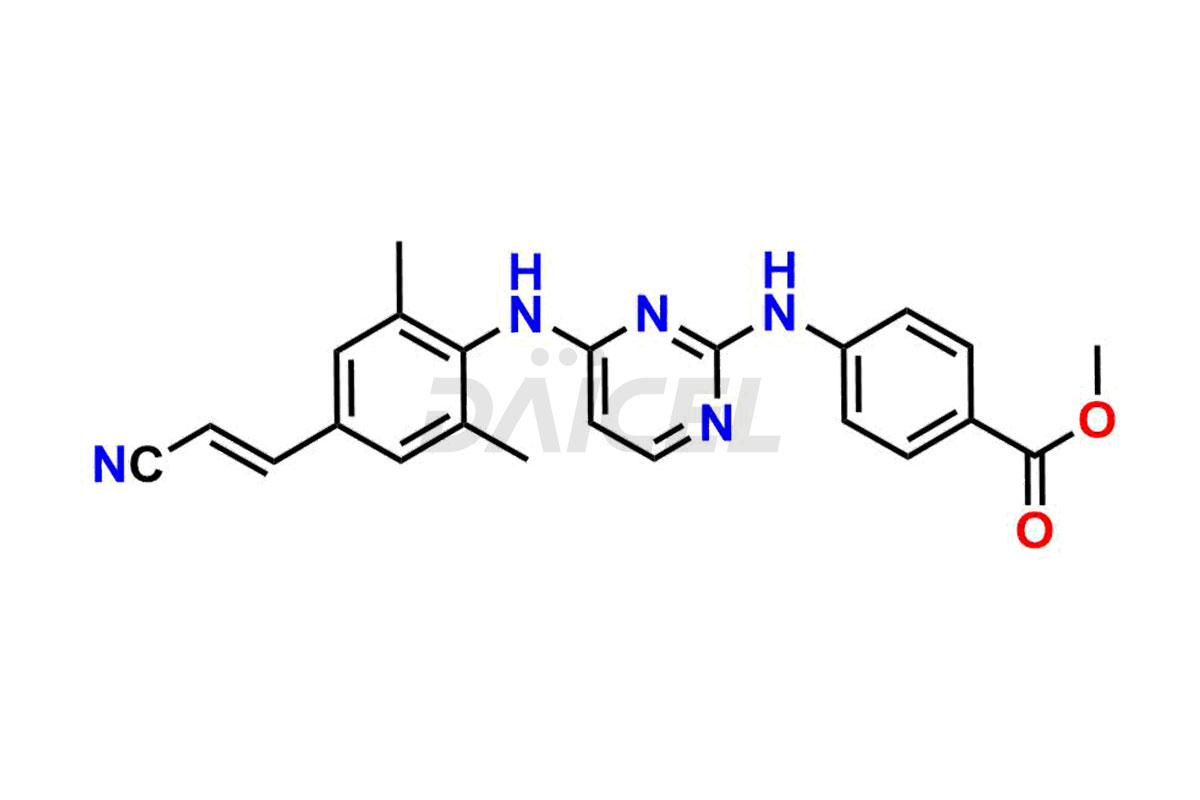
Le nom chimique de la Rilpivirine est 4-[[4-[[4-[(1E)-2-Cyanoethenyl]-2,6-diméthylphényl]amino]-2-pyrimidinyl]amino]benzonitrile. Sa formule chimique est C22H18N6, et son poids moléculaire est d'environ 366.4 g/mol.
La rilpivirine bloque la réplication du VIH-1 par inhibition non compétitive de la transcriptase inverse du VIH-1.
Impuretés et synthèse de la rilpivirine
Les impuretés de la rilpivirine sont des substances chimiques inattendues qui pourraient apparaître lors de la production1 ou le stockage du médicament antirétroviral, la Rilpivirine. Ces impuretés peuvent provenir de différentes sources, telles que des matières premières, des réactifs, des étapes du procédé ou des produits de dégradation. Les impuretés de la rilpivirine nécessitent un contrôle et une surveillance stricts pour garantir la sécurité, l'efficacité et la qualité des analyses des médicaments, et les procédures analytiques aident à identifier, quantifier et caractériser ces impuretés.
Daicel Pharma propose un certificat d'analyse (CoA) pour les normes d'impuretés de la rilpivirine qui sont l'impureté de la rilpivirine 2, l'impureté de la rilpivirine 3, l'impureté de la rilpivirine 4, l'impureté de la rilpivirine 6, l'impureté de l'amide de la rilpivirine-1, l'impureté de l'amide de la rilpivirine-2, l'impureté de la rilpivirine desméthyle, l'impureté de la rilpivirine 6 – Isomère Z et impureté de l’ester méthylique de la rilpivirine. Notre installation d'analyse certifiée cGMP fournit un CoA complet avec des données de caractérisation détaillées telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. Des caractérisations supplémentaires telles que 13C-DEPT sont disponibles sur demande. Nous proposons des impuretés et des produits de dégradation de la Rilpivirine.
Bibliographie
FAQ
Bibliographie
- Guillemont, Jérôme Émile Georges; Palandjian, Patrice ; De Jonge, Marc René ; Koymans, Lucien Maria Henricus ; Vinkers, Hendrik Maarten ; Daeyaert, Frederik Frans Désir; Heeres, janvier ; Van Aken, Koen Jeanne Alfons ; Lewis, Paulus Joannes ; Janssen, Paul Adriaan Jan, Dérivés de pyrimidines inhibiteurs du VIH, Janssen Pharmaceutica NV, Belgique, EP1419152B1, 27 juillet 2011
- Masthanamma, Saskatchewan ; Gottumukkala, Alekhya, Développement et validation de méthodes spectrophotométriques UV pour l'estimation de la rilpivirine en vrac et en formulation pharmaceutique, International Journal of Pharmaceutical Sciences and Research, Volume : 5, Numéro : 2, Pages : 483-489 2014
Foire aux Questions
Existe-t-il des impuretés spécifiques à la Rilpivirine qui peuvent interagir avec d'autres médicaments ou substances ?
Les impuretés de la rilpivirine peuvent potentiellement interagir avec d'autres médicaments ou substances.
Quelles mesures sont prises pendant le processus de fabrication pour minimiser la formation d'impuretés de Rilpivirine ?
Des processus de fabrication rigoureux et des mesures de contrôle de qualité, comme une sélection minutieuse des matières premières, des conditions de réaction optimisées et des techniques de purification, contribuent à minimiser la formation d'impuretés lors de la fabrication de la Rilpivirine.
La présence d'impuretés de Rilpivirine peut-elle entraîner des variations dans ses effets pharmacologiques ou dans la réponse du patient ?
Les impuretés de la rilpivirine peuvent provoquer des variations dans ses effets pharmacologiques ou dans la réponse du patient.
Quelles sont les conditions de température nécessaires pour stocker les impuretés de la Rilpivirine ?
Les impuretés de la rilpivirine doivent être conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.