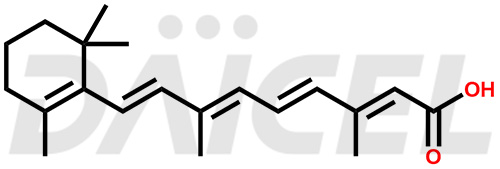
L'acide rétinoïque
Renseignements généraux
Impuretés de l'acide rétinoïque et acide rétinoïque
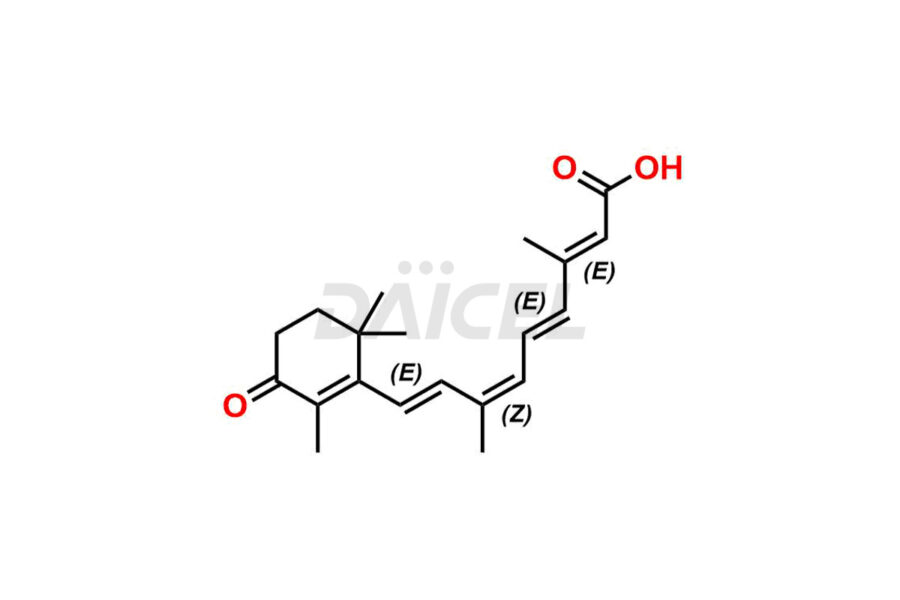
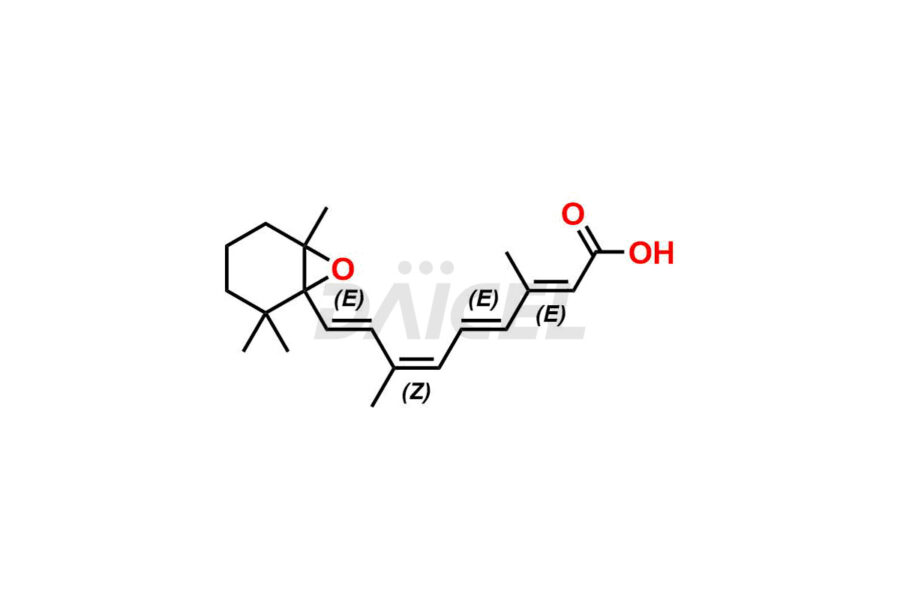
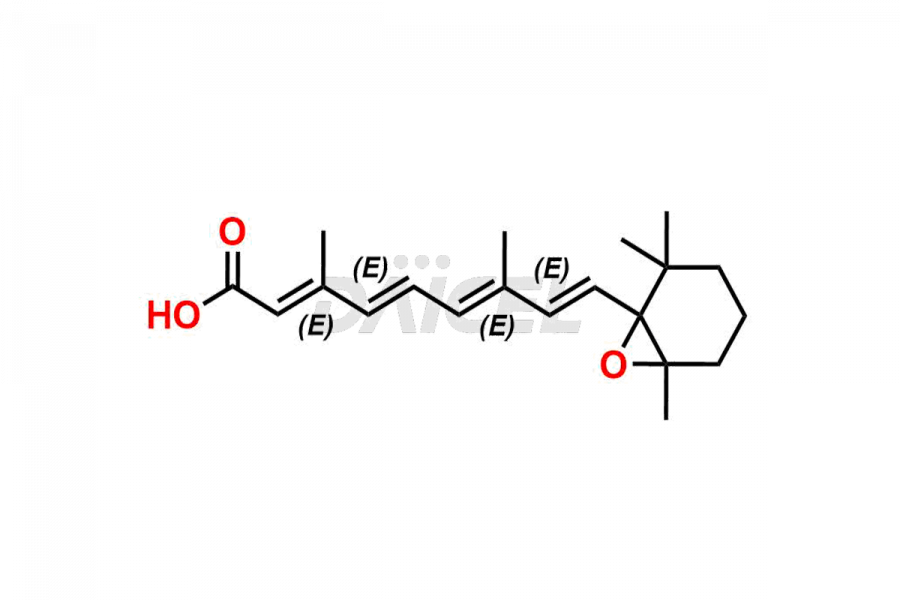
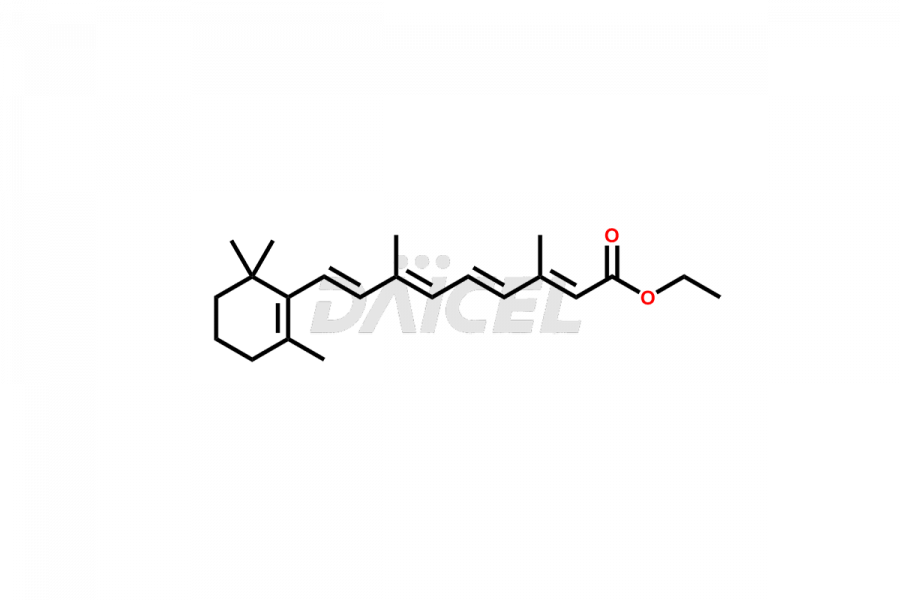
Daicel Pharma propose la synthèse des normes d'impuretés de l'acide rétinoïque, qui comprennent l'acide 4-Oxo-9-Cis rétinoïque, l'acide 5,6-époxy-9-Cis-rétinoïque et l'acide tout-trans 5,6-époxy rétinoïque. L'analyse de la qualité, de l'efficacité, de la sécurité et de la stabilité de l'acide rétinoïque implique l'utilisation de ces normes d'impuretés. Daicel Pharma propose une synthèse personnalisée des impuretés de l'acide rétinoïque et les livre dans le monde entier.
L'acide rétinoïque [CAS : 302/79/4] est un dérivé naturel du rétinol, la vitamine A. Il s'agit d'un acide conjugué entièrement trans-rétinoate.
Acide rétinoïque : utilisation et disponibilité commerciale
L'acide rétinoïque est destiné au traitement topique de l'acné vulgaire, des verrues plates et d'autres affections cutanées (psoriasis, ichtyose congénitale, ichtyose vulgaire, icthyose lamellaire, etc.). Il contribue à la croissance cellulaire et au développement embryonnaire précoce. Il aide également à la prévention et au traitement du cancer.
Ce médicament est disponible sur le marché sous les marques Altreno, Avita, Retin-A, Refissa, etc.
Structure de l'acide rétinoïque et mécanisme d'action 
Le nom chimique de l’acide rétinoïque est l’acide (tout-E)-3,7-diméthyl-9-(2,6,6-triméthyl-1-cyclohexén-1-yl)-2,4,6,8-nonatétraénoïque. Sa formule chimique est C20H28O2, et son poids moléculaire est d'environ 300.4 g/mol.
Le mécanisme d’action précis de l’acide rétinoïque est inconnu.
Impuretés et synthèse de l'acide rétinoïque
Les impuretés de l'acide rétinoïque sont des composés chimiques involontaires présents lors de la fabrication ou du stockage de l'acide rétinoïque, un dérivé de la vitamine A fréquemment utilisé en dermatologie. Ils peuvent se former à partir de matières premières, de réactifs, d’intermédiaires ou de produits de dégradation. Les impuretés de l'acide rétinoïque nécessitent un contrôle et une surveillance stricts pour garantir la sécurité, l'efficacité et la qualité des médicaments, et les procédures analytiques aident à identifier, quantifier et caractériser ces impuretés.
Daicel Pharma fournit un certificat d'analyse (CoA) des normes d'impuretés de l'acide rétinoïque qui comprennent l'acide 4-Oxo-9-Cis rétinoïque, l'acide 5,6-époxy-9-Cis-rétinoïque et l'acide All-trans 5,6-époxy rétinoïque. Acide. Notre installation d'analyse certifiée cGMP fournit un CoA complet avec des données de caractérisation détaillées telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC. Des caractérisations supplémentaires telles que 13C-DEPT sont disponibles sur demande.
Bibliographie
FAQ
Bibliographie
- Solladie, Guy; Girardin, Andre, Synthèse hautement stéréosélective de la vitamine A et de l'acide rétinoïque tout-trans par élimination réductrice induite par le titane de faible valence, Tetrahedron Letters, Volume : 29, Numéro : 2, Pages : 213-16, 1988
- Frolik, Charles A. ; Tavela, Thomas E. ; Peck, Gary L. ; Sporn, Michael B., Détermination par chromatographie liquide à haute pression de l'acide 13-cis-rétinoïque et de l'acide tout-trans-rétinoïque dans le plasma humain, Analytical Biochemistry, Volume : 86, Numéro : 2, Pages : 743-50, 1978
Foire aux Questions
Quelle est la limite acceptable des impuretés de l’acide rétinoïque ?
Les limites acceptables pour les impuretés de l'acide rétinoïque définies par les autorités réglementaires ou les normes de la pharmacopée diffèrent en fonction du type d'impureté spécifique et de son impact potentiel sur la sécurité et l'efficacité du médicament.
Les impuretés de l’acide rétinoïque peuvent-elles être minimisées ?
Oui, la présence d'impuretés d'acide rétinoïque peut être minimisée grâce à un contrôle et une surveillance minutieux pendant le processus de fabrication et par la mise en œuvre de techniques de purification.
Quelle est la directive réglementaire concernant les impuretés de l’acide rétinoïque ?
Les lignes directrices réglementaires concernant les impuretés de l'acide rétinoïque sont déterminées par diverses autorités réglementaires, qui fournissent des recommandations et leurs limites dans les substances pharmaceutiques.
Quelles sont les conditions de température requises pour stocker les impuretés de l’acide rétinoïque ?
Les impuretés de l'acide rétinoïque doivent être conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.