Charger plus
Vous avez vu 9 sur 10 articles
Daicel Pharma synthétise les standards d'impuretés du raloxifène tels que le dimère de raloxifène, le N-oxyde de raloxifène, le chlorhydrate d'acide 2-(4-hydroxyphényl)benzo[b]thiophène-5-ol, le chlorhydrate d'acide 4-(3-(pipéridin-1-yl) propoxy) benzoïque (propyle analogue du composé PA), et plus encore. Ces impuretés sont essentielles pour évaluer la qualité, la stabilité et la sécurité du raloxifène, qui est un ingrédient pharmaceutique actif. De plus, Daicel Pharma propose une synthèse personnalisée des impuretés du raloxifène et les livre dans le monde entier.
Le raloxifène [CAS : 84449/90/1] appartient à la famille des 1-benzothiophènes destinés au traitement de l'ostéoporose. Il fonctionne comme un conservateur de la densité osseuse, un modulateur des récepteurs des œstrogènes et un antagoniste des œstrogènes.
Le raloxifène est destiné aux femmes ménopausées pour prévenir et traiter l'ostéoporose, y compris la perte osseuse induite par les corticostéroïdes, et pour réduire le risque de cancer du sein invasif chez les femmes ménopausées souffrant d'ostéoporose ou à haut risque de cancer du sein invasif. Ce médicament est disponible sous la marque Evista.
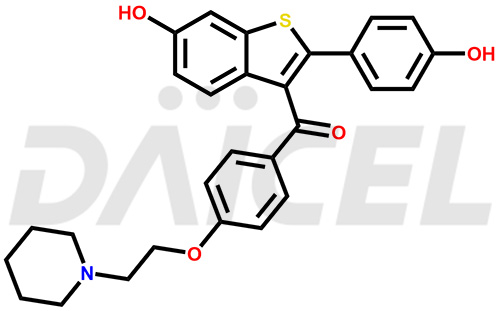
Le nom chimique du raloxifène est [6-Hydroxy-2-(4-hydroxyphényl)benzo[b]thien-3-yl][4-[2-(1-pipéridinyl)éthoxy]phényl]méthanone. Sa formule chimique est C28H27NON4S, et son poids moléculaire est d'environ 473.6 g/mol.
Le raloxifène prévient la production de cytokines et diminue la résorption osseuse chez les femmes ménopausées.
Les impuretés du raloxifène sont des composés chimiques qui se forment en plus de l'API du raloxifène cible lors de sa fabrication.1 ou du stockage. Ils proviennent de matières premières, de réactifs, d’intermédiaires ou de produits de dégradation. L'identification et la caractérisation des impuretés garantissent la qualité, la sécurité et l'efficacité du produit final à base de raloxifène.
Daicel Pharma propose un certificat d'analyse (CoA) pour les normes d'impuretés du raloxifène qui incluent le dimère de raloxifène, le N-oxyde de raloxifène, le 2-(4-hydroxyphényl)benzo[b]thiophène-5-ol, le 4-(3-(pipéridine-1) -yl) propoxy) chlorhydrate d'acide benzoïque (analogue propylique du composé PA), et plus encore. Notre CoA provient de notre laboratoire d'analyse certifié cGMP et comprend des données de caractérisation détaillées telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. Plus de détails de caractérisation, tels que ceux du 13C-DEPT, peuvent être fournis sur demande. Notre équipe de professionnels chez Daicel Pharma est spécialisée dans la synthèse des impuretés du raloxifène et des composés marqués pour tester l'efficacité du raloxifène générique. Nous fournissons le Raloxifène D4, un étalon de Raloxifène marqué au deutérium, essentiel pour la recherche bioanalytique et les études de biodisponibilité/bioéquivalence (BA/BE).
La présence d'impuretés dans le raloxifène pourrait potentiellement influencer la biodisponibilité du médicament.
Les impuretés du raloxifène peuvent varier d'un lot à l'autre et peuvent ne pas être cohérentes.
Les impuretés du raloxifène peuvent se former lors de divers processus tels qu'une dégradation, des réactions secondaires ou une purification incomplète lors de la synthèse ou du stockage du médicament.
Les impuretés du raloxifène sont conservées à une température ambiante régulée de 2 à 8 °C ou comme spécifié sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.