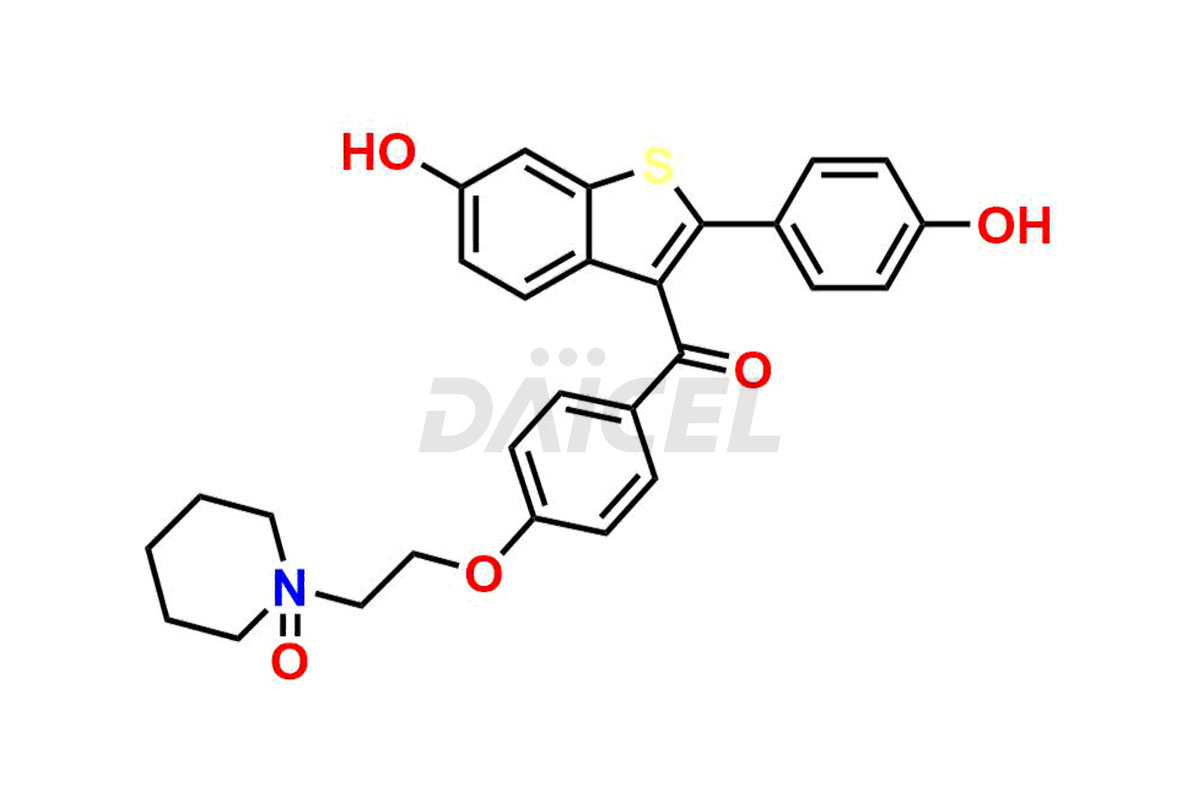
Le raloxifène
Bibliographie
- Jones, Charles David, Composés de benzothiophène et procédé pour les préparer, Eli Lilly and Co., États-Unis, EP0062503A1, 13 octobre 1982
- Basavaiah, Kanakapura ; Kumar, Urdigere Rangachar Anil ; Tharpa, Kalsang, Analyse HPLC gradient du chlorhydrate de raloxifène et son application au contrôle de la qualité des médicaments, Acta Pharmaceutica (Zagreb, Croatie), Volume : 58, Numéro : 3, Pages : 347-356, 2008
Foire aux Questions
Les impuretés du raloxifène peuvent-elles influencer la biodisponibilité du médicament ?
La présence d'impuretés dans le raloxifène pourrait potentiellement influencer la biodisponibilité du médicament.
Les impuretés du raloxifène sont-elles spécifiques au lot ou cohérentes ?
Les impuretés du raloxifène peuvent varier d'un lot à l'autre et peuvent ne pas être cohérentes.
Comment se forment les impuretés du raloxifène ?
Les impuretés du raloxifène peuvent se former lors de divers processus tels qu'une dégradation, des réactions secondaires ou une purification incomplète lors de la synthèse ou du stockage du médicament.
Quelles sont les conditions de température requises pour stocker les impuretés du raloxifène ?
Les impuretés du raloxifène sont conservées à une température ambiante régulée de 2 à 8 °C ou comme spécifié sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.