Pramipexole
Renseignements généraux
Impuretés du pramipexole et pramipexole
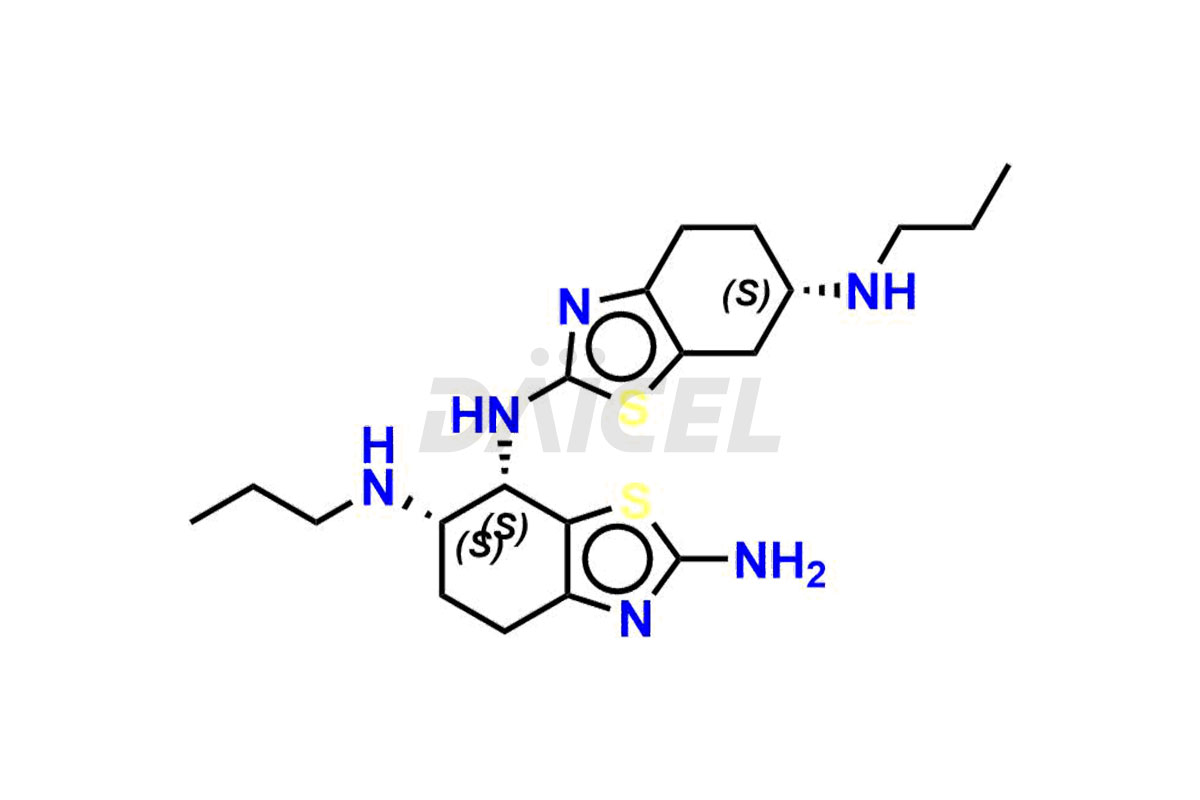
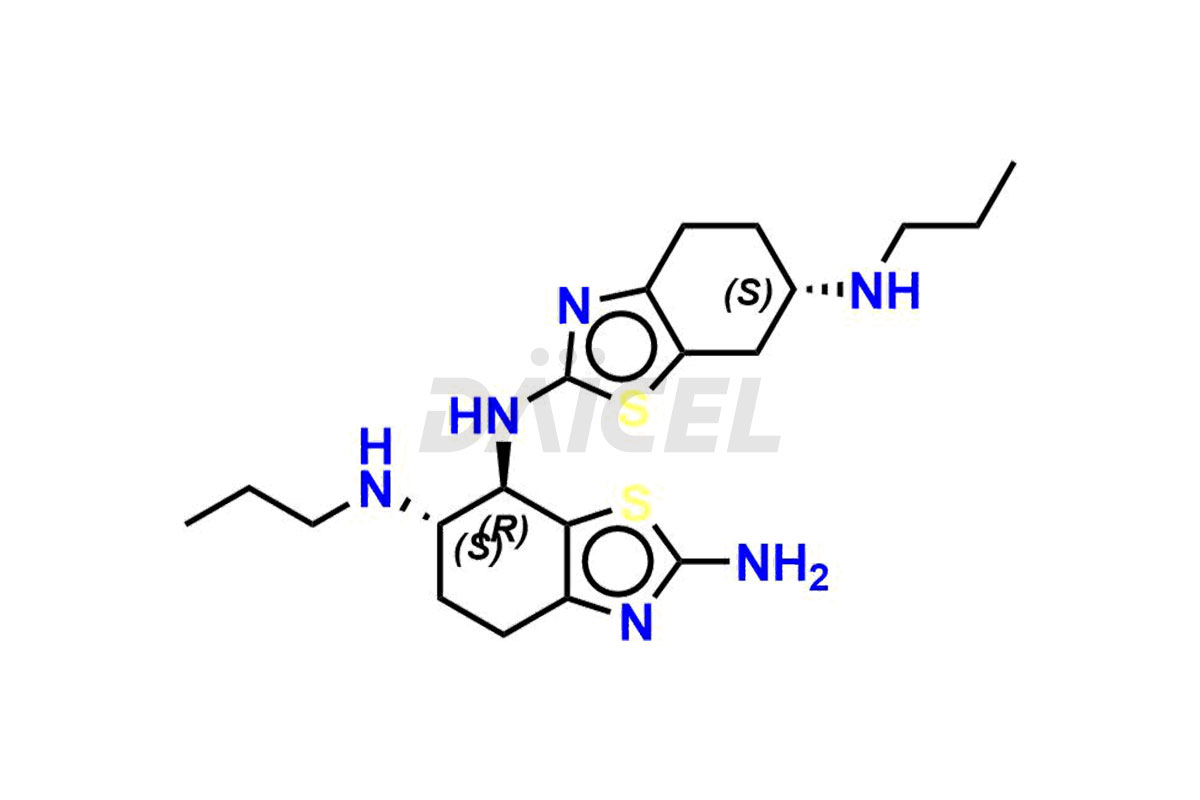
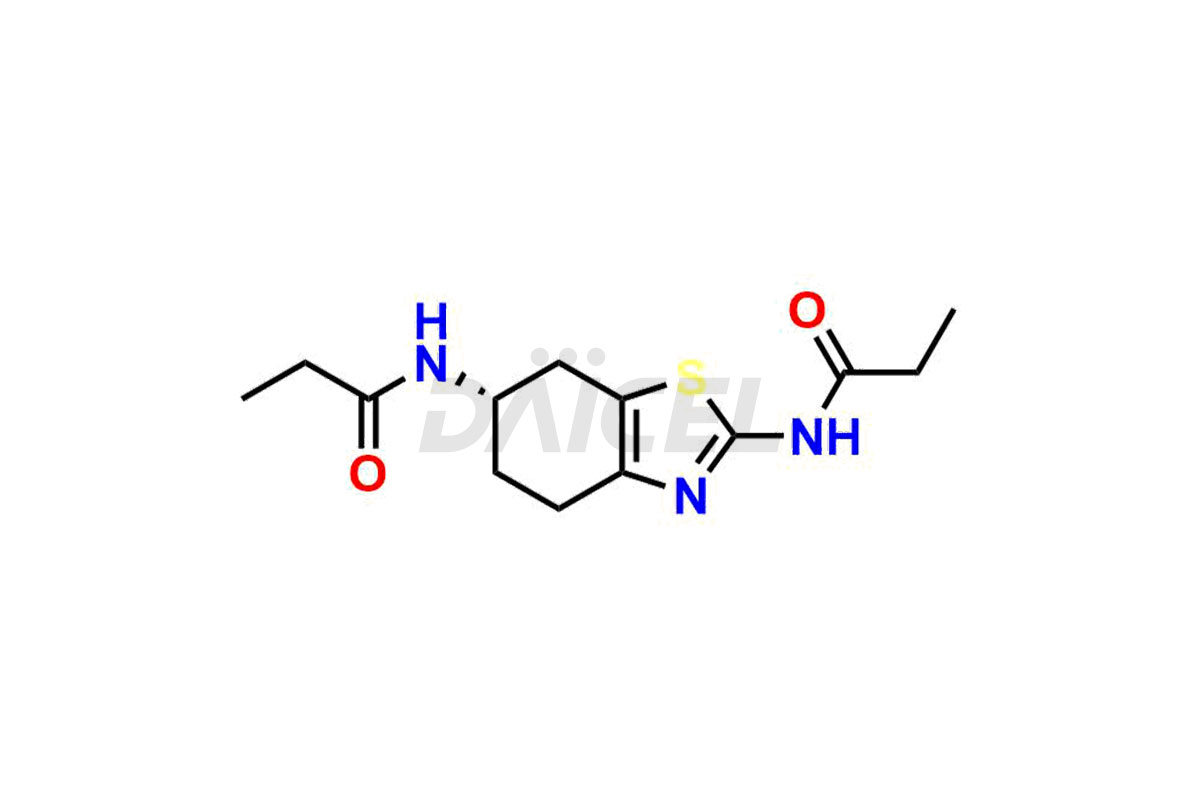
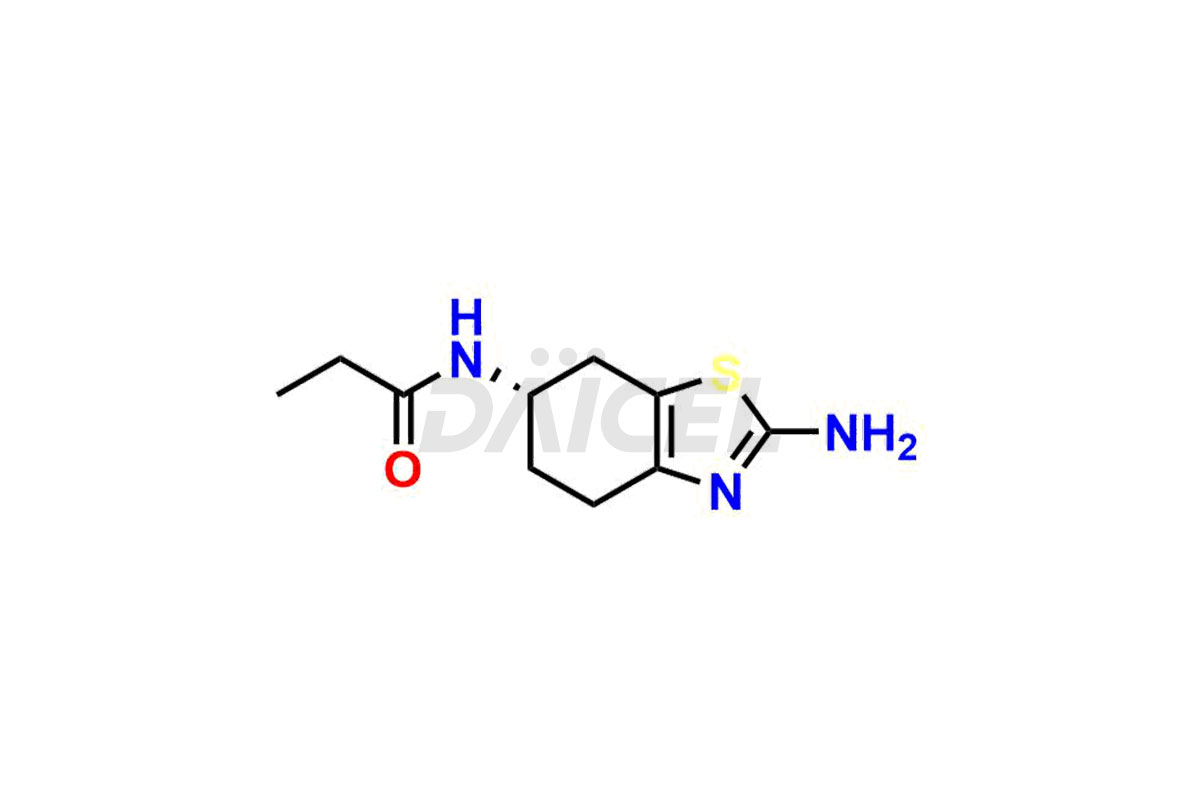
Daicel Pharma synthétise des impuretés de pramipexole de haute qualité, le dimère de pramipexole, le dimère de pramipexole-I, le dimère de pramipexole-II, l'impureté de pramipexole 29, l'impureté de pramipexole E (BP) et le composé D apparenté au pramipexole, qui sont cruciaux dans l'analyse de la qualité, de la stabilité et sécurité biologique du principe pharmaceutique actif pramipexole. De plus, Daicel Pharma propose une synthèse personnalisée d'impuretés de pramipexole et les livre dans le monde entier.
Pramipexole [CAS : 104632-26-0] est un médicament qui stimule les récepteurs de la dopamine. Il traite la maladie de Parkinson et le syndrome des jambes sans repos. Il appartient à la classe des médicaments antiparkinsoniens.
Pramipexole : utilisation et disponibilité commerciale
Le pramipexole est un agoniste dopaminergique non dérivé de l'ergot qui traite la maladie de Parkinson et le syndrome des jambes sans repos. Il peut être utilisé en monothérapie ou en complément d’autres agents de première intention pour la maladie de Parkinson. Le pramipexole fait l'objet de recherches pour traiter la dépression bipolaire, la dépression résistante au traitement, etc. Le pramipexole est disponible sous des marques telles que Mirapex, Pramipexole Dihydrochloride et Mirapex Er.
Structure et mécanisme d'action du pramipexole 
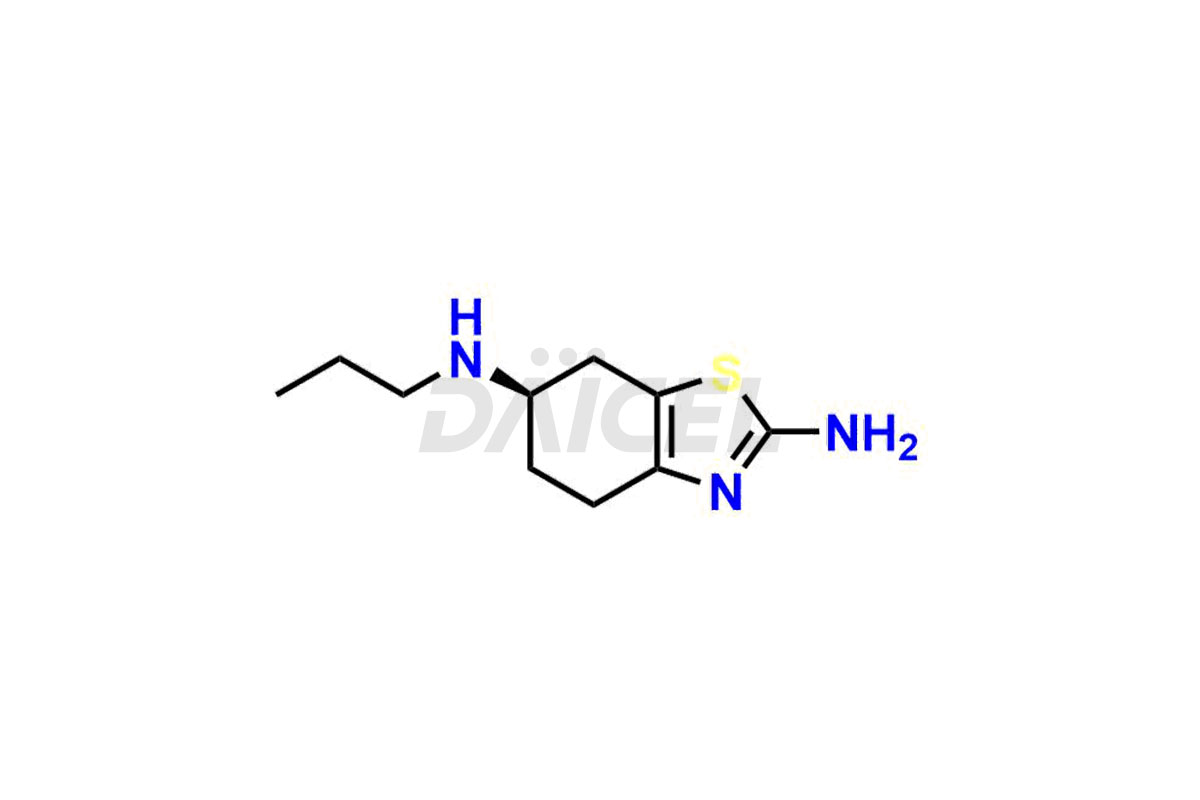
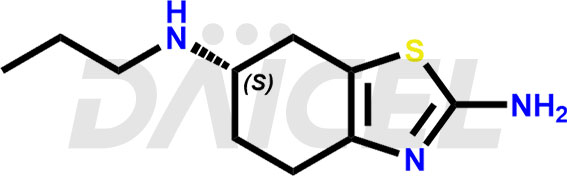
Le nom chimique du pramipexole est (6S)-4,5,6,7-Tetrahydro-N6-propyl-2,6-benzothiazolediamine. Sa formule chimique est C10H17N3S, et son poids moléculaire est d'environ 211.33 g/mol.
Le pramipexole a une activité intrinsèque sur la sous-famille D2 des récepteurs de la dopamine. Il s'agit d'un agoniste dopaminergique non ergot de seigle avec une affinité de liaison plus élevée pour le sous-type du récepteur D3.
Impuretés et synthèse du pramipexole
Des impuretés de pramipexole se forment lors de la synthèse1,2, la purification ou le stockage du médicament. Ces impuretés peuvent inclure des produits d'oxydation, des produits de dégradation résultant de l'exposition à la lumière ou à l'humidité et des solvants résiduels issus du processus de purification. La formation de ces impuretés peut affecter la puissance et la sécurité du médicament et, par conséquent, leurs niveaux doivent être soigneusement surveillés et contrôlés pendant la fabrication et le stockage.
Daicel propose un certificat d'analyse (CoA) d'un centre d'analyse conforme aux BPF c pour les normes d'impuretés du pramipexole, le dimère du pramipexole, le dimère du pramipexole-I, le dimère du pramipexole-II, l'impureté 29 du pramipexole, l'impureté E du pramipexole (BP) et le composé D apparenté au pramipexole. Le CoA comprend des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.3. Nous fournissons également du 13C-DEPT et du CHN sur demande. Nous remettons un rapport de caractérisation complet à la livraison. Daicel possède la technologie et l'expertise nécessaires pour préparer toute impureté ou produit de dégradation inconnu du pramipexole.
Bibliographie
FAQ
Bibliographie
- Griss, Gerhart ; Schneider, Claus; Hurnaus, Rudolf ; Kobinger, Walter ; Pichler, Ludwig ; Bauer, Rudolf ; Mierau, Joachim; Hinzen, Dieter ; Schingnitz, Guenter, Tetrahydro-benzthiazoles, leur préparation et leur utilisation comme produits intermédiaires ou comme produits pharmaceutiques, Thomae, Dr. Karl, GmbH, République fédérale d'Allemagne, US4731374A, 15 mars 1988
- Schneider, Claus S. ; Mierau, Joachim, Agonistes des autorécepteurs de la dopamine : résolution et activité pharmacologique du 2,6-diaminotétrahydrobenzothiazole et d'un analogue aminothiazole de l'apomorphine, Journal of Medicinal Chemistry, Volume : 30, Numéro : 3, Pages : 494-8, 1987
- Bharathi, D. Vijaya ; Hotha, Kishore Kumar ; Sagar, PV Vidya ; Kumar, S. Sirish ; Naidu, A. ; Mullangi, Ramesh, Développement et validation d'une méthode LC-MS/MS sensible avec ionisation par électrospray pour la quantification du pramipexole dans le plasma humain : application à une étude pharmacocinétique clinique, Chromatographie biomédicale, Volume : 23, Numéro : 2, Pages : 212-218 , 2009
Foire aux Questions
Comment minimiser les impuretés présentes dans le pramipexole ?
Les impuretés contenues dans le pramipexole sont minimisées grâce à l'utilisation de matières premières, de réactifs et de solvants de qualité supérieure et au raffinement du processus de fabrication. De plus, il est crucial de maintenir des conditions de stockage appropriées pour éviter la formation d’impuretés.
Les impuretés du pramipexole peuvent-elles affecter sa biodisponibilité ?
Les impuretés du pramipexole affectent sa biodisponibilité en modifiant sa pharmacocinétique. Par exemple, peu d’impuretés sont plus facilement absorbées par l’organisme que l’API, ce qui entraîne une modification de la concentration et de l’efficacité du médicament.
Quel solvant aide à l’analyse des impuretés du pramipexole ?
Le méthanol est le solvant utilisé pour analyser de nombreuses impuretés du pramipexole.
Quelles sont les conditions de température nécessaires pour conserver les impuretés du pramipexole ?
Les impuretés du pramipexole sont conservées à une température ambiante contrôlée entre 2 et 8 ⁰C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.