Charger plus
Vous avez vu 9 sur 17 articles
Daicel Pharma est une source fiable pour synthétiser des impuretés du Nirmatrelvir de haute qualité, en particulier l'impureté acide du Nirmatrelvir, l'impureté chloro du Nirmatrelvir, le chlorhydrate de l'impureté-1 du Nirmatrelvir, le diastéréomère du Nirmatrelvir INT -1, le diastéréomère du Nirmatrelvir INT -2, etc. Ces impuretés aident à évaluer la qualité, la stabilité, et la sécurité de l'ingrédient pharmaceutique actif, le Nirmatrelvir. Daicel Pharma propose également une synthèse personnalisée des impuretés du Nirmatrelvir, qui peut être expédiée dans le monde entier.
nirmatrelvir [CAS : 2628280/40/8] est un médicament oral et fonctionne comme un inhibiteur peptidomimétique de la protéase principale (Mpro) du coronavirus-2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), également connu sous le nom de protéase de type 3C ou protéase 3CL ou protéase nsp5. Son activité antivirale potentielle est dirigée contre le SRAS-CoV-2 et d’autres types de coronavirus.
Le nirmatrelvir, en association avec le ritonavir, a obtenu une autorisation d'utilisation d'urgence de la FDA pour le traitement du COVID-19 léger à modéré chez les patients qui ont été testés positifs pour le SRAS-CoV-2 et qui présentent un risque élevé de maladie grave. L'utilisation de la même combinaison est également approuvée au Canada et en Europe sous autorisation de mise sur le marché conditionnelle. Paxlovid est une association co-emballée de Nirmatrelvir et de Ritonavir utilisée pour traiter le COVID-19 chez les adultes présentant un risque accru d'évolution vers une maladie grave et ne nécessitant pas d'oxygène supplémentaire.
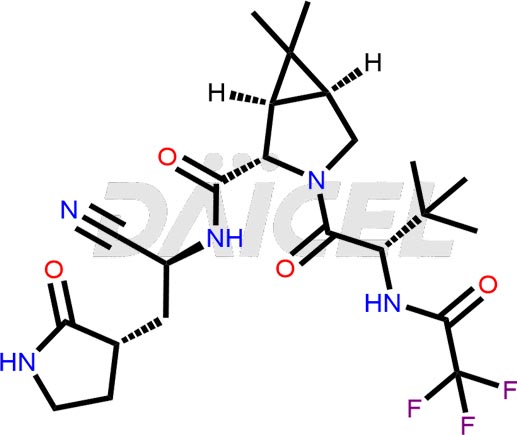
Le nom chimique du nirmatrelvir est (1R,2S,5S)-N-{(1S)-1-cyano-2-[(3S)-2-oxopyrrolidin-3-yl]éthyl}-3-[(2S)- 3,3-diméthyl-2-(2,2,2-trifluoroacétamido)butanoyl]-6,6-diméthyl-3-azabicyclo[3.1.0]hexane-2-carboxamide. Sa formule chimique est C23H32F3N5O4, et son poids moléculaire est d'environ 499.5 g/mol.
Le nirmatrelvir inhibe les résidus de cystéine dans le 3CLPRO du SRAS-CoV-2. Il restreint l'activité de 3CLPRO, empêchant ainsi la réplication du virus.
Les informations disponibles sur les impuretés du Nirmatrelvir sont limitées. Cependant, comme pour toute substance médicamenteuse, des impuretés peuvent se former au cours du processus de fabrication.1, le stockage ou les tests de stabilité. Ils peuvent affecter la qualité, la sécurité et l’efficacité des médicaments. Il est donc essentiel de les identifier et de les contrôler dans des limites acceptables tout au long du processus de développement du médicament.
Daicel Pharma fournit un certificat d'analyse (CoA) pour les normes d'impuretés du Nirmatrelvir, qui incluent l'impureté acide du Nirmatrelvir, l'impureté chloro du Nirmatrelvir, le chlorhydrate de l'impureté-1 du Nirmatrelvir, le diastéréomère du Nirmatrelvir INT -1, le diastéréomère du Nirmatrelvir INT -2, etc. installation analytique qui adhère aux bonnes pratiques de fabrication (cGMP) actuelles et comprend des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC2. Nous fournissons des données de caractérisation supplémentaires telles que 13C-DEPT et CHN sur demande. Daicel Pharma peut également générer des impuretés ou des produits de dégradation inconnus du Nirmatrelvir et fournir des composés marqués pour évaluer l'efficacité du Nirmatrelvir. De plus, Daicel Pharma propose le Nirmatrelvir-D9, un étalon de Nirmatrelvir marqué au deutérium utilisé dans la recherche bioanalytique, telle que les études BA/BE. Un rapport de caractérisation complet fait partie de chaque livraison.
La limite acceptable pour les impuretés du nirmatrelvir est déterminée par les agences de réglementation telles que la FDA, l'EMA et l'ICH. La limite varie en fonction de l'impureté et de son impact potentiel sur la qualité, la sécurité et l'efficacité du médicament.
Les impuretés contenues dans le Nirmatrelvir sont contrôlées pendant le processus de fabrication en mettant en œuvre de bonnes pratiques de fabrication (BPF) et en utilisant des méthodes analytiques appropriées pour l'identification et la quantification des impuretés. Techniques de purification telles que la cristallisation, la distillation et la chromatographie pour éliminer les impuretés.
Une impureté génotoxique du Nirmatrelvir est une impureté susceptible de provoquer des mutations génétiques ou d'autres dommages génétiques. Les agences de réglementation imposent des limites strictes quant à la présence d'impuretés génotoxiques dans les produits pharmaceutiques en raison de leur potentiel cancérigène.
Les impuretés du nirmatrelvir sont conservées à une température ambiante contrôlée entre 2 et 8 ⁰C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.