Charger plus
Vous avez vu 9 sur 17 articles
Daicel Pharma fournit des impuretés Nilotinib de haute qualité, notamment l'isomère Nilotinib Regio (impureté Nilotinib-9), l'isomère NTB Amine Regio, l'impureté isomère 2-méthyle du Nilotinib, l'impureté Nilotinib E CRS, l'impureté Nilotinib F CRS, etc. Ces impuretés sont essentielles pour évaluer la qualité, la stabilité et la sécurité du Nilotinib. De plus, Daicel Pharma propose une synthèse personnalisée des impuretés du nilotinib et les expédie dans le monde entier.
Nilotinib [CAS : 641571/10/0] est un inhibiteur de la tyrosine kinase qui traite la leucémie myéloïde chronique (LMC).
Le nilotinib traite la leucémie myéloïde chronique (LMC) chez les patients en échec ou résistants à d'autres traitements. Il est disponible dans le commerce sous la marque Tasigna. Tasigna est approuvé pour traiter les adultes et les enfants atteints de leucémie myéloïde chronique (LMC) à chromosome Philadelphie positif nouvellement diagnostiquée en phase chronique.
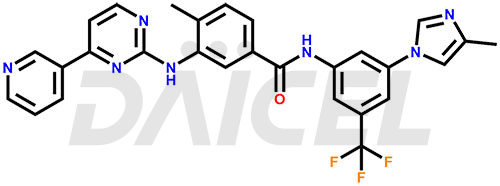
Le nom chimique du nilotinib est 4-Méthyl-N-[3-(4-méthyl-1H-imidazol-1-yl)-5-(trifluorométhyl)phényl]-3-[[4-(3-pyridinyl)-2 -pyrimidinyl]amino]benzamide. Sa formule chimique est C28H22F3N7O, et son poids moléculaire est d'environ 529.5 g/mol.
Le nilotinib inhibe la kinase Bcr-Abl. Il stabilise et se lie au domaine kinase de la protéine Abl.
Les composants ou sous-produits indésirables qui pourraient être présents dans le médicament Nilotinib sont appelés impuretés. Ces impuretés peuvent se développer en raison de la synthèse du médicament1, le stockage ou la détérioration. La pureté, la sécurité et l'efficacité du nilotinib doivent être contrôlées et surveillées.
Daicel fournit un certificat d'analyse (CoA) des normes d'impuretés du nilotinib telles que l'isomère Nilotinib Regio (impureté Nilotinib-9), l'isomère NTB Amine Regio, l'impureté isomère 2-méthyle du Nilotinib, l'impureté Nilotinib E CRS, l'impureté Nilotinib F CRS, etc. . Le CoA est proposé à partir d'un centre d'analyse conforme aux BPF et comprend des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. Sur demande, nous fournissons des données de caractérisation supplémentaires, telles que 13C-DEPT. Daicel Pharma peut fournir des impuretés ou des produits de dégradation inconnus du Nilotinib. Chaque livraison est accompagnée d'un rapport de caractérisation complet.
Le contrôle des impuretés du nilotinib s'effectue grâce à des mesures strictes de contrôle de qualité lors de la fabrication. Les autorités réglementaires fixent des limites spécifiques aux niveaux d'impuretés qui doivent être respectées.
Les impuretés du nilotinib peuvent affecter son efficacité en modifiant la pharmacocinétique, la pharmacodynamique ou la stabilité du médicament. Il est crucial de contrôler et de surveiller les impuretés afin que le médicament conserve sa puissance thérapeutique et produise les résultats thérapeutiques souhaités.
Les génériques du nilotinib sont soigneusement vérifiés pour détecter les impuretés afin de garantir leur qualité, leur sécurité et leur efficacité. Des études comparatives et un contrôle qualité approfondi contribuent à garantir que les versions génériques sont égales en termes de pureté et d’efficacité des médicaments.
Les impuretés du nilotinib doivent être conservées à une température ambiante contrôlée entre 2 et 8 °C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.