Charger plus
Vous avez vu 9 sur 24 articles
Daicel Pharma est un fournisseur de confiance de normes de qualité sur les impuretés du nébivolol, notamment (2S*,2'R*)-Nebivolol Impureté C, (2S*,2'S*)-Nebivolol Impureté C, (R, S, R, R )-Nébivolol, (R, S, S, S)-Nébivolol, (R*)-2-(benzylamino)-1-((S*)-6-fluorochroman-2-yl)éthan-1-ol et de nombreux plus. Ces impuretés sont essentielles pour déterminer la qualité, la stabilité et la sécurité biologique de l'ingrédient pharmaceutique actif Nebivolol. De plus, Daicel Pharma peut synthétiser les impuretés du Nebivolol selon les spécifications précises du client tout en garantissant une livraison dans le monde entier.
Nébivolol [N ° CAS: 99200-09-6] est un médicament appartenant à une classe de médicaments bêtabloquants. Il traite principalement l’hypertension artérielle (hypertension) et certaines maladies cardiaques.
Le nébivolol est un médicament bêtabloquant et antihypertenseur. Il gère l'hypertension artérielle et bloque l'action de certains produits chimiques dans le corps qui peuvent provoquer un rétrécissement des vaisseaux sanguins, entraînant un relâchement et un élargissement des vaisseaux sanguins. Le nébivolol gère la maladie coronarienne et l'insuffisance cardiaque chronique.
Le nébivolol est disponible sous la marque Bystolic, qui contient l'ingrédient actif Nebivolol.
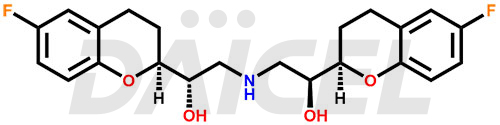
Le nom chimique du nébivolol est rel-(αR, α′R,2R,2′S)-α, α′-[Iminobis(méthylène)]bis[6-fluoro-3,4-dihydro-2H-1-benzopyrane. -2-méthanol]. Sa formule chimique est C22H25F2NON4, et son poids moléculaire est d'environ 405.4 g/mol.
Le mécanisme d’action du nébivolol est inconnu.
Des impuretés de nébivolol peuvent apparaître lors de la synthèse en raison du stockage ou de l'utilisation de matières premières et d'intermédiaires spécifiques dans la fabrication. Ces impuretés comprennent des composés apparentés, des produits de dégradation et des impuretés de processus. Des mesures de contrôle de qualité et des méthodes analytiques strictes sont essentielles pour garantir la pureté et la sécurité du Nebivolol destiné aux patients.
Daicel Pharma fournit un certificat d'analyse (CoA) complet pour les étalons d'impuretés du nébivolol, tels que (2S*, 2'R*)-nébivolol impureté C, (2S*, 2'S*)-nébivolol impureté C, (R, S, R, R)-Nébivolol, (R, S, S, S)-Nébivolol, (R*)-2-(benzylamino)-1-((S*)-6-fluorochroman-2-yl)éthane- 1-ol et bien d'autres. Le CoA comprend des données de caractérisation détaillées telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC. De plus, à la livraison, un 13C-DEPT complet est également fourni. Daicel Pharma possède la technologie et l'expertise nécessaires pour synthétiser toute impureté ou produit de dégradation inconnu du nébivolol. Nous proposons des composés étiquetés pour quantifier l'efficacité du Nebivolol générique. Daicel Pharma fournit également le (R, S, S, S)-Nebivolol-D4, le Nitroso Nebivolol D4 et le (S, R, R, R)-Nebivolol-D4, des composés du Nebivolol marqués au deutérium, qui sont essentiels pour le BA/ Etudes BE.
Les méthodes analytiques telles que la méthode de chromatographie liquide ultra-performante en phase inverse aident à estimer quantitativement les impuretés du nébivolol.
Oui, les impuretés contenues dans le Nebivolol peuvent avoir un impact sur la sécurité des patients. Selon leur nature et leur concentration, les contaminants peuvent provoquer des effets indésirables ou réduire l’efficacité du médicament.
Le méthanol est utilisé pour atteindre la solubilité et la différenciation idéales des impuretés dans le Nebivolol.
Les impuretés du nébivolol doivent généralement être conservées à une température ambiante contrôlée entre 2 et 8 ⁰C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.