Mebeverine
Renseignements généraux
Impuretés de la mébévérine et mébévérine
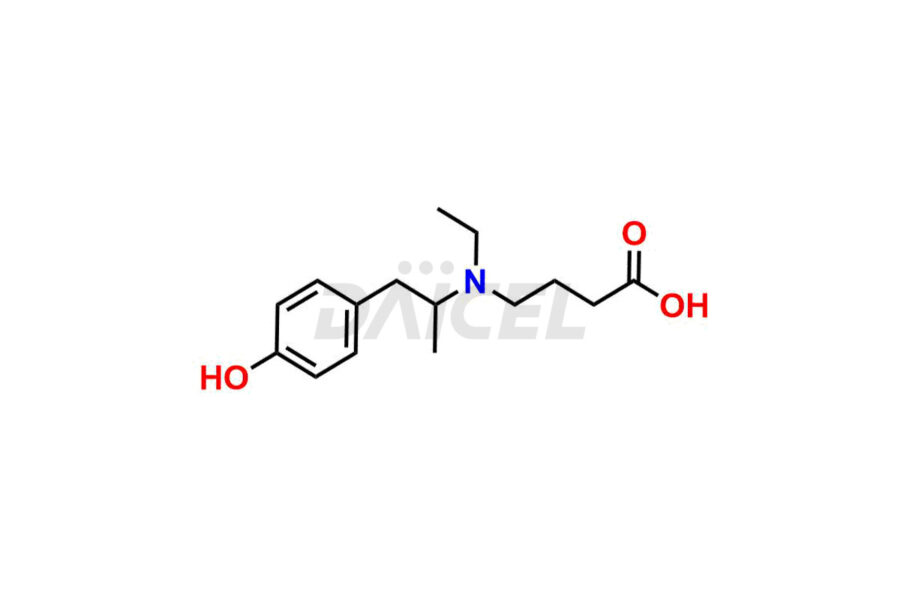
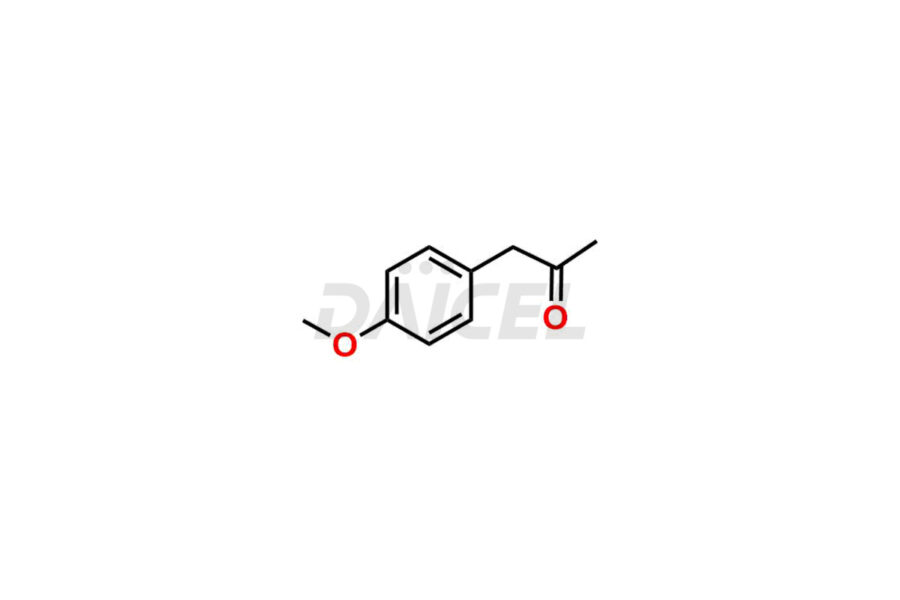
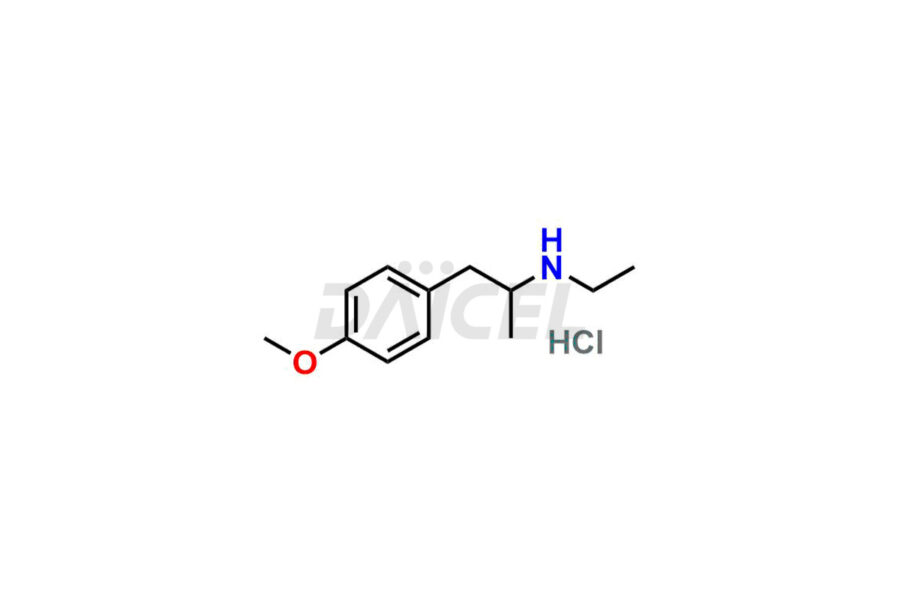
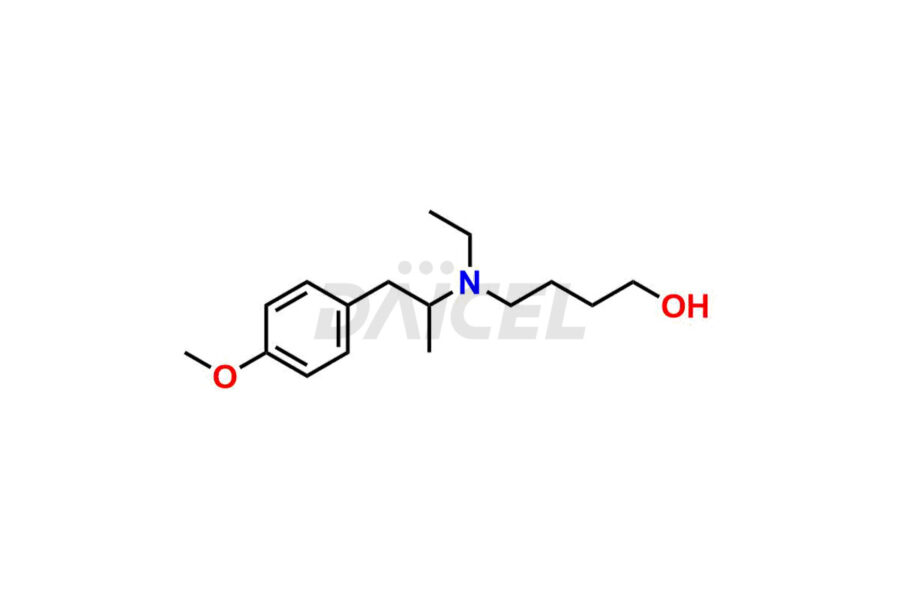
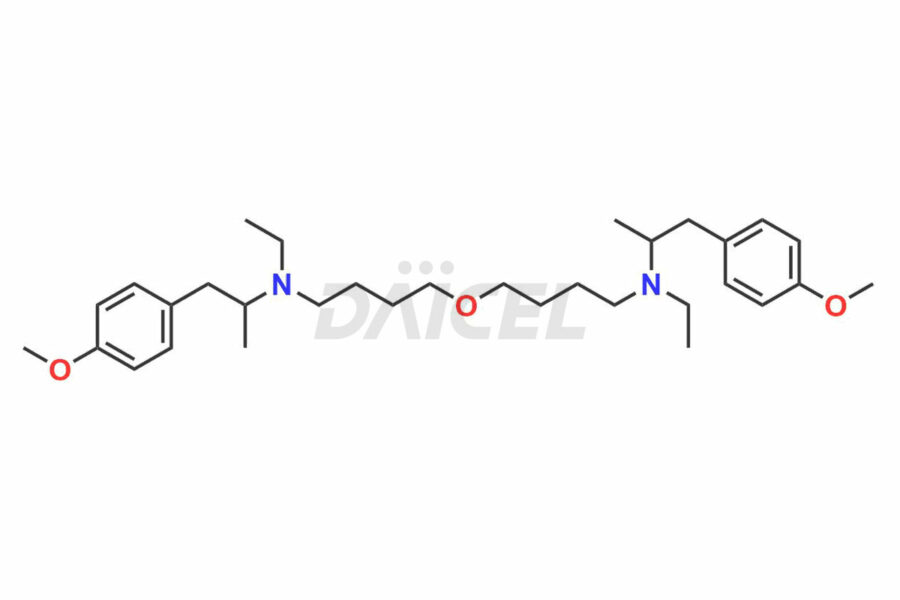
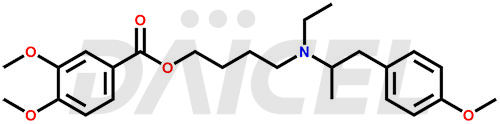
Pour évaluer la pureté et l'innocuité de la mébévérine, un ingrédient pharmaceutique actif, Daicel Pharma propose une synthèse personnalisée des standards d’impuretés de la Mébévérine. Ces étalons d'impuretés comprennent des composés cruciaux tels que l'acide desméthyl mébévérine, l'impureté A de la mébévérine EP, l'impureté B de la mébévérine EP, l'impureté C de la mébévérine EP et l'impureté J de la mébévérine. De plus, Daicel Pharma propose des options de livraison mondiales pour les étalons d'impuretés de la mébévérine.
Enquête sur les applications thérapeutiques de la mébévérine [CAS : 3625/06/7] s'est concentré sur le traitement du syndrome du côlon irritable (SCI) et des spasmes gastro-intestinaux post-cholécystectomie. Cet agent antispasmodique est destiné au soulagement symptomatique des douleurs abdominales causées par les spasmes des muscles lisses intestinaux et les troubles fonctionnels dus au SCI.
Mébévérine : utilisation et disponibilité commerciale
Les marques sous lesquelles la mébévérine est disponible sont Colofac, Colofac IBS, Aurobeverine, etc. La mébévérine agit comme un agent antispasmodique, ciblant directement les muscles lisses intestinaux. Le traitement par la mébévérine a montré des résultats positifs dans la réduction de différents symptômes intestinaux associés à des affections telles que le syndrome du côlon irritable (SCI), notamment les douleurs abdominales, l'inconfort, la distension, les habitudes intestinales irrégulières et les ballonnements.
Structure et mécanisme d'action de la mébévérine
Le nom chimique de la mébévérine est l'ester 3,4-[éthyl(p-méthoxy-α-méthylphénéthyl)amino]butylique de l'acide 4-diméthoxybenzoïque. Sa formule chimique est C25H35NON5, et son poids moléculaire est d'environ 429.5 g/mol.
Le mécanisme d’action de la mébévérine n’est pas connu.
Impuretés et synthèse de la mébévérine
Pour maintenir la pureté et la qualité de la mébévérine, des tests réguliers et une surveillance des impuretés sont cruciaux. La mébévérine, utilisée pour le traitement des troubles gastro-intestinaux, peut contenir des impuretés provenant de la fabrication1 ou une dégradation. Ils peuvent inclure des substances apparentées, des isomères ou des solvants résiduels utilisés pendant la production. Le respect des normes réglementaires garantit des niveaux d'impuretés acceptables dans les formulations de Mebeverine, garantissant ainsi la sécurité et l'efficacité du produit. Des mesures de contrôle de qualité rigoureuses et des techniques analytiques aident à identifier et à quantifier les impuretés dans les échantillons de mébévérine. La surveillance des impuretés de la mébévérine est essentielle pour son efficacité et son assurance qualité tout au long de sa durée de conservation.
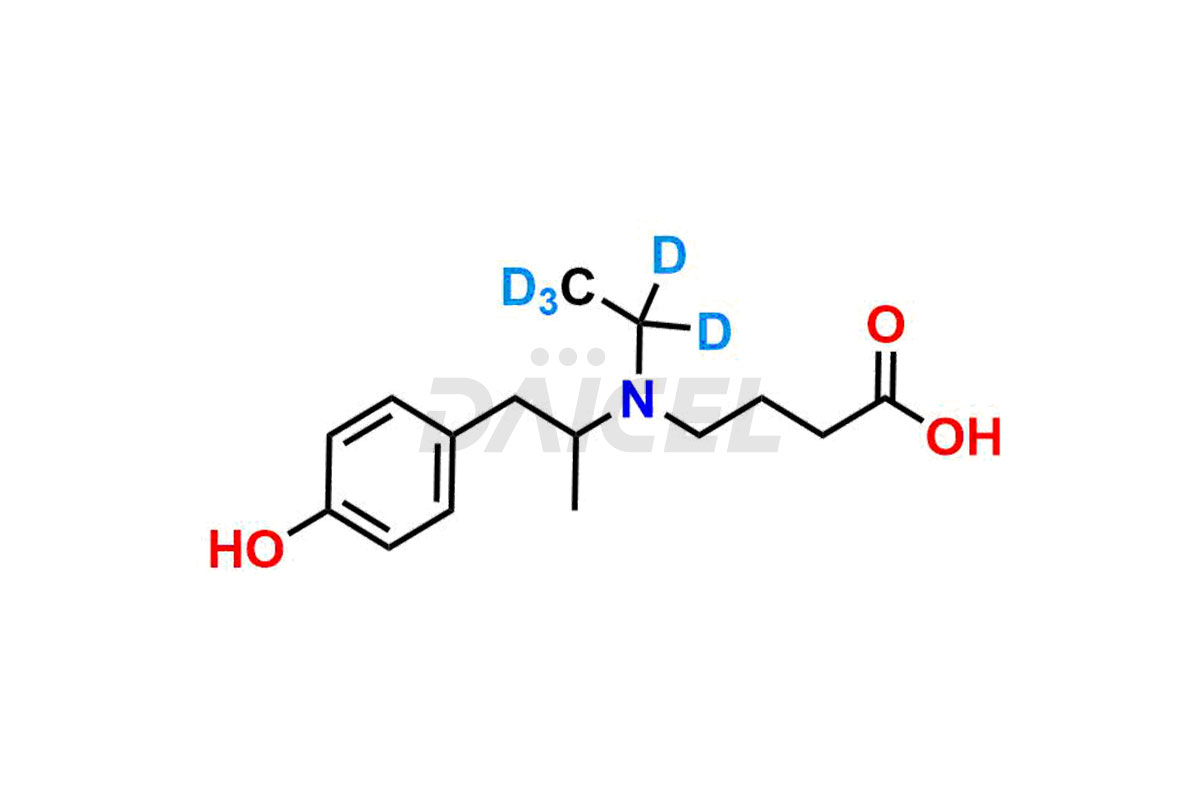
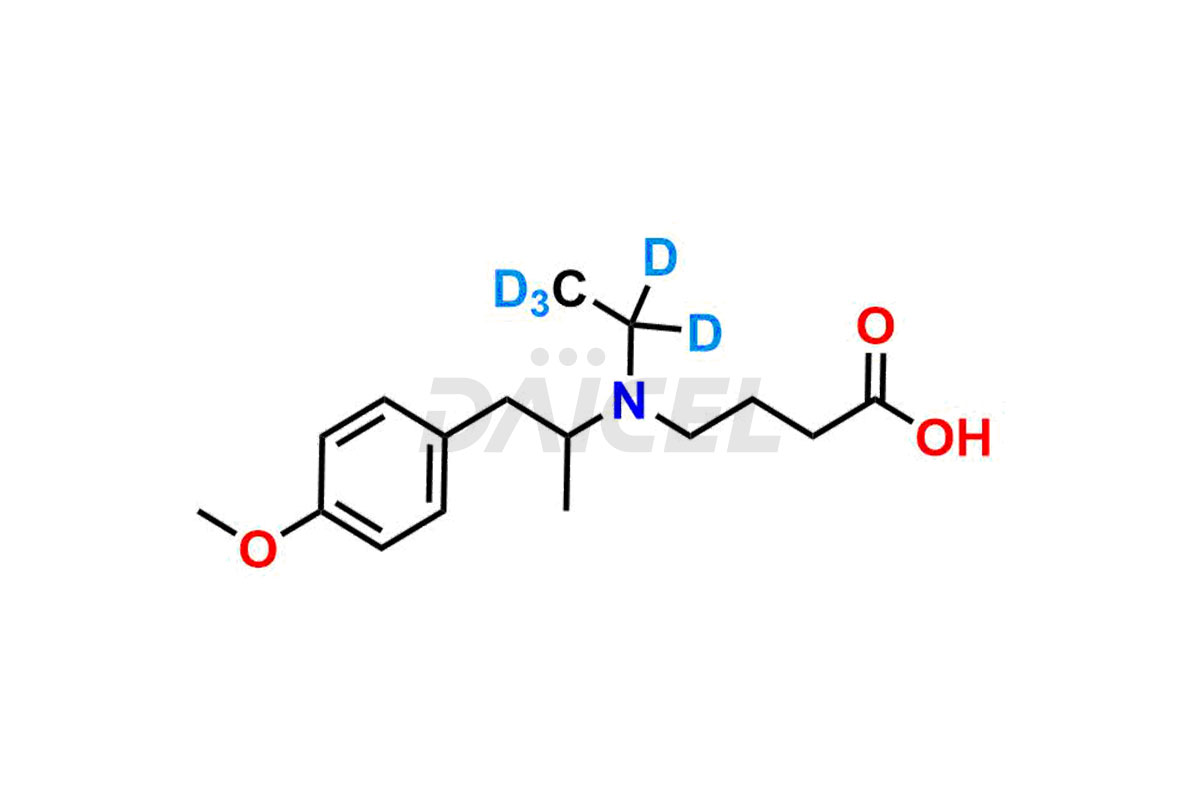
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés de mébévérine, qui comprennent l'acide desméthyl mébévérine, l'impureté A de mébévérine EP, l'impureté B de mébévérine EP, l'impureté C de mébévérine EP et l'impureté J de mébévérine. proposent l'acide desméthyl mébévérine D5 et l'acide mébévérine D5, des composés de mébévérine marqués au deutérium, qui sont essentiels à la conduite de recherches bioanalytiques et d'études BA/BE. Nos étalons d’impuretés mébévérine disposent d’un certificat d’analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. De plus, nous pouvons synthétiser des normes d'impuretés inconnues de la mébévérine, des produits de dégradation et des composés marqués pour évaluer l'efficacité de la mébévérine générique. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- V. Philips' Gloeilampenfabrieken, Améliorations apportées ou liées à la production d'alcools aminés estérifiés, GB1009082A, 3 novembre 1965
- De Schutter, JA; De Croo, F. ; Van der Weken, G. ; Van den Bossche, W. ; De Moerloose, P., Étude de stabilité et détermination quantitative du chlorhydrate de mébévérine dans des comprimés au moyen d'une chromatographie liquide haute performance en phase inversée, Chromatographia, Volume : 20, Numéro : 3, Pages : 185-92, 1985
Foire aux Questions
Les impuretés de la mébévérine peuvent-elles affecter la biodisponibilité du principe actif ?
Certaines impuretés présentes dans les formulations de mébévérine peuvent potentiellement avoir un impact sur la biodisponibilité de l'ingrédient actif, entraînant des variations dans l'absorption et l'efficacité du médicament.
Les impuretés de la mébévérine sont-elles testées pour leurs interactions potentielles avec d'autres médicaments ?
Les impuretés contenues dans la mébévérine ne sont pas testées pour détecter des interactions spécifiques avec d'autres médicaments. Cependant, les interactions médicamenteuses impliquant le principe actif sont prises en compte sur la base des connaissances cliniques.
Les impuretés de la mébévérine peuvent-elles être présentes sous différentes formes polymorphes ?
Les impuretés contenues dans la mébévérine peuvent exister sous différentes formes polymorphes, influençant leurs propriétés physicochimiques et leur impact potentiel sur la qualité du produit.
Quelle est la température de conservation recommandée pour les impuretés de la Mébévérine ?
Les impuretés de la mébévérine doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.