Charger plus
Vous avez vu 9 sur 17 articles
Pour évaluer la pureté et l'innocuité de la lurasidone, un ingrédient pharmaceutique actif, Daicel Pharma propose une synthèse personnalisée des standards d’impuretés de Lurasidone. Ces normes d'impuretés comprennent des composés cruciaux tels que l'impureté Endo-Époxyde de Lurasidone, la Lurasidone Endo Hydroxy, l'isomère de Lurasidone Endo-RS+SR (Cis-Endo), l'isomère de Lurasidone-1, l'impureté d'oléfine de Lurasidone-1, et plus encore. De plus, Daicel Pharma propose des options de livraison mondiales pour les étalons d'impuretés de Lurasidone.
Lurasidone [CAS : 367514/87/2] est un médicament antipsychotique atypique destiné au traitement de la schizophrénie et de la dépression bipolaire. Il agit comme un antagoniste adrénergique, dopaminergique et sérotoninergique, ce qui en fait un agent antipsychotique de deuxième génération. La lurasidone, sous sa forme de sel de chlorhydrate, est utilisée à des fins thérapeutiques.
La lurasidone, commercialisée sous le nom de marque Latuda, est un médicament appartenant à la classe des benzisothiazole. C'est un antipsychotique atypique utilisé pour traiter la schizophrénie et la dépression bipolaire. Initialement approuvé par la FDA pour traiter la schizophrénie chez les adultes, il a ensuite obtenu l'approbation de la FDA pour la dépression bipolaire en juin 2013. Il s'agit d'un développement important puisqu'il est devenu le premier médicament approuvé pour la monothérapie et le traitement d'appoint au lithium ou au valproate. Par la suite, en janvier 2017, la Lurasidone a reçu l’approbation de la FDA pour le traitement de la schizophrénie chez les adolescents. En mars 2018, son utilisation incluait des patients pédiatriques (âgés de 10 à 17 ans) pour traiter les épisodes dépressifs majeurs associés à la dépression bipolaire.
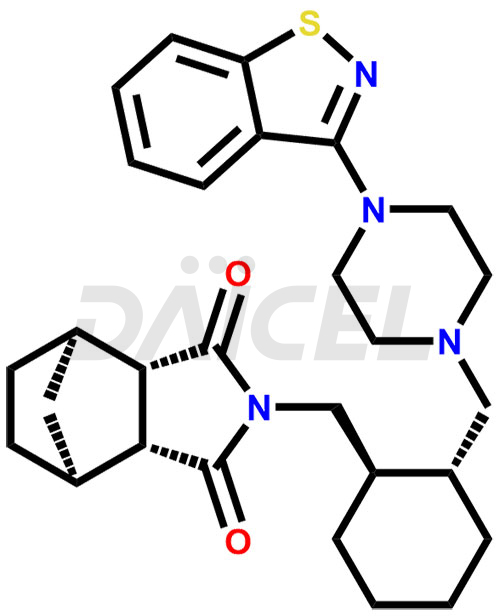
Le nom chimique de la lurasidone est (3aR,4S,7R,7aS)-2-[[(1R,2R)-2-[[4-(1,2-Benzisothiazol-3-yl)-1-pipérazinyl]méthyl] cyclohexyl]méthyl]hexahydro-4,7-méthano-1H-isoindole-1,3(2H)-dione. Sa formule chimique est C28H36N4O2S, et son poids moléculaire est d'environ 492.7 g/mol.
Le mécanisme d’action de la Lurasidone est inconnu.
L’analyse et le contrôle des impuretés de la Lurasidone1, un médicament antipsychotique, est essentiel pour garantir sa sécurité et son efficacité. Les impuretés contenues dans les formulations de lurasidone peuvent inclure des substances apparentées et des produits de dégradation. Les techniques analytiques telles que la chromatographie liquide haute performance (HPLC) et la chromatographie liquide (LC) aident à identifier et à quantifier les impuretés. Des mesures de contrôle et des spécifications strictes limitent les niveaux d'impuretés dans la Lurasidone, conformément aux exigences réglementaires.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés de Lurasidone, qui comprennent l'impureté Endo-Epoxyde de Lurasidone, Lurasidone Endo Hydroxy, Lurasidone Endo-RS+SR Isomer (Cis-Endo), Lurasidone isomer-1. , Lurasidone Olefin Impurity-1, et plus encore. Nos étalons d'impuretés de lurasidone disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. De plus, nous pouvons synthétiser des étalons d’impuretés et des produits de dégradation inconnus de la lurasidone. Chaque livraison dispose d'un rapport de caractérisation complet.
Oui, les impuretés contenues dans la lurasidone peuvent affecter sa biodisponibilité en modifiant ses propriétés pharmacocinétiques, telles que l'absorption, la distribution, le métabolisme et l'excrétion. Leur contrôle garantit des performances constantes du médicament.
Les recherches en cours visent à développer des méthodes d'analyse et des processus de fabrication plus efficaces pour minimiser les impuretés contenues dans la Lurasidone, garantissant ainsi qu'elle répond aux normes de qualité et de sécurité les plus élevées.
Les fabricants mettent en œuvre des contrôles rigoureux en cours de processus et effectuent des tests et une surveillance réguliers des matières premières, des produits intermédiaires et des produits finaux pour garantir que les niveaux d'impuretés dans la Lurasidone se situent dans des limites acceptables.
Les impuretés de la lurasidone doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.