Lumatepérone
Renseignements généraux
Impuretés de la lumatepérone et lumatepérone
Daicel Pharma est une source fiable pour synthétiser des impuretés de lumateperone de haute qualité, en particulier la desméthyl lumateperone, le métabolite de lumateperone 308, le métabolite de lumateperone 565, le métabolite de lumateperone M131, le métabolite de lumateperone M309, le tosylate de lumateperone et l'ortho isomère de lumateperone (sel de tosylate). Ces impuretés aident à évaluer la qualité, la stabilité et la sécurité de l’ingrédient pharmaceutique actif, la Lumateperone. Daicel Pharma propose également une synthèse personnalisée d'impuretés de Lumateperone, qui peut être expédiée dans le monde entier.
Lumatepérone [CAS : 313368/91/1] est un médicament antipsychotique atypique traitant la schizophrénie. Il appartient à la deuxième génération de médicaments antipsychotiques et module sélectivement et simultanément les niveaux de sérotonine, de dopamine et de glutamate dans le cerveau humain.
Lumateperone : utilisation et disponibilité commerciale
La lumatepérone est un médicament destiné au traitement de la schizophrénie chez l'adulte et des épisodes dépressifs associés au trouble bipolaire (appelé dépression bipolaire) chez l'adulte, seul ou en association avec du lithium ou du valproate. Il est disponible sous la marque Caplyta. La Lumateperone est un antipsychotique atypique de deuxième génération. Il est unique dans son mécanisme d’action pour gérer et traiter divers troubles neuropsychiatriques.
Structure et mécanisme d'action de la lumatepérone 
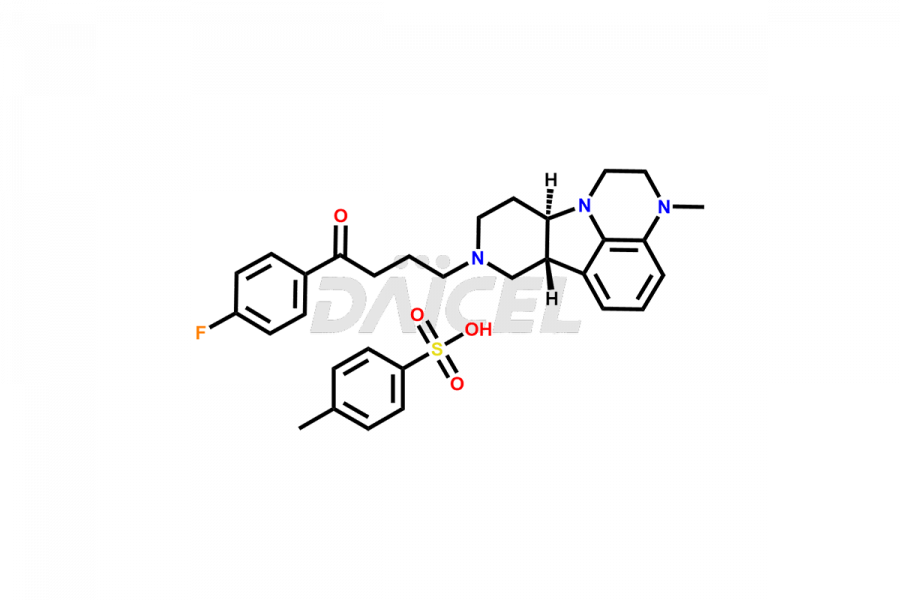
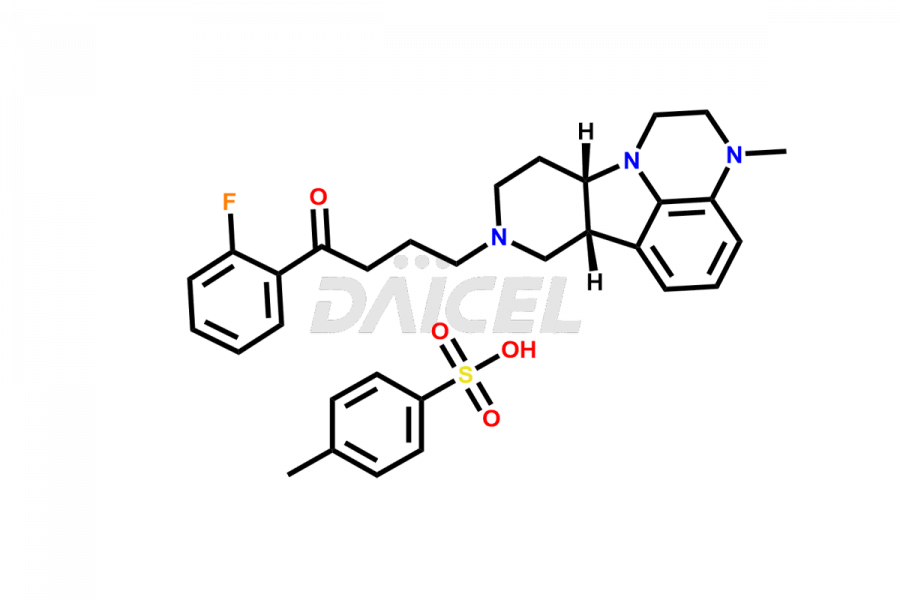
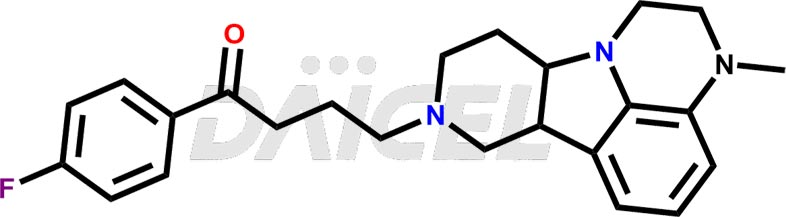
Le nom chimique de la Lumateperone est 1-(4-Fluorophényl)-4-[(6bR,10aS)-2,3,6b,9,10,10a-hexahydro-3-méthyl-1H-pyrido[3′,4′ :4,5]pyrrolo[1,2,3-de]quinoxalin-8(7H)-yl]-1-butanone. Sa formule chimique est C24H28FN3O, et son poids moléculaire est d'environ 393.5 g/mol.
Le mécanisme d'action de Lumateperone est inconnu concernant le traitement de la schizophrénie. Mais l’efficacité de la lumatepérone est médiée par une combinaison d’activité antagoniste postsynaptique au niveau des récepteurs centraux de la dopamine D2 et d’activité antagoniste au niveau des récepteurs centraux de la sérotonine 5-HT2A.
Impuretés et synthèse de la lumatepérone
Lors de la synthèse1 et le stockage de Lumateperone, des impuretés peuvent se former, notamment des impuretés dégradantes, liées au processus et potentiellement génotoxiques. Contrôle de ces impuretés2 est essentiel pour garantir la sécurité, la qualité et l’efficacité du médicament. Diverses techniques, telles que la chromatographie liquide haute performance (HPLC), sont utilisées pour identifier, quantifier et contrôler ces impuretés.
Daicel Pharma délivre un certificat d'analyse (CoA) pour les normes d'impuretés de la lumatepérone, notamment la desméthyl lumatepérone, le métabolite de la lumatepérone 308, le métabolite de la lumatepérone 565, le métabolite de la lumatepérone M131, le métabolite de la lumatepérone M309, le tosylate de lumatepérone et l'isomère ortho de la lumatepérone (sel de tosylate). Le CoA provient d'une installation d'analyse conforme aux bonnes pratiques de fabrication (cGMP) actuelles et comprend des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC. Nous fournissons des données de caractérisation supplémentaires telles que 13C-DEPT et CHN sur demande. Daicel Pharma peut préparer des impuretés ou des produits de dégradation inconnus de la Lumateperone et proposer des composés étiquetés pour aider à mesurer l'efficacité de la Lumateperone. De plus, nous proposons du sel tosylate de Lumateperone 13CD3 hautement pur, un étalon de Lumateperone marqué au deutérium pour la recherche bioanalytique et les études BA/BE. Un rapport de caractérisation complet accompagne chaque livraison.
Bibliographie
FAQ
Bibliographie
- Robichaud, Albert J.; Lee, Taekyu ; Deng, Wei; Mitchell, Ian S. ; Haydar, Simon ; Chen, Wenting; McClung, Christopher D. ; Calvello, Émilie JB; Zawrotny, David M., Gamma-carbolines fusionnées à hétérocycle substitué, Du Pont Pharmaceuticals Company, États-Unis, US6548493B1, 15 avril 2003
- Mates et.al, dérivés de Pyrido[3′,4′:4,5]pyrrolo[1,2,3-de]quinoxalines et [1,4]oxazino[2,3,4-hi]pyrido[4,3 -b]indole dérivés, Intra-Cellular Therapies, Inc, US8993572B2, 31 mars 2015
Foire aux Questions
Comment minimiser les impuretés contenues dans Lumateperone ?
Les impuretés contenues dans Lumateperone sont minimisées grâce à des matières premières de haute qualité, des processus de fabrication optimisés et des conditions de stockage appropriées. De plus, des méthodes analytiques les surveillent et les contrôlent.
Quel est le rôle des tests analytiques dans le contrôle des impuretés de Lumateperone ?
Les tests analytiques jouent un rôle essentiel dans le contrôle des impuretés contenues dans la Lumateperone en fournissant des informations sur l'identité et la quantité du produit médicamenteux.
Quel solvant aide à l’analyse des impuretés de Lumateperone ?
L'acétonitrile est un solvant utilisé dans l'analyse de nombreuses impuretés du Lumateperone.
Quelles sont les conditions de température nécessaires pour stocker les impuretés de Lumateperone ?
Les impuretés de Lumateperone sont conservées à une température ambiante contrôlée entre 2 et 8 ⁰C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.