Lovastatine
Renseignements généraux
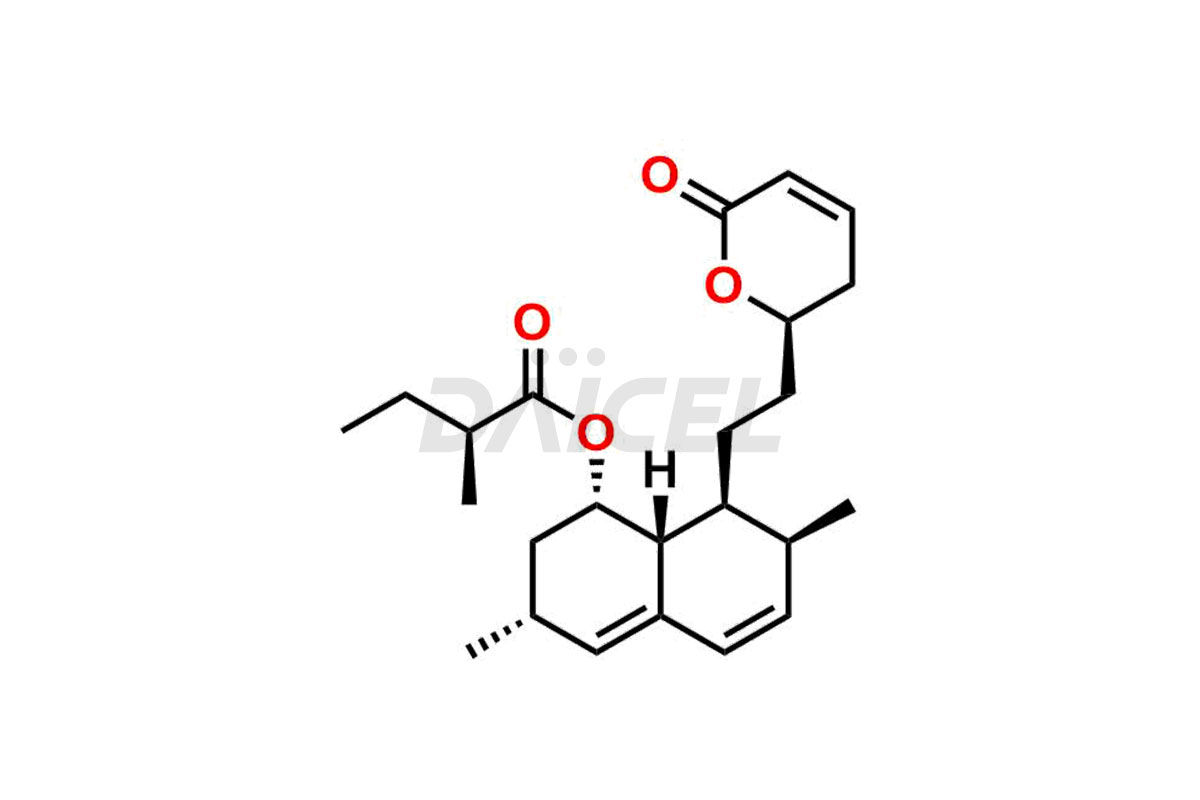
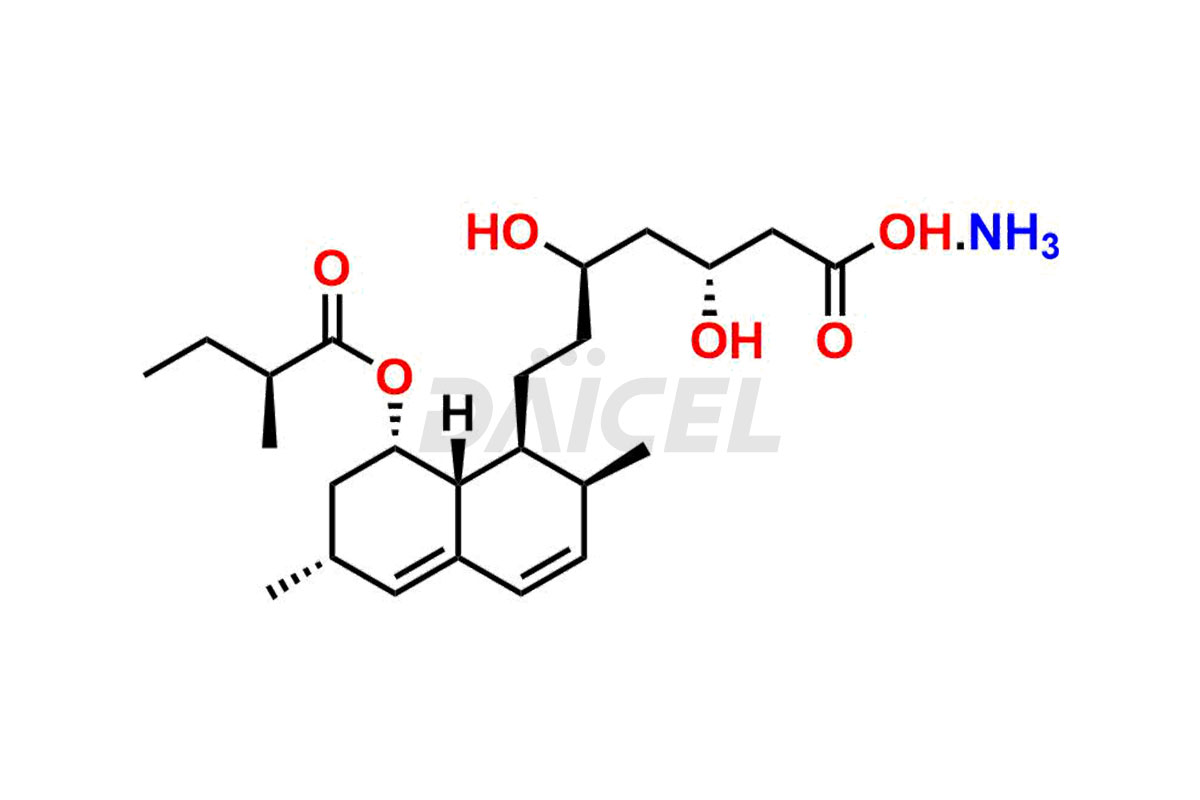
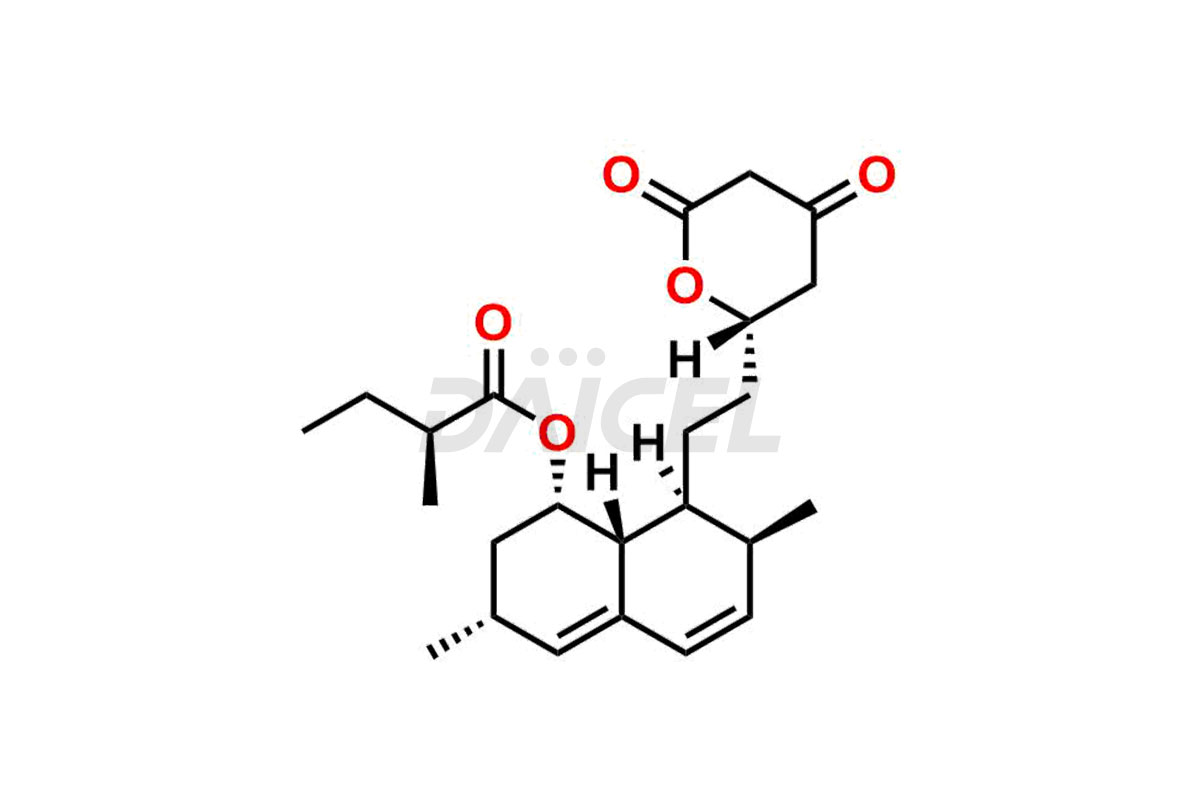
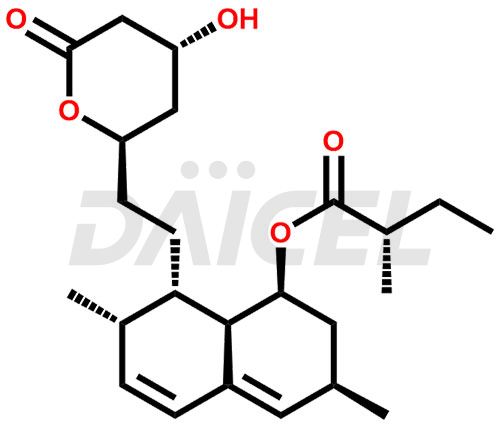
Impuretés de la lovastatine et lovastatine
Pour évaluer la pureté et l'innocuité de la Lovastatine, un ingrédient pharmaceutique actif, Daicel Pharma propose une synthèse personnalisée des standards d'impuretés de la lovastatine. Ces normes d'impuretés comprennent des composés cruciaux tels que la déhydro lovastatine, le sel d'ammonium de l'hydroxyacide de lovastatine et le composé n° 6 apparenté à la lovastatine. De plus, Daicel Pharma propose des options de livraison mondiales pour les étalons d'impuretés de la lovastatine.
Lovastatine [CAS : 75330/75/5], dérivé du champignon Aspergillus terreus, est un métabolite de lactone doté de propriétés hypocholestérolémiantes et d'effets antinéoplasiques. En tant que membre de la classe des médicaments des statines, il abaisse le taux de cholestérol dans le corps.
Lovastatine : utilisation et disponibilité commerciale
La lovastatine, commercialisée sous les marques Altoprev et Mevacor, est une statine utilisée pour traiter et prévenir diverses affections liées aux taux de lipides. Il traite les maladies coronariennes, l'hypercholestérolémie. Il traite également l'hypercholestérolémie familiale hétérozygote chez les adolescents. La lovastatine a été isolée d'une souche d'Aspergillus terreus.
Structure et mécanisme d'action de la lovastatine
Le nom chimique de la lovastatine est (1S,3R,7S,8S,8aR)-8-(2-((2R,4R)-4-hydroxy-6-oxotetrahydro-2H-pyran-2-yl)éthyl)-3,7 ,1,2,3,7,8,8-diméthyl-1a-hexahydronaphtalén-2-yle (S)-XNUMX-méthylbutanoate. Sa formule chimique est C24H36O5, et son poids moléculaire est d'environ 404.5 g/mol.
La lovastatine est hydrolysée en acide β-hydroxy, un inhibiteur de réduction de l'HMG-CoA. Il convertit en outre le HMG-CoA en mévalonate.
Impuretés et synthèse de la lovastatine
Dans l'industrie pharmaceutique, l'analyse et le contrôle des impuretés de la Lovastatine1, un médicament hypocholestérolémiant, est essentiel pour garantir sa sécurité et son efficacité. Ils peuvent inclure des composés apparentés et des produits de dégradation. Des techniques analytiques telles que la chromatographie liquide haute performance (HPLC) et la chromatographie liquide (LC) permettent d'identifier et de quantifier ces impuretés. Des mesures de contrôle et des spécifications strictes limitent la présence d'impuretés de lovastatine conformément aux directives réglementaires.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés de lovastatine, qui comprennent la déhydro lovastatine, le sel d'ammonium de l'hydroxyacide de lovastatine et le composé n° 6 apparenté à la lovastatine. Nos étalons d'impuretés de lovastatine disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. De plus, nous pouvons synthétiser des étalons d’impuretés et des produits de dégradation inconnus de la lovastatine. Chaque livraison bénéficie d’un rapport de caractérisation complet, garantissant qualité et transparence.
Bibliographie
FAQ
Bibliographie
- Patchett, Arthur A. ; Kuo, Chan Hwa, Produits d'hydrogénation de mévinoline et de dihydromévinoline, procédé de préparation de ceux-ci et composition pharmaceutique antihypercholestérolémique les contenant, Merck and Co., Inc., États-Unis, EP33537B1, 29 mai 1985
- Houck, Antoine ; Thomas, Scott ; Ellison, Dean K., Détermination par chromatographie liquide des impuretés connues de faible niveau dans le médicament en vrac à base de lovastatine : une application de la chromatographie haute-basse, Talanta, Volume : 40, Numéro : 4, Pages : 491-4, 1993
Foire aux Questions
Comment les impuretés de la lovastatine sont-elles surveillées lors des tests de stabilité ?
Les tests de stabilité de la lovastatine consistent à soumettre le produit médicamenteux à diverses conditions pour évaluer son profil d'impuretés au fil du temps. Il garantit que les niveaux d'impuretés restent dans des limites acceptables tout au long de la durée de conservation du produit.
Quel est le rôle des études de validation dans le contrôle des impuretés de la lovastatine ?
Des études de validation sont menées pour garantir que les méthodes analytiques utilisées pour l'analyse des impuretés dans la Lovastatine sont exactes, précises et fiables, permettant un contrôle efficace des impuretés pendant la fabrication.
Quel solvant aide à analyser les impuretés de la lovastatine ?
Le méthanol est le solvant utilisé lors de l’analyse de nombreuses impuretés de la Lovastatine.
Quelle est la température de stockage recommandée pour les impuretés de la Lovastatine ?
Les impuretés de la lovastatine doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.