Linézolide
Renseignements généraux
Impuretés du linézolide et linézolide
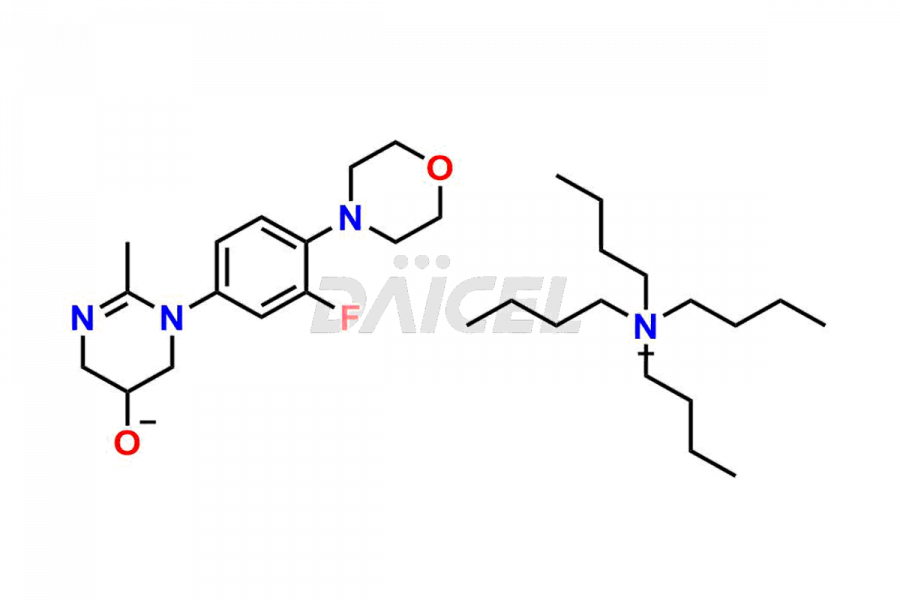
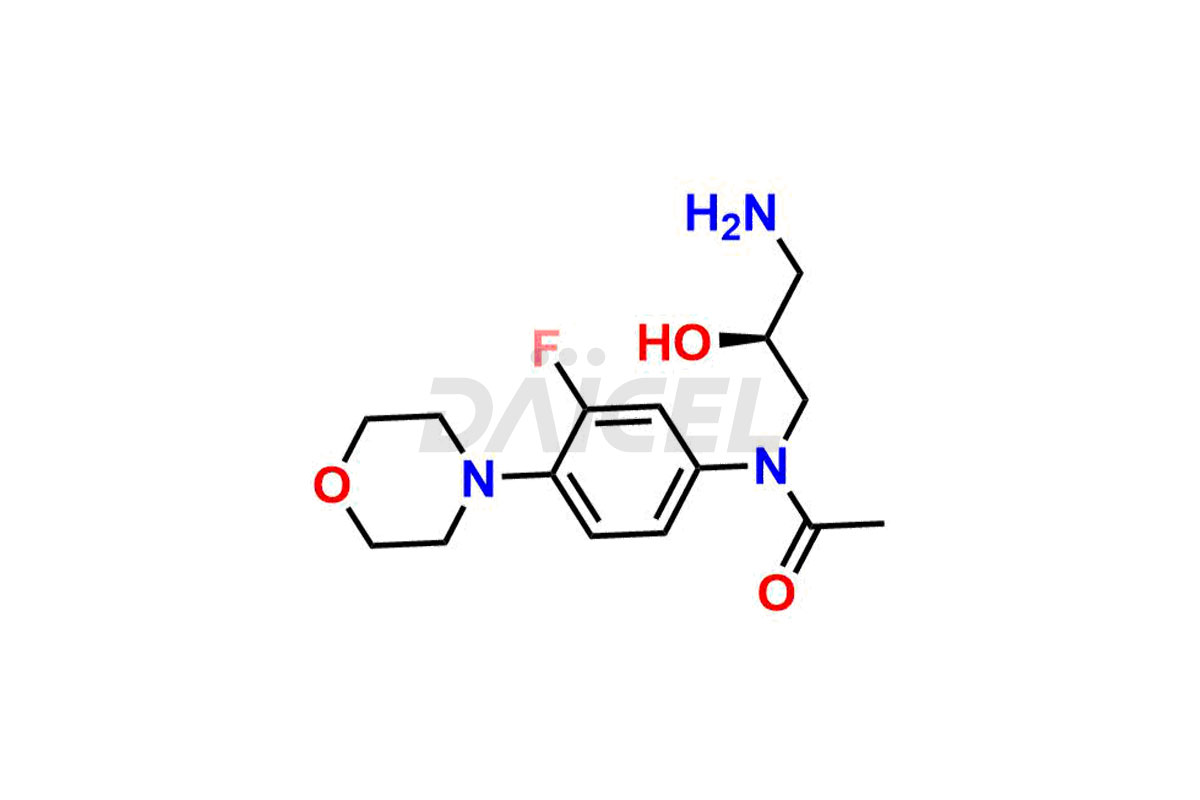
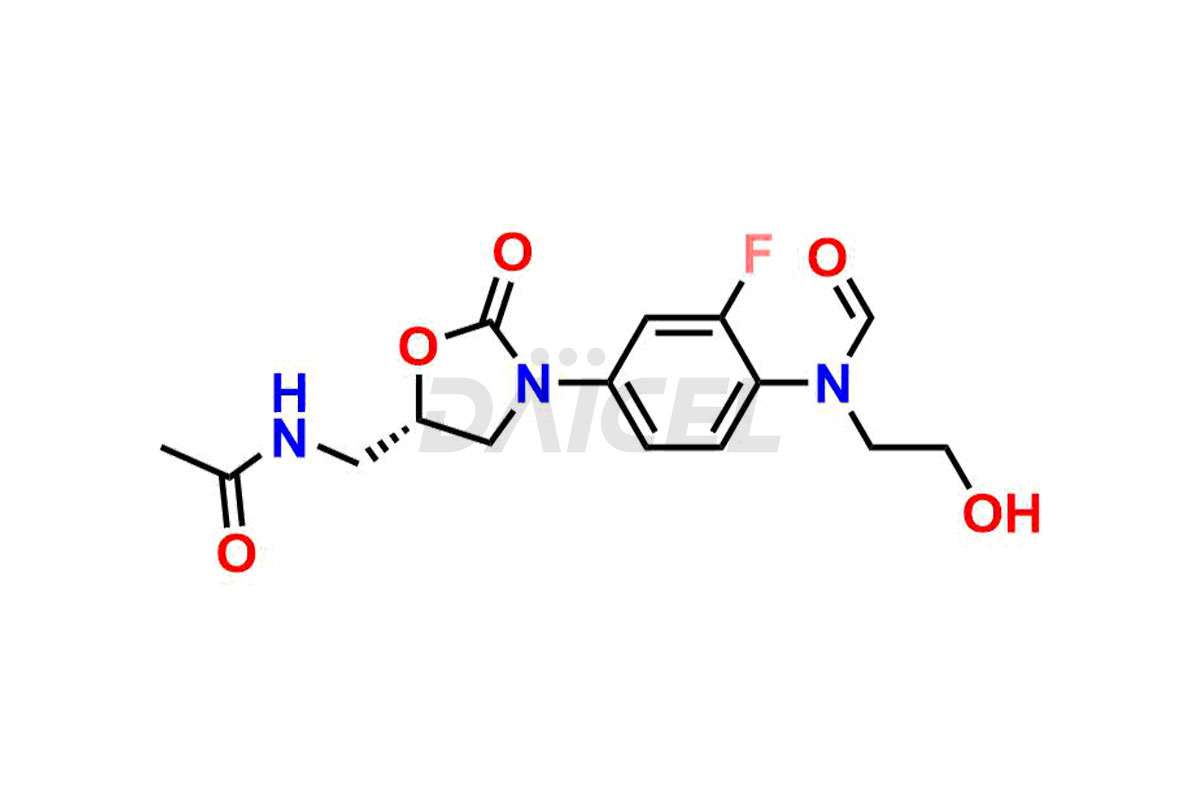
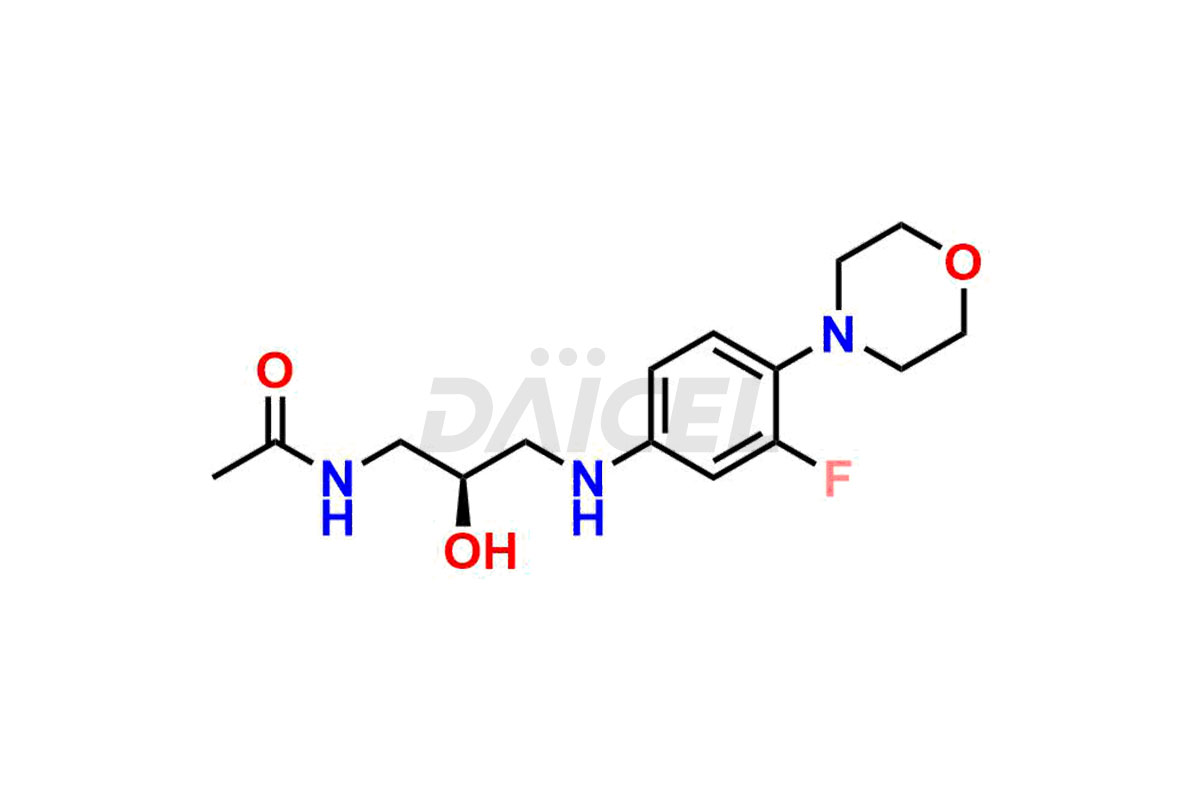
Pour évaluer la pureté et l'innocuité du linézolide, un ingrédient pharmaceutique actif essentiel, Daicel Pharma propose une synthèse personnalisée des standards d’impuretés du linézolide. Ces normes d'impuretés comprennent des composés cruciaux tels que le 1-(3-fluoro-4-morpholinophényl)-2-méthyl-1,4,5,6-tétrahydropyrimidin-5-ol, le désacétyl-N, le O-descarbonyl linézolide, l'impureté linézolide - D, impureté de linézolide -F, impureté de linézolide E, isomère R du linézolide, composé apparenté au linézolide C et composé apparenté au linézolide D. De plus, Daicel Pharma propose des options de livraison mondiales pour les étalons d'impuretés du linézolide.
Linézolide [CAS : 165800-03-3] est un dérivé synthétique de l'oxazolidinone qui agit comme un agent antibactérien en inhibant une étape précoce de la synthèse des protéines bactériennes. Il affecte également la tension artérielle en inhibant la monoamine oxydase. Ce médicament traite les infections de la peau et des voies respiratoires causées par des bactéries à Gram positif.
Linézolide : utilisation et disponibilité commerciale
Zyvox est le nom de marque sous lequel le médicament Linezolid est disponible. Il s’agit d’un médicament antimicrobien synthétique à base d’oxazolidinone. Le linézolide traite les infections à Gram positif, notamment la pneumonie bactérienne, les infections de la peau et des structures cutanées et les infections à entérocoques résistants à la vancomycine (ERV).
Structure du linézolide et mécanisme d’action
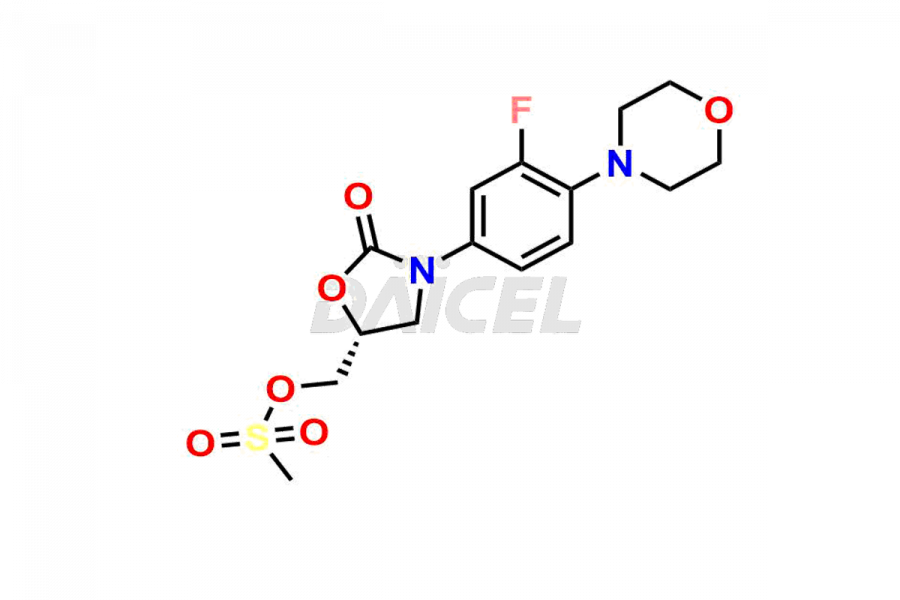
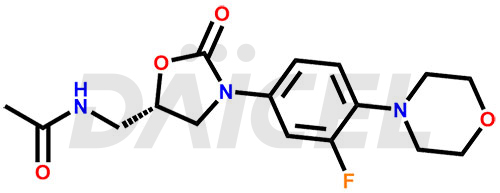
Le nom chimique du linézolide est N-[[(5S)-3-[3-Fluoro-4-(4-morpholinyl)phényl]-2-oxo-5-oxazolidinyl]méthyl]acétamide. Sa formule chimique est C16H20FN3O4, et son poids moléculaire est d'environ 337.35 g/mol.
Le linézolide inhibe la synthèse des protéines bactériennes en empêchant la formation d'un complexe d'initiation fonctionnel 70S qui provoque le processus de traduction bactérienne.
Impuretés et synthèse du linézolide
Les impuretés contenues dans le linézolide sont des substances indésirables qui peuvent être présentes dans le produit médicamenteux contenant l'ingrédient pharmaceutique actif (API). Ils peuvent provenir de la fabrication1,2, les matières premières ou les interactions avec des facteurs environnementaux. Les impuretés courantes du linézolide comprennent les substances apparentées, les produits de dégradation, les solvants résiduels et les impuretés liées au processus. Il est essentiel de surveiller et de contrôler les niveaux d’impuretés pour garantir la sécurité, l’efficacité et la qualité du produit médicamenteux Linezolid. Les autorités réglementaires ont fixé des lignes directrices et des limites spécifiques pour les niveaux d'impuretés afin de maintenir la pureté et de minimiser les risques potentiels associés au médicament. Des mesures de contrôle de qualité strictes tout au long de la fabrication minimisent les niveaux d'impuretés et garantissent l'intégrité du produit.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés de linézolide, qui comprennent le 1-(3-fluoro-4-morpholinophényl)-2-méthyl-1,4,5,6-tétrahydropyrimidin-5- ol, désacétyl-N, O-descarbonyl linézolide, impureté linézolide -D, impureté linézolide -F, impureté linézolide E, isomère R linézolide, composé apparenté au linézolide C et composé apparenté au linézolide D. Nos normes d'impuretés linézolides ont un certificat détaillé de Analyse (CoA) qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.3. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. De plus, nous pouvons synthétiser des étalons d’impuretés et des produits de dégradation inconnus du linézolide. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Barbachyn, Michael R. ; Brickner, Steven J. ; Hutchinson, Douglas K., Substituted Oxazine And Thiazine Oxazolidinone Antimicrobiens, Upjohn Co., États-Unis, EP717738B1, 20 octobre 1999
- Brickner, Steven J. ; Hutchinson, Douglas K. ; Barbachyn, Michael R. ; Manninen, Peter R. ; Ulanowicz, Debra A. ; Garmon, Stuart A. ; Grega, Kevin C. ; Hendges, Susan K. ; Toops, Dana S, Synthèse et activité antibactérienne de l'U-100592 et de l'U-100766, Deux agents antibactériens oxazolidinone pour le traitement potentiel des infections bactériennes à Gram positif multirésistantes, Journal of Medicinal Chemistry, Volume : 39, Numéro : 3, Pages : 673-9, 1996
- Peng, Geoffrey W. ; Stryd, Ronald P. ; Murata, Shoiji ; Igarashi, Mayumi; Chiba, Koji ; Aoyama, Hiroyuki ; Aoyama, Makiko ; Zenki, Tomoko; Ozawa, Naoki, Détermination du linézolide dans le plasma par chromatographie liquide haute performance en phase inversée, Journal of Pharmaceutical and Biomedical Analysis, Volume : 20, Numéro : 1-2, Pages : 65-73, 1999
Foire aux Questions
Les impuretés du linézolide peuvent-elles varier d'un lot à l'autre ?
Oui, la présence et les niveaux d'impuretés dans le linézolide peuvent varier d'un lot à l'autre en raison des variations du processus, des matières premières et d'autres facteurs. Cependant, les fabricants visent à maintenir une qualité constante et à minimiser les niveaux d'impuretés dans des limites acceptables.
Existe-t-il des méthodes spécifiques utilisées pour détecter et quantifier les impuretés du linézolide ?
Oui, des méthodes analytiques telles que la chromatographie liquide haute performance (HPLC) et la spectrométrie de masse (MS) sont couramment utilisées pour détecter et quantifier les impuretés du linézolide. Ces méthodes permettent une évaluation et un contrôle précis des niveaux d’impuretés.
Quel solvant aide à analyser les impuretés du linézolide ?
Le méthanol est un solvant utilisé lors de l’analyse de nombreuses impuretés du linézolide.
Quelle est la température de stockage recommandée pour les impuretés du linézolide ?
Les impuretés du linézolide doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.