Charger plus
Vous avez vu 9 sur 11 articles
Pour évaluer la pureté et l'innocuité de la linagliptine, un ingrédient pharmaceutique actif essentiel, Daicel Pharma propose une synthèse personnalisée des standards d’impuretés Linagliptine. Ces normes d'impuretés comprennent des composés cruciaux tels que la 8-bromo-3-méthyl-7-(2-butynyl)-xanthine, l'impureté E de linagliptine, le méthyldimère de linagliptine, l'impureté de linagliptine N-glucose, la STD interne de l'impureté de linagliptine nitroso, l'isomère S de linagliptine, N-acétyl linagliptine, N-Boc linagliptine, N-carbamoyl linagliptine et N-formyl linagliptine. De plus, Daicel Pharma propose des options de livraison mondiales pour les étalons d'impuretés de linagliptine.
La linagliptine [CAS : 668270/12/0], un puissant inhibiteur de la dipeptidyl peptidase 4 (DPP-4) à base de dihydropurinedione, est biodisponible par voie orale et présente une activité hypoglycémique. Il traite le diabète de type 2 en association avec un régime alimentaire et de l'exercice, seuls ou avec d'autres agents hypoglycémiants oraux.
La linagliptine, commercialisée sous Tradjenta, traite le diabète sucré de type 2 pour améliorer le contrôle glycémique chez les adultes. Il agit en monothérapie chez les patients insuffisamment contrôlés par le régime alimentaire et l'exercice physique seuls et pour lesquels la metformine est inadaptée ou contre-indiquée en raison d'une insuffisance rénale.
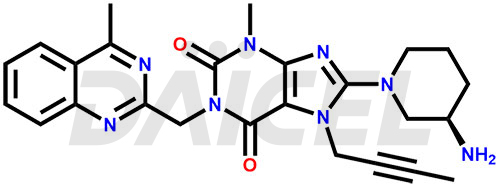
Le nom chimique de la linagliptine est 8-[(3R)-3-Amino-1-pipéridinyl]-7-(2-butyn-1-yl)-3,7-dihydro-3-méthyl-1-[(4- méthyl-2-quinazolinyl)méthyl]-1H-purine-2,6-dione. Sa formule chimique est C25H28N8O2, et son poids moléculaire est d'environ 472.5 g/mol.
La linagliptine dégrade l'hormone incrétine, le peptide-1 de type glucagon (GLP-1). Il stimule la libération d'insuline de manière glucose-dépendante et diminue les niveaux de glucagon dans la circulation.
Les impuretés de Linagliptine font référence à des substances inattendues qui peuvent être présentes dans les formulations de Linagliptine. Ils peuvent provenir de la fabrication1, les matières premières ou les conditions de stockage. Leur présence peut potentiellement affecter sa pureté, sa puissance et sa qualité globale. Des mesures rigoureuses de contrôle de qualité par les fabricants de produits pharmaceutiques contribuent à garantir la sécurité et l’efficacité des médicaments. Ces mesures comprennent des tests et des analyses approfondis pour identifier et quantifier les impuretés et le strict respect des directives et normes réglementaires. En contrôlant les niveaux d'impuretés dans des limites acceptables, les sociétés pharmaceutiques s'efforcent de fournir aux patients des formulations de linagliptine de haute qualité pour traiter le diabète sucré de type 2, minimisant ainsi les risques potentiels associés aux impuretés.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés de linagliptine, qui comprennent la 8-bromo-3-méthyl-7-(2-butynyl)-xanthine, l'impureté E de linagliptine, le méthyldimère de linagliptine et l'impureté de linagliptine N-glucose. , MST interne de l'impureté Linagliptine Nitroso, Linagliptine S-isomère, N-Acétyl Linagliptine, N-Boc Linagliptine, N-Carbamoyl Linagliptine et N-Formyl Linagliptine. Nos étalons d'impuretés de linagliptine disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. De plus, nous pouvons synthétiser des étalons d’impuretés et des produits de dégradation inconnus de la linagliptine. Chaque livraison dispose d'un rapport de caractérisation complet.
Les directives réglementaires décrivent la documentation et la déclaration nécessaires des impuretés de Linagliptine pour garantir la transparence et la responsabilité.
Les tests de génotoxicité sont généralement effectués pour évaluer le potentiel des impuretés de la linagliptine à causer des dommages ou des mutations à l'ADN.
Des processus de fabrication inappropriés, tels qu'une mauvaise manipulation ou une contamination, peuvent contribuer à la formation d'impuretés dans la linagliptine.
Les impuretés de la linagliptine doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.