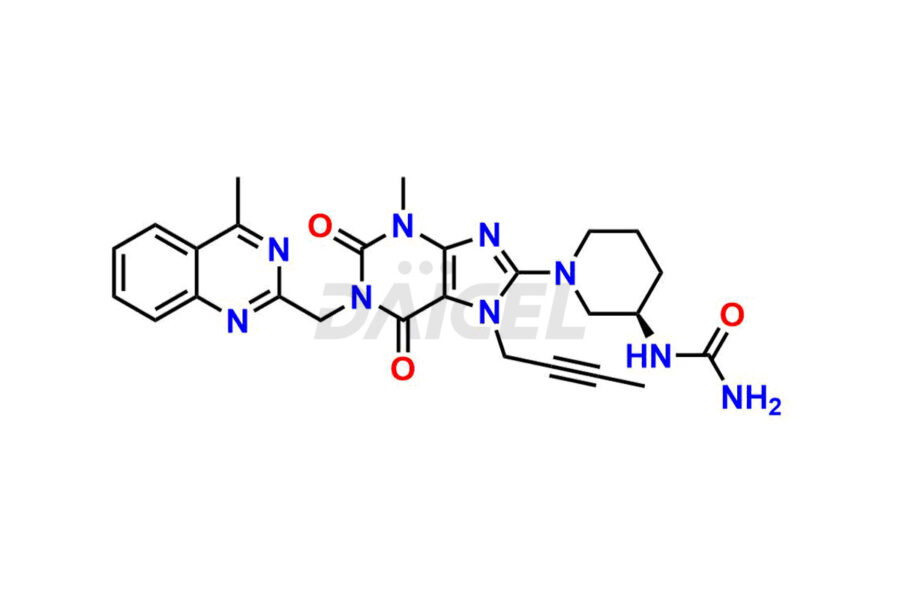
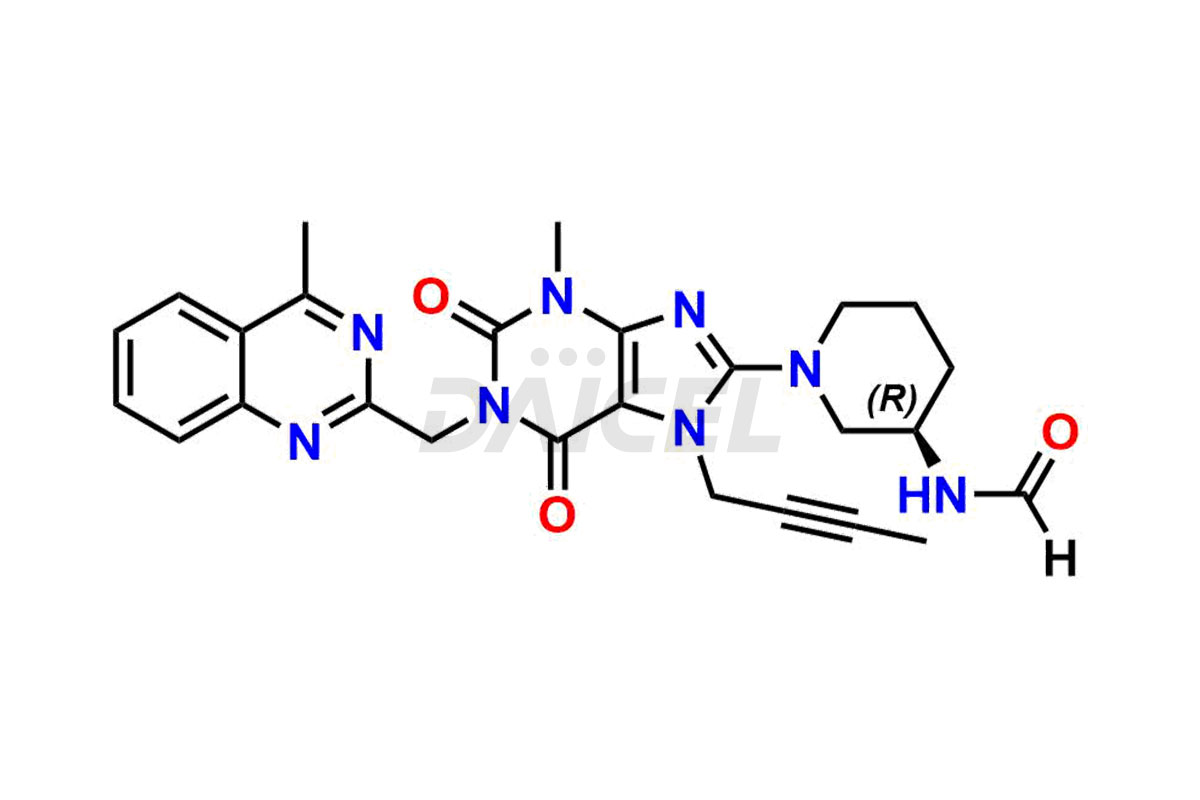
La linagliptine
Bibliographie
- Himmelsbach, Frank ; Langkopf, Elke ; Eckhardt, Matthias ; Marc, Michael ; Maier, Roland ; Lotz, Ralf Richard Hermann ; Tadayyon, Mohammad,8-[3-amino-pipéridin-1-yl]-xanthines, leur préparation et leur utilisation comme compositions pharmaceutiques, Boehringer Ingelheim Pharma GmbH & Co. K.-G., Allemagne, US7407955B2, 5 août 2008. XNUMX
- El-Bagary, Ramzia Ismail ; Elkady, Ehab Farouk ; Ayoub, Bassam Mahfouz, Détermination spectrofluorométrique de la linagliptine en vrac et sous forme pharmaceutique, European Journal of Chemistry, Volume : 5, Numéro : 2, Pages : 380-382, 3 pp., 2014
Foire aux Questions
Existe-t-il des directives ou des exigences spécifiques pour signaler les impuretés de la linagliptine ?
Les directives réglementaires décrivent la documentation et la déclaration nécessaires des impuretés de Linagliptine pour garantir la transparence et la responsabilité.
Les impuretés de la linagliptine sont-elles testées pour leur potentiel génotoxique ?
Les tests de génotoxicité sont généralement effectués pour évaluer le potentiel des impuretés de la linagliptine à causer des dommages ou des mutations à l'ADN.
Les impuretés de la linagliptine peuvent-elles résulter de processus de fabrication inadéquats ?
Des processus de fabrication inappropriés, tels qu'une mauvaise manipulation ou une contamination, peuvent contribuer à la formation d'impuretés dans la linagliptine.
Quelle est la température de stockage recommandée pour les impuretés de la linagliptine ?
Les impuretés de la linagliptine doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.