herbe de vie
Renseignements généraux
Impuretés du Lifitegrast et Lifitegrast
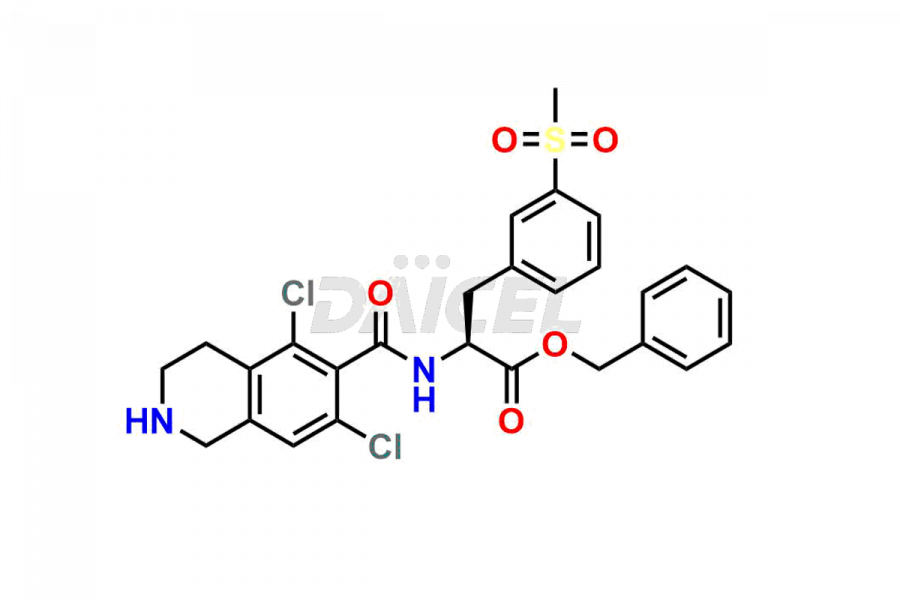
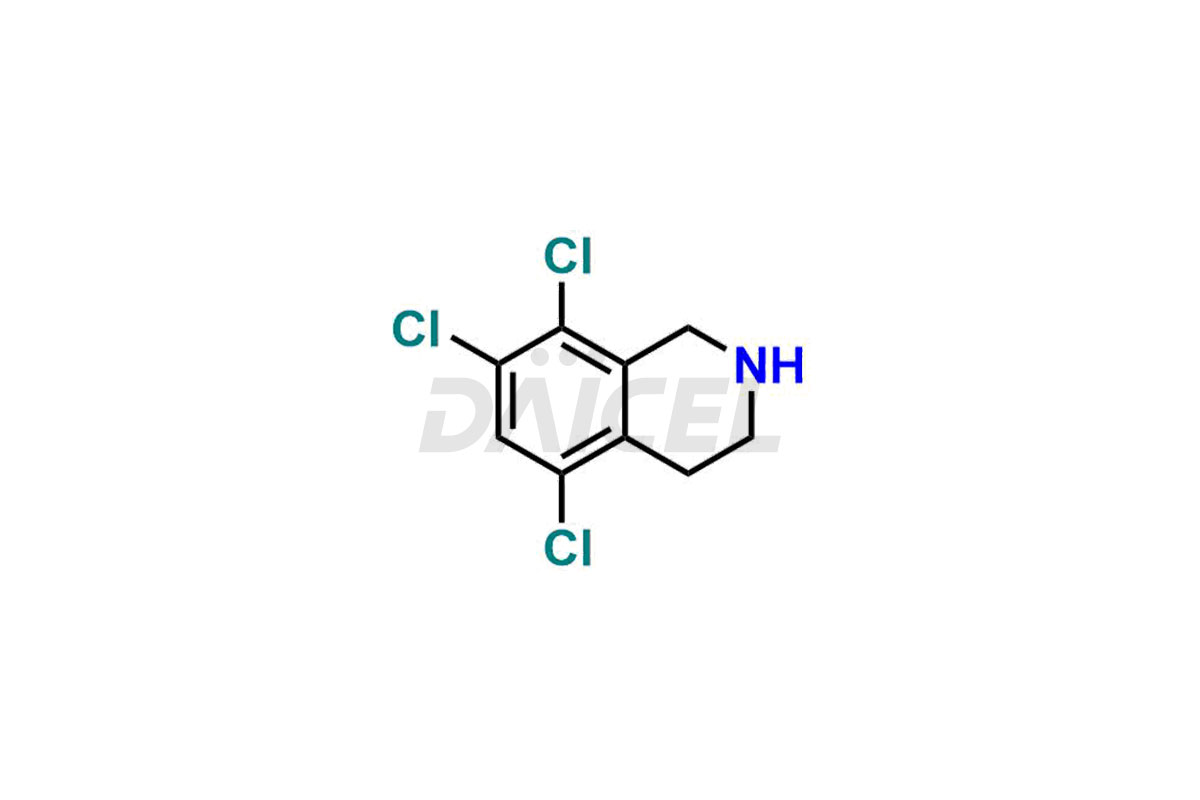
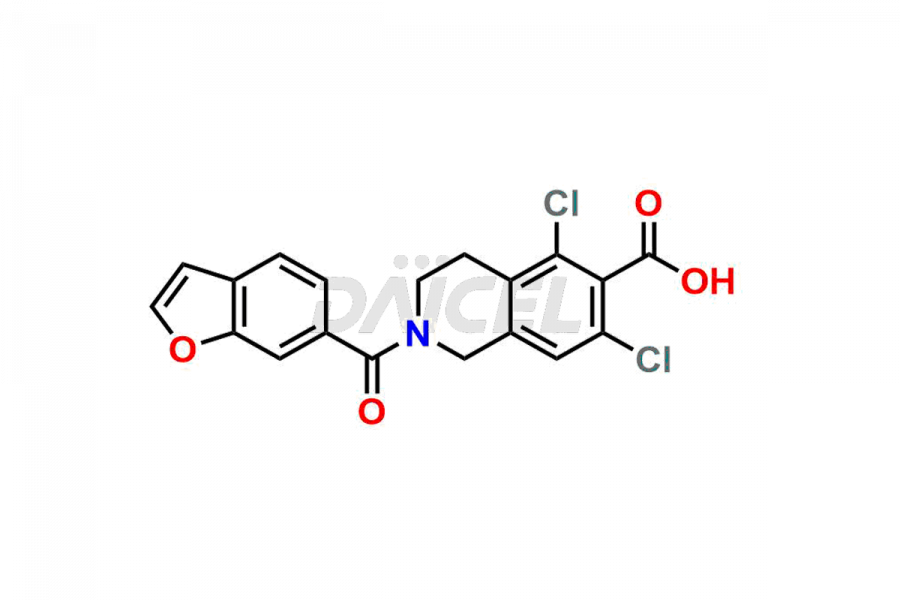
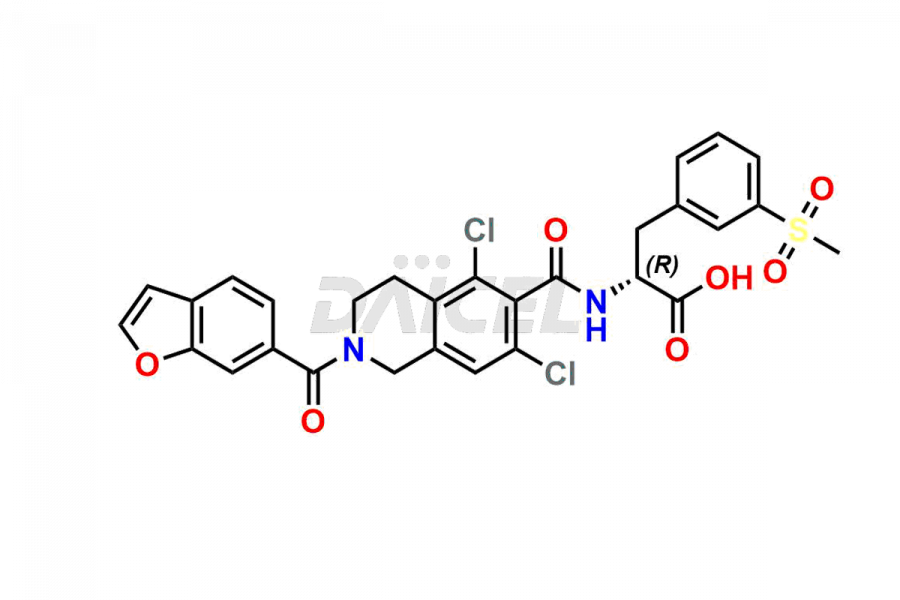
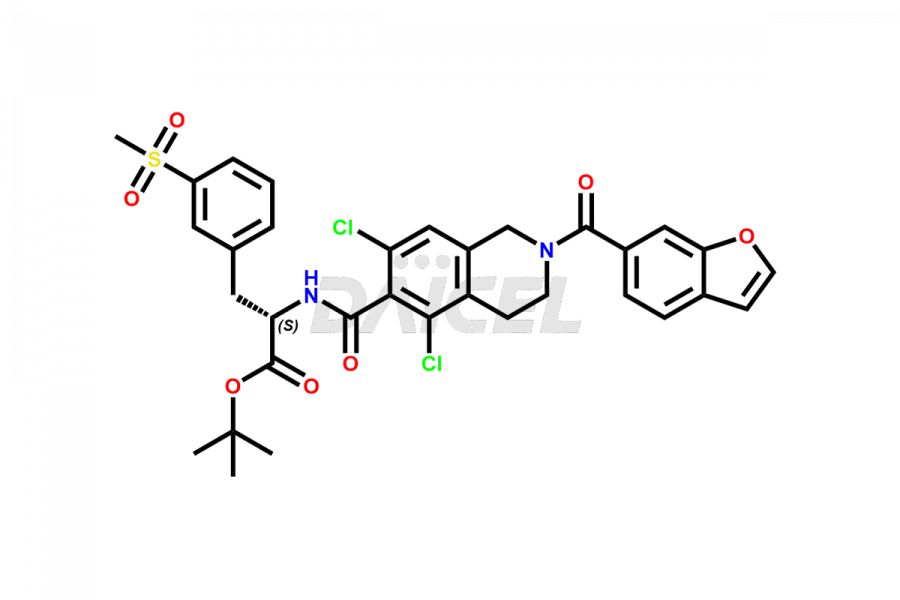
Pour la pureté et la sécurité du Lifitegrast, un ingrédient pharmaceutique actif, Daicel Pharma propose une synthèse personnalisée des normes d'impuretés Lifitegrast. Ces normes d'impuretés comprennent des composés cruciaux tels que le (S)-benzyl 2-(5,7-dichloro-1,2,3,4-tetrahydroisoquinoline-6-carboxamido)-3 -(3-(méthylsulfonyl)phényl)propanoate, 5,7,8 ,1,2,3,4-trichloro-1-tétrahydroisoquinoléine, impureté Lifitegrast 3, impureté Lifitegrast 5, impureté Lifitegrast XNUMX, isomère R Lifitegrast et impureté ester tert-butylique Lifitegrast. De plus, Daicel Pharma propose des options de livraison mondiales pour les étalons d'impuretés Lifitegrast.
herbe de vie [CAS : 1025967-78-5] est un médicament anti-inflammatoire et un antagoniste de l'antigène 1 associé à la fonction lymphocytaire pour le traitement de la kératoconjonctivite sèche, également connue sous le nom de syndrome de l'œil sec.
Lifitegrast : utilisation et disponibilité commerciale
Le lifitegrast, commercialisé sous le nom de Xiidra, est un agent anti-inflammatoire topique approuvé par la FDA américaine pour traiter le syndrome de l'œil sec. Il agit comme un antagoniste de l’antigène 1 associé à la fonction des petits lymphocytes (LFA-1), réduisant l’inflammation et gérant les symptômes de sécheresse oculaire. Le lifitegrast est administré sous forme d'une goutte d'une solution ophtalmique à 5 % et utilisé pour les larmes artificielles.
Structure et mécanisme d'action du Lifitegrast
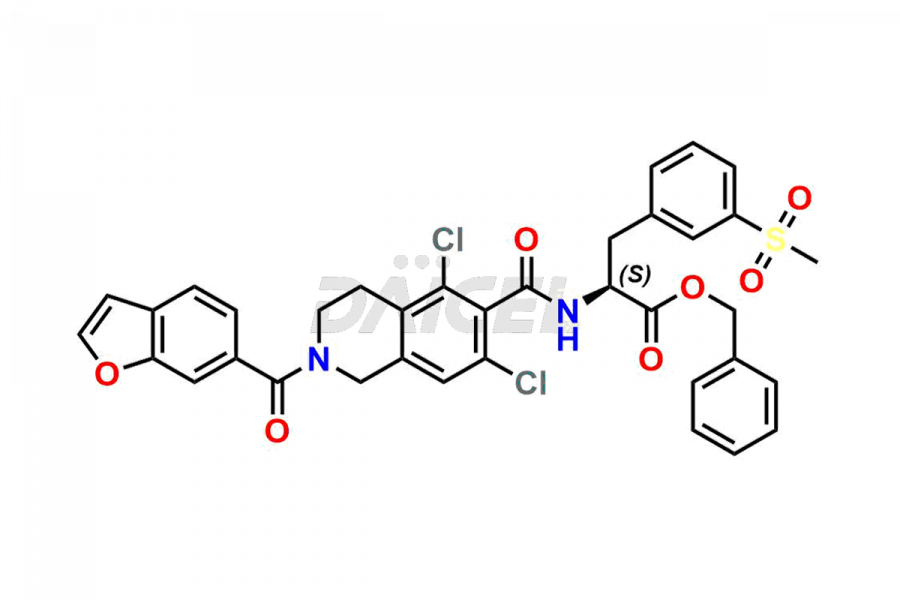
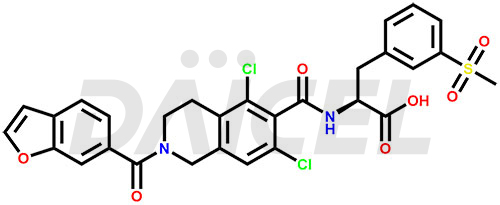
Le nom chimique du Lifitegrast est N-[[2-(6-Benzofuranylcarbonyl)-5,7-dichloro-1,2,3,4-tetrahydro-6-isoquinolinyl]carbonyl]-3-(méthylsulfonyl)-L-phénylalanine. . Sa formule chimique est C29H24Cl2N2O7S, et son poids moléculaire est d'environ 615.5 g/mol.
Le lifitegrast bloque l'interaction de l'antigène 1 associé à la fonction lymphocytaire (LFA-1) avec sa molécule d'adhésion intercellulaire de ligand apparenté 1 (ICAM-1).
Impuretés et synthèse du Lifitegrast
Les impuretés du Lifitegrast sont des substances involontaires qui peuvent être présentes dans les formulations du Lifitegrast. Ils peuvent survenir lors de la synthèse du médicament1, le stockage ou le transport. Il est essentiel de surveiller et de contrôler de près les niveaux d’impuretés du Lifitegrast pour garantir sa sécurité, son efficacité et sa qualité. Les fabricants de produits pharmaceutiques emploient des mesures de contrôle de qualité rigoureuses pour minimiser les niveaux d'impuretés et maintenir la pureté du Lifitegrast. En adhérant à des directives et des normes réglementaires strictes, les entreprises s'efforcent de fournir aux patients des formulations de Lifitegrast fiables et efficaces pour traiter le syndrome de l'œil sec. Une surveillance et des tests continus permettent de garantir que les impuretés sont maintenues à des niveaux acceptables, préservant ainsi leur intégrité tout au long de leur durée de conservation.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour préparer des étalons d'impuretés de Lifitegrast, qui comprennent le (S)-benzyl 2-(5,7-dichloro-1,2,3,4-tétrahydroisoquinoline-6-carboxamido)-3 -(3-(méthylsulfonyl)phényl)propanoate, 5,7,8-trichloro-1,2,3,4-tétrahydroisoquinoline, impureté 1 de Lifitegrast, impureté 3 de Lifitegrast, impureté 5 de Lifitegrast, isomère R de Lifitegrast et tert-butyle de Lifitegrast impureté ester. Nos étalons d'impuretés Lifitegrast disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. De plus, nous pouvons synthétiser des étalons d’impuretés et des produits de dégradation inconnus du Lifitegrast. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Gadek, Thomas ; Burnier, John, Compositions et méthodes de traitement des troubles oculaires, Sarcode, États-Unis, EP1881823B1, 3 décembre 2014
- Kumar, Ajay ; Chalannavar, Raju Krishna, Caractérisation des produits de dégradation du lifitegrast par spectrométrie de masse : développement et validation d'une méthode HPLC en phase inversée indicatrice de stabilité, Analytical Chemistry Letters, Volume : 12, Numéro : 6, Pages : 730-744, 2022
Foire aux Questions
Les profils d'impuretés dans le Lifitegrast varient-ils entre les différents lots ?
Bien que les fabricants s'efforcent de maintenir des profils d'impuretés cohérents, des variations mineures des niveaux d'impuretés peuvent se produire entre les lots de Lifitegrast.
Les impuretés du Lifitegrast peuvent-elles avoir un impact sur la biodisponibilité du médicament ?
Certaines impuretés peuvent interférer avec l'absorption, la distribution ou le métabolisme du Lifitegrast, affectant potentiellement sa biodisponibilité et ses effets thérapeutiques.
Existe-t-il des impuretés du Lifitegrast pouvant résulter de la dégradation des excipients ?
La dégradation des excipients utilisés dans Lifitegrast peut conduire à la formation d'impuretés, qui doivent être soigneusement contrôlées et surveillées.
Quelle est la température de stockage recommandée pour les impuretés du Lifitegrast ?
Les impuretés du lifitegrast doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.