Charger plus
Vous avez vu 9 sur 28 articles
Pour la pureté et la sécurité de la Lévothyroxine, un ingrédient pharmaceutique actif, Daicel Pharma propose une synthèse personnalisée des standards d’impuretés de la lévothyroxine. Ces normes d'impuretés comprennent des composés cruciaux tels que l'acide 3,3′,5-triiodothyroacétique, la 3-Diiodo-L-thyronine, la 5-diiodo-L-tyrosine, l'impureté F de la lévothyroxine, l'impureté de la lévothyroxine-J, la lévothyroxine-N. -Lactoside, T3,5-Aldéhyde (Impurité-I) et plus encore. De plus, Daicel Pharma propose des options de livraison mondiales pour les étalons d'impuretés de lévothyroxine.
La lévothyroxine [CAS : 51-48-9] est une version synthétique de la thyroxine, qui fonctionne comme une hormone thyroïdienne et un médicament antithyroïdien. La triiodothyronine (T3) exerce une gamme de stimulations métaboliques sur les cellules. La lévothyroxine, qui ressemble chimiquement à l'hormone thyroïdienne naturelle, imite ses fonctions et neutralise les affections liées à la thyroïde.
La lévothyroxine, disponible sous des marques telles que Euthyrox, Levo-T, Synthroid, Levolet, Levoxyl, Thyquidity, Thyro-Tabs, Tirosint, Tirosint-Sol, Unithroid, etc., est un médicament oral principalement utilisé pour traiter diverses formes d'hypothyroïdie. De plus, la lévothyroxine a reçu l'approbation de la FDA américaine pour supprimer la thyrotropine hypophysaire en tant que traitement d'appoint du cancer de la thyroïde bien différencié dépendant de la thyrotropine.
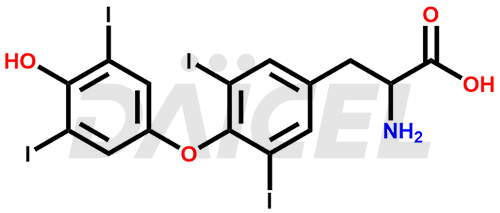
Le nom chimique de la lévothyroxine est O-(4-Hydroxy-3,5-diiodophényl)-3,5-diiodo-L-tyrosine. Sa formule chimique est C15H11I4NON4, et son poids moléculaire est d'environ 776.87 g/mol.
La lévothyroxine influence directement la transcription de l'ADN pour augmenter le métabolisme corporel en augmentant la gluconéogenèse, la synthèse des protéines, la mobilisation des réserves de glycogène et d'autres fonctions.
Les impuretés de lévothyroxine font référence à des substances involontaires qui peuvent être présentes dans les formulations de lévothyroxine. Ils peuvent survenir pendant le processus de fabrication1 ou le stockage du médicament. Il est crucial de surveiller et de contrôler les niveaux d'impuretés dans la lévothyroxine, car ils peuvent affecter la pureté, la puissance et la sécurité du médicament. Des mesures strictes de contrôle de qualité aident à minimiser les niveaux d'impuretés et à garantir la fiabilité et l'efficacité de la lévothyroxine pour le traitement de l'hypothyroïdie. En maintenant des normes strictes, les fabricants de produits pharmaceutiques s'efforcent de fournir aux patients des formulations de lévothyroxine de haute qualité qui répondent aux exigences réglementaires et offrent les bénéfices thérapeutiques escomptés.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés de lévothyroxine, qui comprennent l'acide 3,3′,5-Triiodothyroacetic, 3, 5-Diiodo-L-thyronine, 3,5-diiodo-L- tyrosine, impureté F de lévothyroxine, impureté-J de lévothyroxine, lévothyroxine-N-lactoside, aldéhyde T4 (impureté-I), et plus encore. De plus, nous proposons des étalons de lévothyroxine marqués au deutérium comme la Lévothyroxine-D3, qui est essentielle pour mener des recherches bioanalytiques et des études BA/BE. Nos étalons d'impuretés de lévothyroxine disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. De plus, nous pouvons synthétiser des normes d'impuretés inconnues de la lévothyroxine, des produits de dégradation et des composés marqués pour évaluer l'efficacité de la lévothyroxine générique. Chaque livraison dispose d'un rapport de caractérisation complet.
Des niveaux plus élevés d'impuretés dans la lévothyroxine peuvent avoir un impact sur sa réponse thérapeutique, son efficacité ou sa cohérence, nécessitant des mesures de contrôle strictes lors de la fabrication.
Certaines impuretés de la lévothyroxine peuvent subir des transformations chimiques ou une dégradation pendant le stockage, ce qui peut affecter la pureté et la stabilité globales du médicament.
Certaines impuretés peuvent interférer avec la pharmacocinétique ou la pharmacodynamique de la lévothyroxine, affectant potentiellement ses interactions avec d'autres médicaments.
Les impuretés de lévothyroxine doivent être conservées à une température ambiante contrôlée, généralement entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.