Charger plus
Vous avez vu 9 sur 27 articles
Daicel Pharma propose des options de livraison dans le monde entier pour la synthèse personnalisée d'étalons d'impuretés du lenvatinib, y compris des étalons d'impuretés cruciaux tels que le 2,4-dichloro-7-méthoxyquinoline-6-carboxamide, le 3,4-dichloro-7-méthoxyquinoline-6-carboxamide, le 4-( 4-amino-3-hydroxyphénoxy)-7-méthoxyquinoline-6-carboxamide, 4-Amino-2,3,5-Trichlorophénol, impureté chloro Lenvatinib, impureté Lenvatinib-10 et plus. Ces normes d'impuretés jouent un rôle essentiel dans l'évaluation de la pureté et de la sécurité du Lenvatinib, un ingrédient pharmaceutique actif.
Lénvatinib [CAS : 417716/92/8] est un inhibiteur des récepteurs de la tyrosine kinase et un agent antinéoplasique disponible par voie orale. Il traite le carcinome rénal réfractaire et le cancer médullaire avancé et métastatique de la thyroïde.
Le lenvatinib traite le carcinome hépatocellulaire (CHC) non résécable ou avancé, le cancer de la thyroïde différencié réfractaire à l'iode radioactif (DTC) et le carcinome rénal avancé (CCR). Commercialisé sous la marque Lenvima, il s’agit d’un inhibiteur de la tyrosine kinase à récepteurs multiples qui inhibe efficacement les récepteurs du VEGF, conduisant à de puissants effets antiangiogéniques. De plus, le lenvatinib bloque le FGFR, le RET, le PDGFRa et le KIT, provoquant ainsi la suppression de la prolifération des cellules malignes.
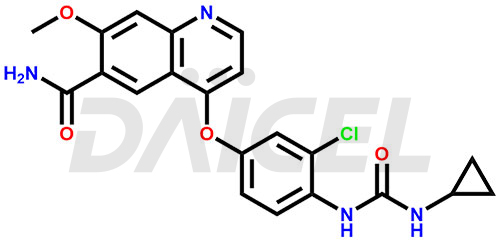
Le nom chimique du lenvatinib est 4-[3-Chloro-4-[[(cyclopropylamino)carbonyl]amino]phénoxy]-7-méthoxy-6-quinolinecarboxamide. Sa formule chimique est C21H19CIN4O4, et son poids moléculaire est d'environ 426.9 g/mol.
Le lenvatinib bloque les activités kinases des récepteurs du facteur de croissance endothélial vasculaire (VEGF) et des récepteurs du facteur de croissance des fibroblastes (FGF), FGFR1, 2, 3 et 4.
Pendant la fabrication1 du Lenvatinib, des impuretés peuvent se former sous forme de sous-produits ou de produits de dégradation. Ils peuvent provenir des matières premières, des intermédiaires ou des conditions de réaction. Il est crucial d’identifier, de caractériser et de contrôler ces impuretés pour garantir la sécurité et l’efficacité du médicament. Des techniques analytiques telles que la chromatographie liquide haute performance (HPLC) et la spectrométrie de masse (MS) permettent de détecter et de quantifier les impuretés. Des mesures strictes de contrôle de qualité garantissent que les niveaux d'impuretés restent dans des limites acceptables, maintenant ainsi la pureté et la qualité du Lenvatinib.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour préparer les étalons d'impuretés du lenvatinib. Nous proposons une gamme d'étalons d'impuretés pour le lenvatinib, tels que le 2,4-dichloro-7-méthoxyquinoline-6-carboxamide, le 3,4-dichloro-7-méthoxyquinoline-6-carboxamide, le 4-(4-amino-3-hydroxyphénoxy) -7-méthoxyquinoline-6-carboxamide, 4-Amino-2,3,5-Trichlorophénol, impureté chloro Lenvatinib, impureté Lenvatinib-10 et plus. Nos étalons d'impuretés disposent d'un certificat d'analyse (CoA) détaillé et d'un rapport de caractérisation complet. Le CoA englobe les données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Des données supplémentaires, telles que 13C-DEPT, peuvent être fournies sur demande. Nous pouvons synthétiser des étalons d’impuretés ou des produits de dégradation inconnus du Lenvatinib. Chaque livraison dispose d'un rapport de caractérisation complet.
Des impuretés contenues dans le lenvatinib peuvent se former pendant le processus de fabrication, les conditions de stockage ou en raison d'interactions avec d'autres composants. Des facteurs tels que la température, le pH et l'exposition à la lumière peuvent contribuer à la formation d'impuretés.
Les autorités réglementaires, telles que la Pharmacopée américaine (USP) ou le Conseil international pour l'harmonisation (ICH), fournissent des lignes directrices sur les limites acceptables d'impuretés contenues dans le lenvatinib afin de garantir sa sécurité et sa qualité.
Les impuretés contenues dans le lenvatinib peuvent potentiellement avoir un impact sur son efficacité ou sa sécurité. Certains peuvent avoir des effets toxiques ou altérer les propriétés thérapeutiques du médicament, ce qui rend crucial leur contrôle dans des limites acceptables.
Il est recommandé de conserver les impuretés du lenvatinib à une température ambiante contrôlée, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.