Charger plus
Vous avez vu 9 sur 20 articles
Daicel Pharma propose des options de livraison dans le monde entier pour la synthèse personnalisée d'étalons d'impuretés de lénalidomide, y compris des étalons d'impuretés cruciaux tels que le 4-nitrophthalide (impureté lactone de lénalidomide KSM), l'impureté de lénalidomide Amadori, l'impureté de lénalidomide-3, l'impureté Amadori à chaîne ouverte de lénalidomide, le méthyle 2-(bromométhyle). )-4-nitrobenzoate, 2-(bromométhyl)-5-nitrobenzoate de méthyle, 2-(bromométhyl)-6-nitrobenzoate de méthyle et 2-(chlorométhyl)-3-nitrobenzoate de méthyle. Ces normes d'impuretés jouent un rôle essentiel dans l'évaluation de la pureté et de la sécurité du lénalidomide, un ingrédient pharmaceutique actif.
Lénalidomide [CAS : 191732-72-6] est un analogue de la thalidomide aux propriétés anticancéreuses. C'est un agent immunomodulateur et antinéoplasique traitant le myélome multiple. Dérivé du phtalimide et de la pipéridone, le lénalidomide présente des caractéristiques immunomodulatrices et anti-angiogéniques. Il prend en charge l'anémie transfusionnelle dans les syndromes myélodysplasiques et le lymphome à cellules du manteau récidivant ou réfractaire.
Le lénalidomide, disponible sous le nom de Revlimid, est un analogue de la thalidomide approuvé par la FDA américaine et utilisé pour traiter diverses affections. Il prend en charge le syndrome myélodysplasique (SMD) chez les patients présentant une anémie transfusionnelle ou une anomalie génétique. Le lénalidomide est également utilisé pour le myélome multiple réfractaire ou en rechute, soit en monothérapie, soit en association avec la dexaméthasone, le bortézomib et la dexaméthasone, ou le melphalan et la prednisone pour les patients nouvellement diagnostiqués qui ne sont pas éligibles à une greffe. De plus, il traite le lymphome à cellules du manteau récidivant ou réfractaire.
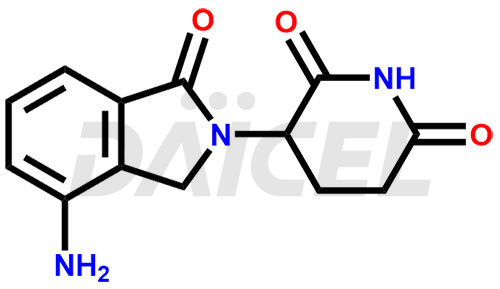
Le nom chimique du lénalidomide est 3-(4-Amino-1,3-dihydro-1-oxo-2H-isoindol-2-yl)-2,6-pipéridinedione. Sa formule chimique est C13H13N3O3, et son poids moléculaire est d'environ 259.26 g/mol.
Le lénalidomide empêche la sécrétion de cytokines pro-inflammatoires et augmente la sécrétion de cytokines anti-inflammatoires.
Pendant la fabrication1 du lénalidomide, des impuretés peuvent se former comme sous-produits. Ils peuvent affecter la qualité et la sécurité du médicament. Diverses techniques analytiques, comme la chromatographie liquide haute performance (HPLC), permettent d'identifier et de quantifier ces impuretés. Des mesures de contrôle strictes garantissent que les niveaux d'impuretés restent dans des limites acceptables. Le profil d'impuretés du lénalidomide est étroitement surveillé tout au long du processus de fabrication afin de maintenir sa pureté et sa puissance.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour préparer les normes d'impuretés du lénalidomide. Nous proposons une gamme d'étalons d'impuretés de lénalidomide, tels que le 4-nitrophthalide (impureté de lactone de lénalidomide KSM), l'impureté de lénalidomide Amadori, l'impureté de lénalidomide-3, l'impureté d'Amadori à chaîne ouverte de lénalidomide, le 2-(bromométhyl)-4-nitrobenzoate de méthyle, le méthyle 2. -(bromométhyl)-5-nitrobenzoate, 2-(bromométhyl)-6-nitrobenzoate de méthyle et 2-(chlorométhyl)-3-nitrobenzoate de méthyle. Nos impuretés disposent d'un certificat d'analyse (CoA) détaillé et d'un rapport de caractérisation complet. Le CoA englobe les données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Des données supplémentaires, telles que 13C-DEPT, peuvent être fournies sur demande. Nous pouvons synthétiser des étalons d’impuretés ou des produits de dégradation inconnus du lénalidomide. Chaque livraison dispose d'un rapport de caractérisation complet.
Des techniques analytiques telles que la chromatographie liquide haute performance (HPLC), la chromatographie liquide (LC) ou la spectrométrie de masse (MS) permettent de détecter et de quantifier les impuretés du lénalidomide.
Des mesures de contrôle de qualité strictes sont mises en œuvre pendant le processus de fabrication du lénalidomide pour minimiser les impuretés. Cela comprend la surveillance et l’optimisation des conditions de réaction, des étapes de purification et des conditions de stockage.
Oui, les impuretés contenues dans le lénalidomide peuvent contribuer à la dégradation et réduire sa stabilité au fil du temps, ce qui pourrait avoir un impact sur sa durée de conservation et son efficacité thérapeutique.
Il est recommandé de conserver les impuretés du lénalidomide à une température ambiante contrôlée, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.