Lamivudine
Renseignements généraux
Impuretés de la lamivudine et lamivudine
Daicel Pharma synthétise des impuretés de lamivudine de haute qualité comme la 2′-Epi Lamivudine, l'énantiomère de lamivudine, l'impureté de lamivudine G, l'impureté de lamivudine H, l'impureté de lamivudine J et la trans-lamivudine, qui sont cruciales dans l'analyse de la qualité, de la stabilité et de la sécurité biologique du ingrédient pharmaceutique actif Lamivudine. De plus, Daicel Pharma propose une synthèse personnalisée des impuretés de lamivudine et les livre dans le monde entier.
Lamivudine [CAS : 134678/17/4] est un analogue nucléosidique synthétique qui fonctionne comme un inhibiteur de la transcriptase inverse et est utilisé pour traiter les personnes atteintes d'infections par le virus de l'immunodéficience humaine (VIH) et le virus de l'hépatite B (VHB).
Lamivudine : utilisation et disponibilité commerciale
La lamivudine est un médicament sur ordonnance appartenant à la classe des inhibiteurs nucléosidiques de la transcriptase inverse (INTI), utilisé en association avec d'autres médicaments pour traiter le virus de l'immunodéficience humaine de type 1 (VIH-1) et en monothérapie contre le virus de l'hépatite B (VHB). infections. Il réduit la charge virale mais n’éradique pas le virus du corps humain. La lamivudine est disponible sous forme de comprimés et de solution buvable et est également incluse dans plusieurs co-formulations telles que Cimduo, Dovato, Triumeq. Epivir est le nom commercial de la lamivudine.
Structure et mécanisme d'action de la lamivudine 
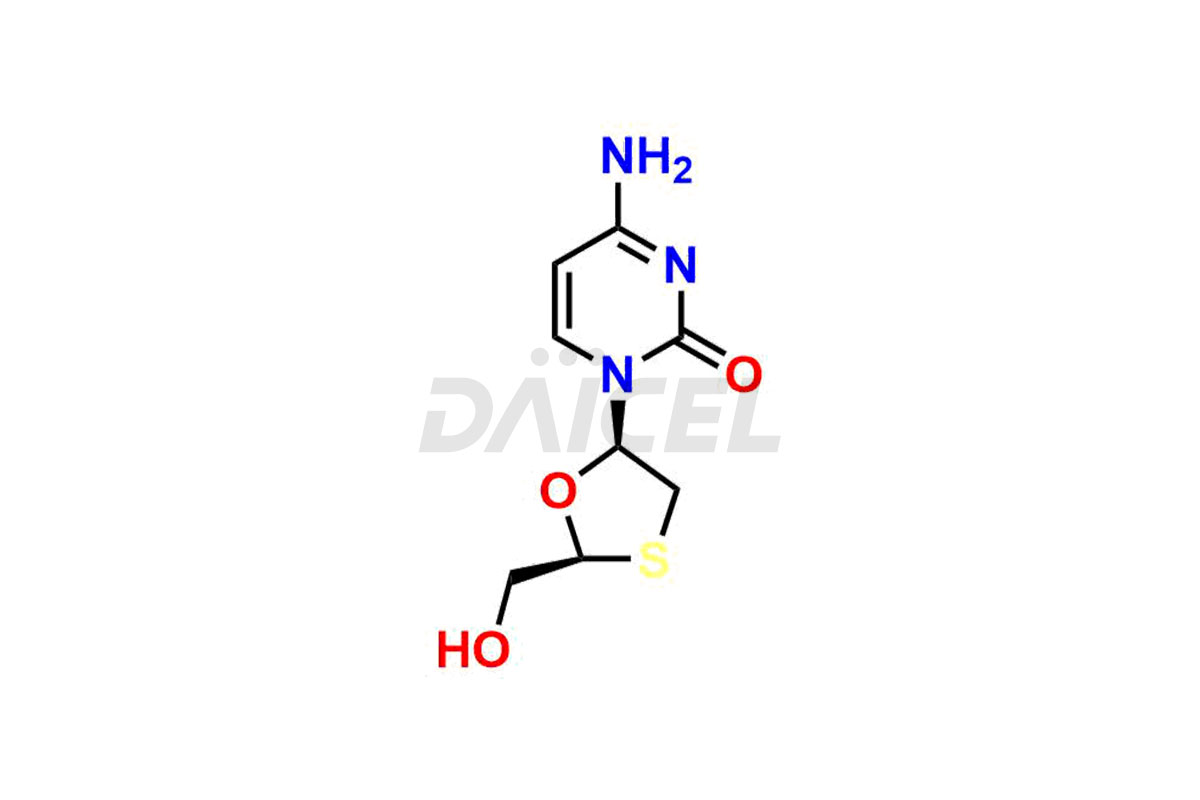
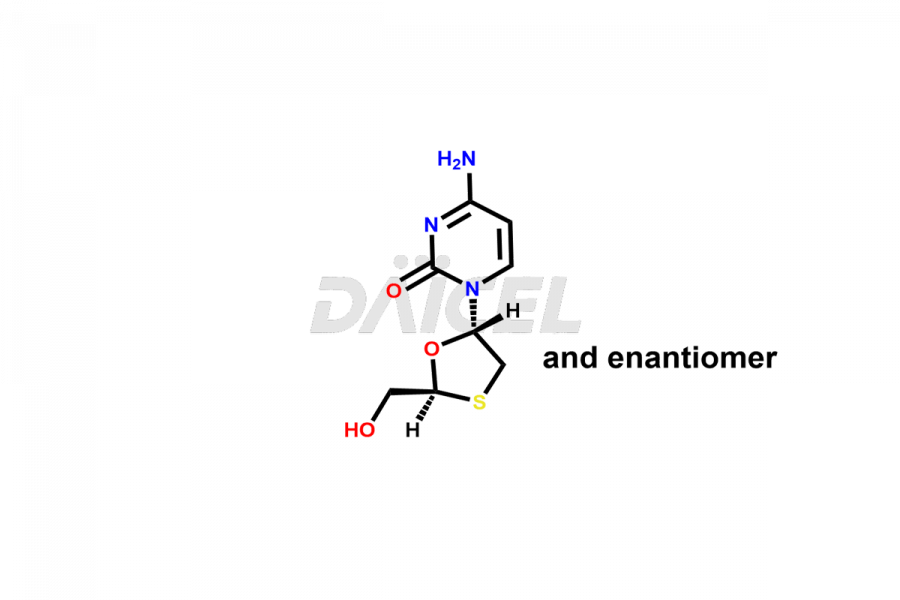
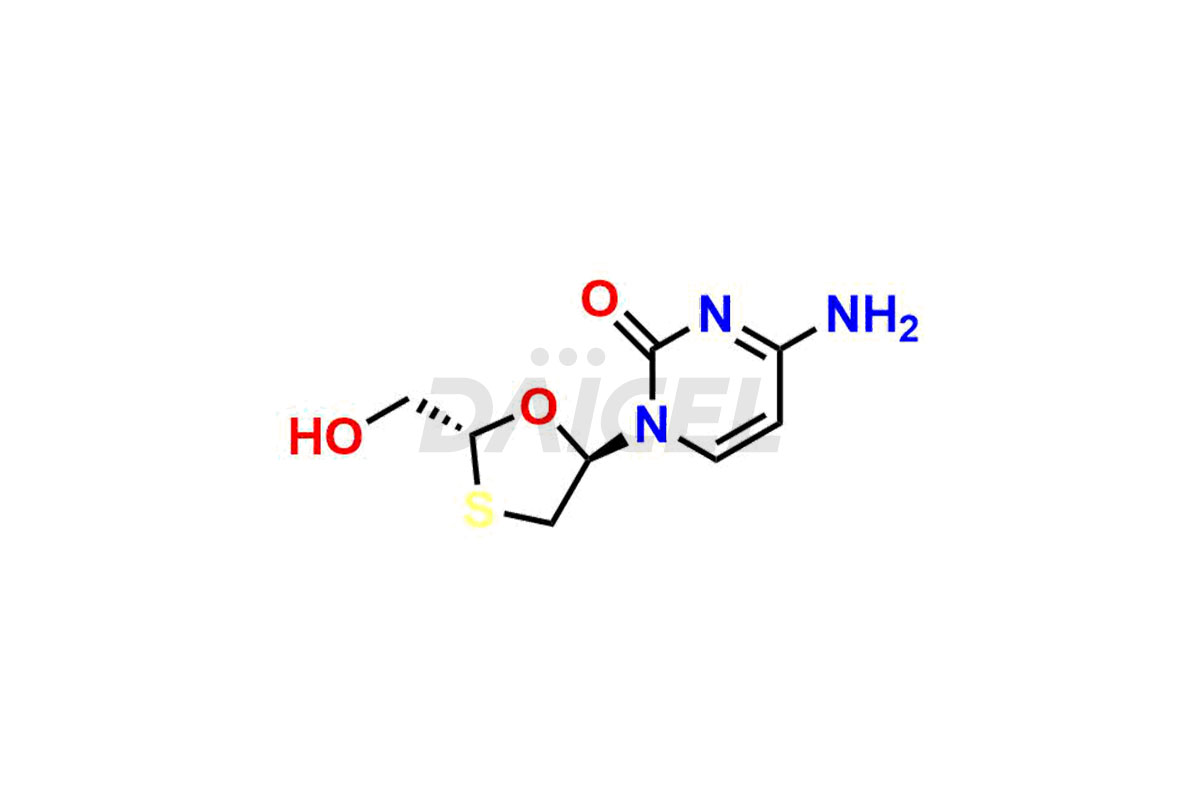
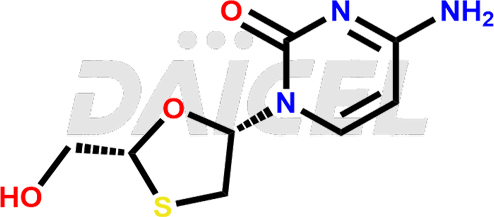
Le nom chimique de la lamivudine est 4-Amino-1-[(2R,5S)-2-(hydroxyméthyl)-1,3-oxathiolan-5-yl]-2(1H)-pyrimidinone. Sa formule chimique est C8H11N3O3S, et son poids moléculaire est d'environ 229.26 g/mol.
La lamivudine est phosphorylée en lamivudine triphosphate (L-TP), son métabolite actif 5′-triphosphate. Il inhibe la transcriptase inverse (RT) du VIH-1 via la terminaison de la chaîne d'ADN après incorporation dans l'ADN viral.
Impuretés et synthèse de la lamivudine
La lamivudine forme des impuretés lors de son processus de fabrication1, le stockage et le transport. Les impuretés proviennent de diverses sources, telles que les matières premières, les solvants, les réactifs ou les produits de dégradation. Ils peuvent affecter la qualité, la sécurité et l’efficacité du produit médicamenteux et leur contrôle est donc crucial. Des directives réglementaires strictes exigent la surveillance et le contrôle des impuretés dans des limites acceptables tout au long du cycle de vie du médicament afin de garantir la qualité de la lamivudine.
Daicel fournit un certificat d'analyse (CoA) pour les étalons d'impuretés de lamivudine, la 2′-épi-lamivudine, l'énantiomère de lamivudine, l'impureté de lamivudine G, l'impureté de lamivudine H, l'impureté de lamivudine J et la trans-lamivudine. Le CoA est émis par une installation d'analyse conforme aux BPF et contient des données de caractérisation complètes, telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2. Des données de caractérisation supplémentaires, telles que 13C-DEPT et CHN, peuvent être fournies sur demande. Daicel peut également préparer toute impureté ou produit de dégradation inconnu de la lamivudine. Nous remettons un rapport de caractérisation complet à la livraison.
Bibliographie
FAQ
Bibliographie
- Coates, Jonathan Alan Victor ; Mouton, Ian Martin ; Penn, Charles Richard ; Stockeur, Richard ; Williamson, Christopher, Analogues nucléosidiques du 1,3-oxathiolane, IAF Biochem International Inc., Canada, EP625150A1 1, 14 novembre 1991
- Hsyu, Poe-Hirr ; Lloyd, Thomas L., Analyse chromatographique liquide haute performance automatisée de la (-)-2'-désoxy-3'-thiacytidine dans les fluides biologiques à l'aide de l'enrichissement séquentiel automatisé de traces de systèmes de dialysat, Journal of Chromatography B : Biomedical Sciences and Applications, Volume : 655, Numéro : 2, Pages : 253-60, 1994
Foire aux Questions
Comment les impuretés de Lamivudine sont-elles identifiées et quantifiées ?
Les impuretés contenues dans la lamivudine sont identifiées et quantifiées à l'aide de diverses méthodes analytiques, telles que la chromatographie liquide haute performance (HPLC) et la chromatographie liquide-spectroscopie de masse (LC-MS). Ces méthodes séparent, identifient et quantifient les impuretés présentes dans le produit médicamenteux.
Comment les impuretés sont-elles contrôlées lors de la fabrication de la Lamivudine ?
Les impuretés sont contrôlées lors de la fabrication de la lamivudine en utilisant des processus de synthèse, de purification et de formulation appropriés. De plus, des conditions de stockage et un emballage appropriés empêchent la formation et l’accumulation d’impuretés.
La présence d’impuretés de Lamivudine peut-elle affecter l’efficacité du médicament ?
La présence d'impuretés dans la lamivudine peut affecter l'efficacité du médicament, car elles peuvent interférer avec le mécanisme d'action du médicament ou modifier son profil pharmacocinétique.
Quelles sont les conditions de température nécessaires pour conserver les impuretés de la lamivudine ?
Les impuretés de la lamivudine sont conservées à une température ambiante contrôlée entre 2 et 8 ⁰C ou comme indiqué sur le certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.