Iopamidol
Renseignements généraux
Impuretés de l'Iopamidol et Iopamidol
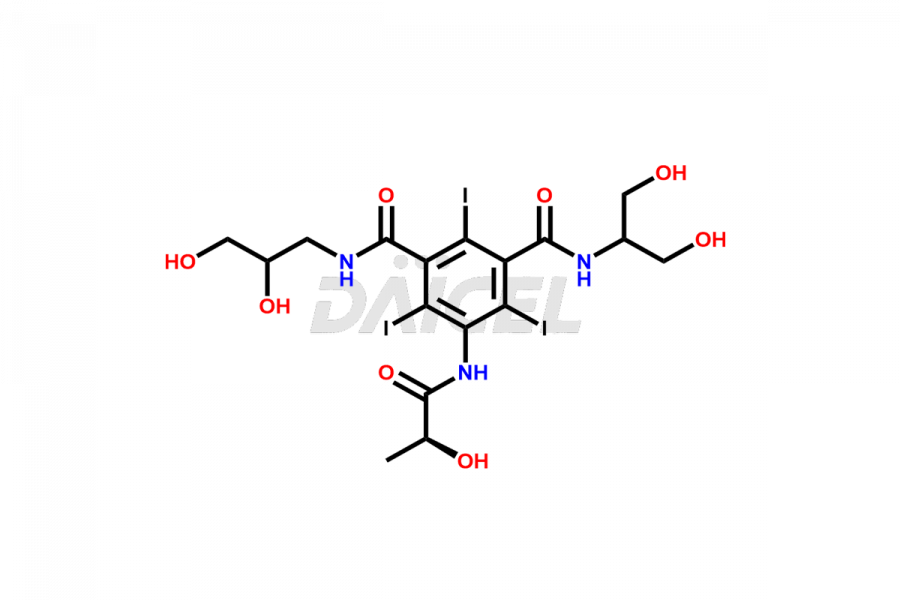
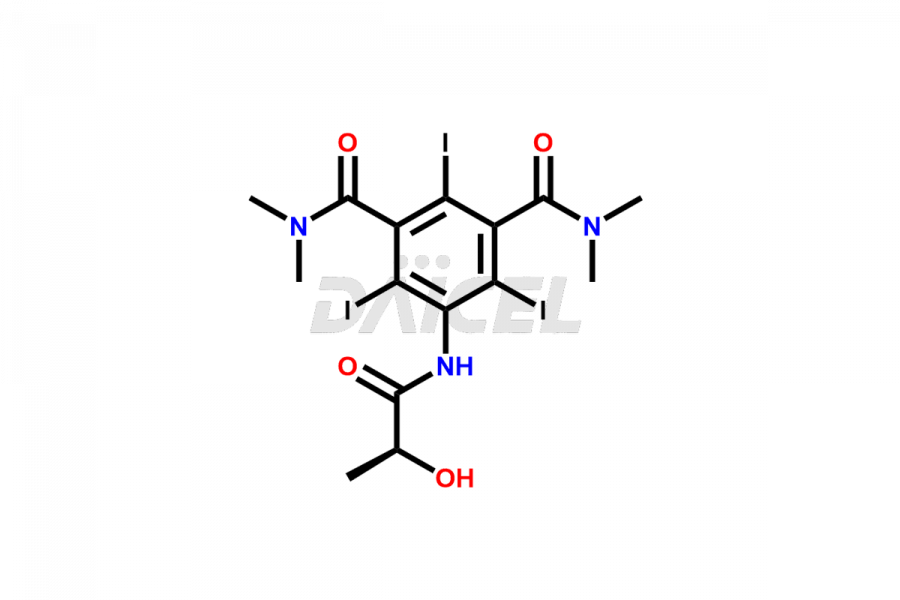
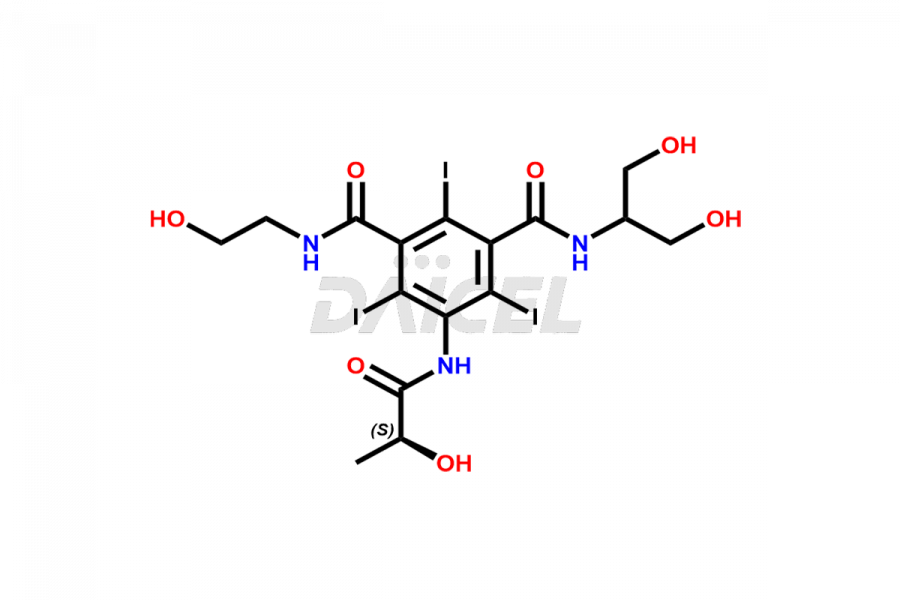
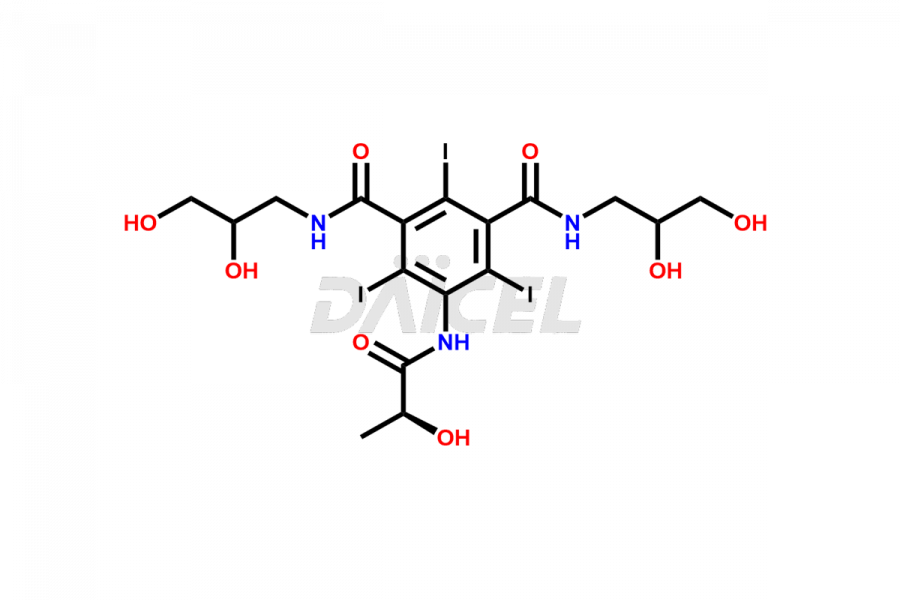
Daicel Pharma synthétise des normes d'impuretés pour l'Iopamidol, un ingrédient pharmaceutique actif. Nous proposons des normes d'impuretés cruciales telles que l'isomère 2,3-dihydroxypropyle/Iso Iopamidol, le bis-diméthylamino Iopamidol, le dérivé hydroxyéthyle (ou) le butryl (ou) l'impureté EP-J, l'iso Iso Iopamidol, le dérivé N, N diméthylamino, le diméthyle. amino Iopamidol, Iopamidol EP Impurity-F et O-Acetyl Iopamidol/AP ADI, qui jouent un rôle essentiel dans l'évaluation de la pureté et de la sécurité de l'Iopamidol. Daicel Pharma propose également une synthèse personnalisée des normes d'impuretés de l'Iopamidol pour répondre aux besoins spécifiques des clients et aux options de livraison dans le monde entier.
Iopamidol [CAS : 60166/93/0] est un agent de contraste non ionique soluble dans l'eau utilisé dans les procédures radiologiques telles que la myélographie, l'arthrographie, la néphroangiographie, l'artériographie, etc. C'est un composé benzènedicarboxamide et agit comme un milieu radio-opaque dans ces procédures.
Iopamidol : utilisation et disponibilité commerciale
Isovue-128, Isovue-200, etc. sont les marques sous lesquelles Iopamidol est disponible. Il s'agit d'un produit de contraste radiographique non ionique et hydrosoluble contenant de l'iode organique. L'iopamidol a pour but de bloquer les rayons X, permettant ainsi la visualisation des structures corporelles dépourvues d'iode. Le degré d'opacité observé est directement lié à la quantité d'agent de contraste iodé présente sur le trajet des rayons X. La distribution et l'élimination de l'Iopamidol jouent un rôle crucial dans la visualisation des structures corporelles.
Structure de l'iopamidol et mécanisme d'action 
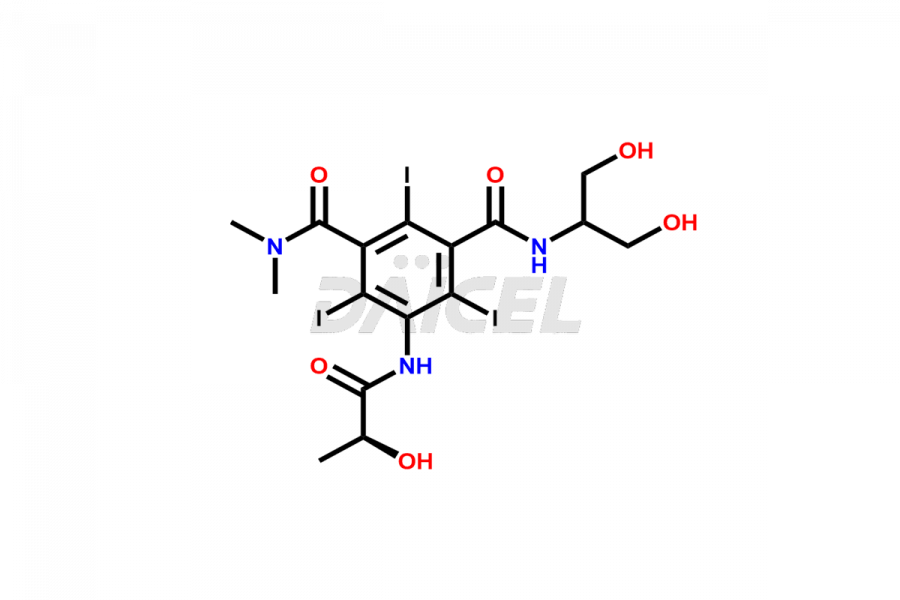
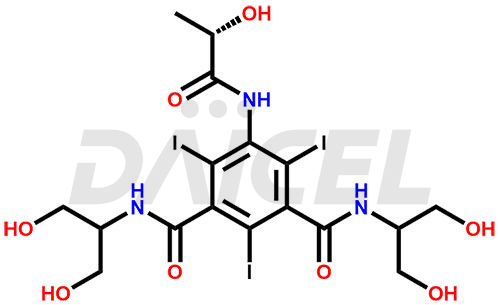
Le nom chimique de l'iopamidol est N1, N3-Bis[2-hydroxy-1-(hydroxyméthyl)éthyl]-5-[[(2S)-2-hydroxy-1-oxopropyl]amino]-2,4,6-triiodo. -1,3-benzènedicarboxamide. Sa formule chimique est C17H22I3N3O8, et son poids moléculaire est d'environ 777.1 g/mol.
L'iopamidol améliore l'imagerie cérébrale tomodensitométrique avec une efficacité radiographique.
Impuretés et synthèse de l'iopamidol
Le contrôle et l’analyse des impuretés de l’Iopamidol sont cruciaux pour garantir sa qualité et sa sécurité en tant que produit de contraste radiographique. Ils peuvent provenir de diverses sources, notamment du processus de synthèse et des conditions de stockage. Il est essentiel de surveiller et de contrôler les niveaux d’impuretés à chaque étape de préparation. Les techniques analytiques telles que la chromatographie liquide haute performance (HPLC) et la spectrométrie de masse (MS) contribuent au profilage et à la quantification des impuretés. Des mesures de contrôle de qualité strictes peuvent répondre aux exigences réglementaires et maintenir la pureté et la sécurité de l'Iopamidol. Des tests et une surveillance réguliers aident à minimiser les impuretés et à garantir la qualité souhaitée de l'agent de contraste.
Daicel Pharma, conformément aux normes cGMP, exploite une installation d'analyse où nous préparons des étalons d'impuretés d'Iopamidol comme l'isomère 2,3-dihydroxypropyle/Iso Iopamidol, le Bis-Diméthylamino Iopamidol, le dérivé hydroxyéthyle (ou) le butryl (ou) l'impureté EP-J , Iso Iso Iopamidol, dérivé N, N diméthyl amino, diméthyl amino Iopamidol, Iopamidol EP Impurity-F et O-Acétyl Iopamidol/AP ADI. Nous proposons un certificat d'analyse (CoA) complet pour ces normes d'impuretés, fournissant un rapport de caractérisation détaillé. Le CoA comprend des données obtenues grâce à des techniques d’analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. Nous pouvons synthétiser des étalons d’impuretés ou des produits de dégradation inconnus de l’Iopamidol. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Felder, Ernst ; Pitre, Davide, Dérivés d'amide hydroxylés non ionisants solubles dans l'eau de l'acide 2,4,6-triiodo-isophtalique, Savac A.-G., Suisse, US4001323A, 4 janvier 1977.
- Shihabi, ZK; Rocco, MV ; Hinsdale, ME, Analyse de l'agent de contraste iopamidol dans le sérum par électrophorèse capillaire, Journal of Liquid Chromatography, Volume : 18, Numéro : 18 et 19, Pages : 3825-31, 1995
Foire aux Questions
Les impuretés de l’Iopamidol peuvent-elles avoir un impact sur sa stabilité ?
Certaines impuretés contenues dans l'Iopamidol peuvent affecter sa stabilité. Ils peuvent contribuer aux processus de dégradation, entraînant une durée de conservation réduite ou des modifications des propriétés du médicament. Et le contrôle des impuretés aide à maintenir la stabilité.
Comment les impuretés de l’Iopamidol sont-elles identifiées ?
Les impuretés présentes dans l'Iopamidol sont identifiées à l'aide de techniques analytiques telles que la spectrométrie de masse, la spectroscopie de résonance magnétique nucléaire et la spectroscopie infrarouge. Ces méthodes aident à déterminer la structure chimique et la composition des impuretés.
Quel solvant aide à analyser les impuretés de l’Iopamidol ?
L'eau est couramment utilisée comme solvant lors de l'analyse de nombreuses impuretés contenues dans l'Iopamidol.
Comment les impuretés de l’Iopamidol doivent-elles être stockées en termes de température ?
Il est recommandé de conserver les impuretés de l'Iopamidol à température ambiante, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.