Imatinib
Renseignements généraux
Impuretés de l'Imatinib et Imatinib
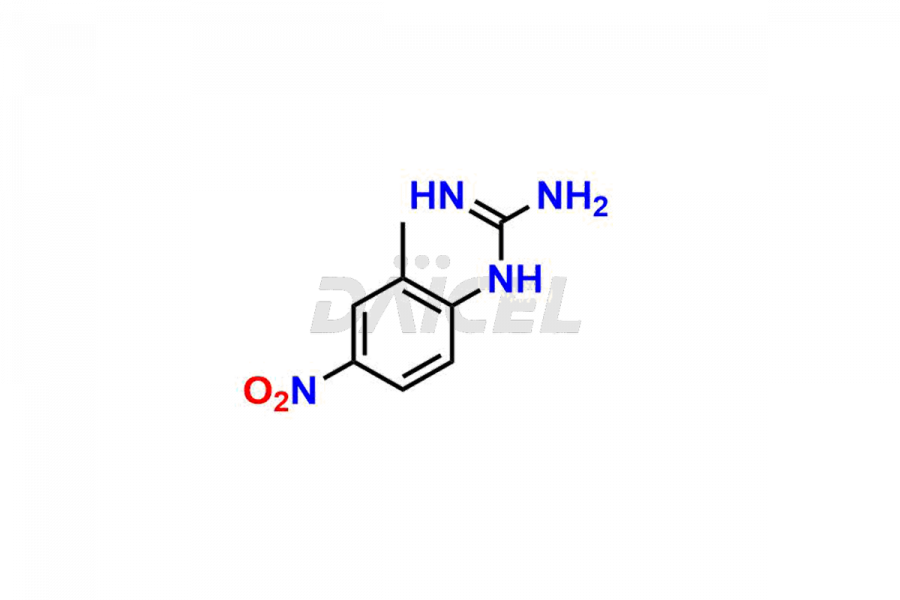
Daicel Pharma propose des options de livraison dans le monde entier pour une synthèse personnalisée des impuretés de l'Imatinib, y compris des impuretés telles que la 1-(2-méthyl-3-nitrophényl)guanidine, la 1-(2-méthyl-4-nitrophényl)guanidine, la 1-(2-méthyl- Nitrate de 5-nitrophényl)guanidine, N-(2-méthyl-5-nitrophényl)-N'-Carbamoyl Guanidine et N-Desméthyl Imatinib. Ces impuretés jouent un rôle essentiel dans l’évaluation de la pureté et de la sécurité de l’Imatinib, un ingrédient pharmaceutique actif.
Utilisé comme son sel mésylate, l'Imatinib [CAS : 152459/95/5] est un benzamide et un inhibiteur de petite molécule kinase pour le traitement du cancer. Il traite la leucémie myéloïde chronique et les tumeurs stromales gastro-intestinales causées par des tyrosine kinases anormales et constitutivement exprimées qui entraînent une croissance cellulaire non régulée.
Imatinib : utilisation et disponibilité commerciale
Le mésylate d'imatinib (Imatinib), ou Gleevec, est un inhibiteur oral de la tyrosine kinase approuvé par la FDA américaine pour traiter la leucémie myéloïde chronique. Il a également reçu l'approbation pour plusieurs autres conditions oncologiques. Ils comprennent divers stades de leucémie myéloïde chronique à chromosome Philadelphie positif, la leucémie lymphoblastique aiguë à chromosome Philadelphie positif en rechute/réfractaire, les maladies myélodysplasiques/myéloprolifératives avec réarrangements génétiques spécifiques, la mastocytose systémique agressive, le syndrome hyperéosinophile/leucémie éosinophile chronique, le dermatofibrosarcome protuberans, non résécable/métastatique. tumeurs stromales gastro-intestinales (GIST) et traitement adjuvant après résection de GIST Kit-positif.
Structure et mécanisme d'action de l'imatinib 
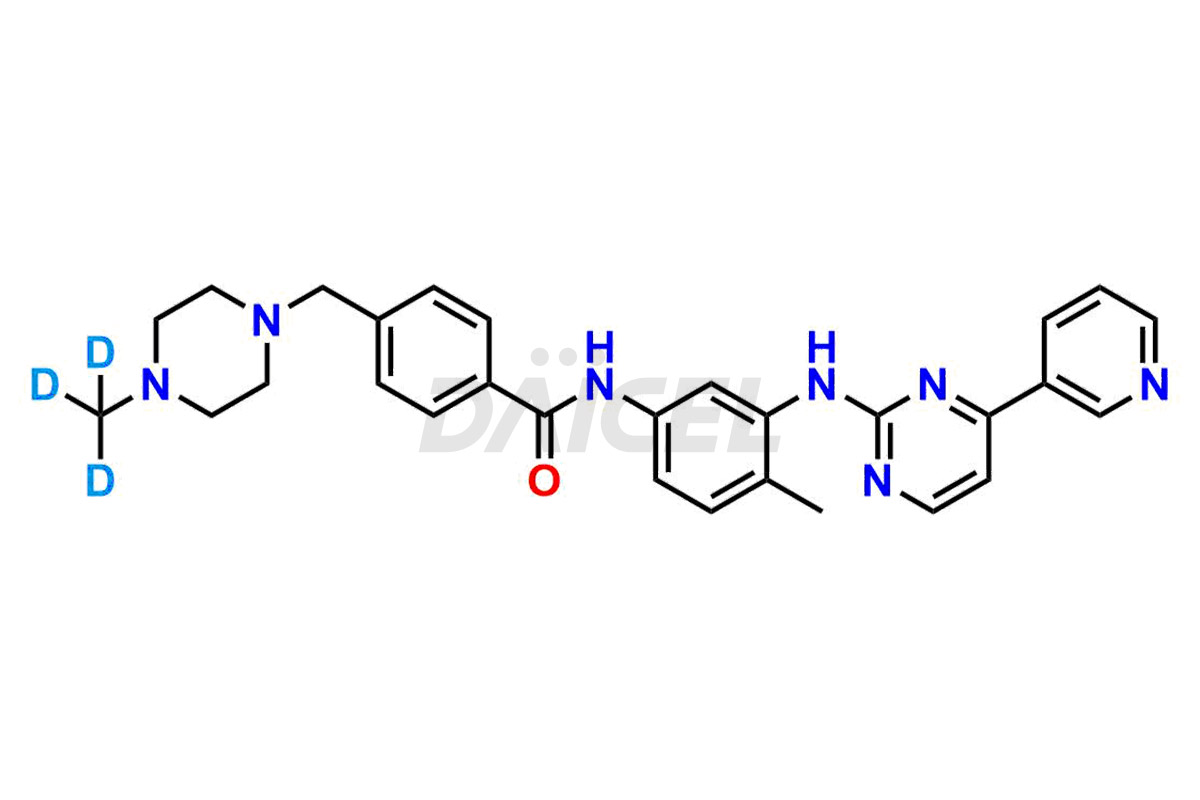
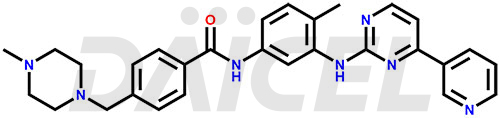
Le nom chimique de l'imatinib est 4-[(4-méthyl-1-pipérazinyl)méthyl]-N-[4-méthyl-3-[[4-(3-pyridinyl)-2-pyrimidinyl]amino]phényl]benzamide. Sa formule chimique est C29H31N7O, et son poids moléculaire est d'environ 493.6 g/mol.
L'imatinib induit l'apoptose et inhibe l'activité de la tyrosine kinase Bcr-Abl. Une anomalie du chromosome Philadelphie dans la leucémie myéloïde chronique (LMC) crée une tyrosine kinase anormale.
Impuretés et synthèse de l'imatinib
L'imatinib peut contenir des impuretés qui peuvent être présentes en raison de divers facteurs lors de sa synthèse1 et le stockage. Les impuretés courantes de l'Imatinib comprennent des substances apparentées provenant de processus de synthèse ou de dégradation incomplets, des impuretés organiques provenant de matières premières ou d'intermédiaires, des impuretés inorganiques telles que des métaux lourds ou des sels et des solvants résiduels utilisés lors de la fabrication. Les autorités réglementaires ont établi des limites pour les niveaux d'impuretés afin de garantir la qualité et la sécurité de l'Imatinib. Des mesures de contrôle de qualité strictes mises en œuvre par les fabricants minimisent les impuretés et répondent aux exigences réglementaires pour le produit final.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés d'imatinib telles que la 1-(2-méthyl-3-nitrophényl)guanidine, la 1-(2-méthyl-4-nitrophényl)guanidine, la 1-( Nitrate de 2-méthyl-5-nitrophényl)guanidine, N-(2-méthyl-5-nitrophényl)-N'-Carbamoyl Guanidine et N-Desméthyl Imatinib. Nous proposons un étalon d'Imatinib marqué au deutérium, Imatinib-D3, essentiel pour la recherche bioanalytique et les études BA/BE. Nos impuretés disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. Nous pouvons synthétiser des impuretés inconnues de l'Imatinib, des produits de dégradation et des composés marqués. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Zimmermann, Juerg, Dérivés de pyrimidine et procédé pour leur préparation, Ciba-Geigy A.-G., Suisse, EP564409B1, 19 janvier 2001
- Widmer, N. ; Béguin, A. ; Rochat, B. ; Buclin, T. ; Kovacsovics, T. ; Duchosal, MA; Leyvraz, S. ; Rosselet, A. ; Biollaz, J. ; Decosterd, LA, Détermination de l'imatinib (Gleevec) dans le plasma humain par extraction en phase solide-chromatographie liquide-détection de l'absorbance ultraviolette, Journal of Chromatography B : Analytical Technologies in the Biomedical and Life Sciences, Volume : 803, Numéro : 2, Pages : 285-292, 2004
Foire aux Questions
Comment les autorités réglementaires surveillent-elles et garantissent-elles le respect des limites d'impuretés dans l'Imatinib ?
Les autorités réglementaires effectuent des inspections des installations de fabrication, examinent les données des tests de contrôle qualité et évaluent la conformité aux directives réglementaires pour surveiller les niveaux d'impuretés dans l'Imatinib. Ils peuvent également effectuer une surveillance et un échantillonnage après commercialisation pour vérifier la conformité continue.
Existe-t-il des impuretés spécifiques à l'Imatinib qui nécessitent une attention particulière ?
Certaines impuretés de l'Imatinib, telles que les impuretés génotoxiques, font l'objet d'une attention particulière en raison de leur potentiel à endommager l'ADN et à avoir des effets néfastes sur la santé. Les fabricants disposent de stratégies de contrôle robustes pour minimiser les impuretés génotoxiques et garantir que leurs niveaux se situent dans des limites acceptables.
Quel solvant aide à analyser les impuretés de l’Imatinib ?
Le DMSO ou l'eau sont les solvants couramment utilisés lors de l'analyse de nombreuses impuretés de l'Imatinib.
Comment les impuretés de l’Imatinib doivent-elles être conservées en termes de température ?
Il est recommandé de conserver les impuretés de l'imatinib à température ambiante, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.