Charger plus
Vous avez vu 9 sur 35 articles
Daicel Pharma propose des options de livraison dans le monde entier pour une synthèse personnalisée des impuretés de l'ibuprofène, y compris des impuretés telles que l'Ibuprofène Ph. Eur. Impureté G, impureté inconnue de l'ibuprofène, 3-hydroxy-2,2-diméthylpropyl 2-(4-isobutylphényl)propanoate, esters d'ibuprofène 1,2-propylène glycol (mélange d'isomères régio et stéréo), ibuprofène 1,2,3-propanetriol esters (mélange d'isomères régio et stéréo), etc. Ces impuretés jouent un rôle essentiel dans l’évaluation de la pureté et de la sécurité de l’ibuprofène, un ingrédient pharmaceutique actif.
L'ibuprofène [CAS : 15687/27/1], un anti-inflammatoire non stéroïdien (AINS) et un dérivé de l'acide propionique aident à soulager les symptômes liés à l'arthrite, à la dysménorrhée primaire et à la fièvre. Il présente des effets analgésiques, anti-inflammatoires et antipyrétiques.
L'ibuprofène, disponible sous diverses marques commerciales, Advil, Caldolor, Ibuprohm, Medipren, Nuprin, etc., est un anti-inflammatoire non stéroïdien (AINS). Il prend en charge et traite les maladies inflammatoires, les troubles rhumatoïdes, les douleurs légères à modérées, la fièvre, la dysménorrhée et l'arthrose. Il est disponible sur ordonnance pour les affections plus graves et en vente libre pour un léger soulagement de la douleur.
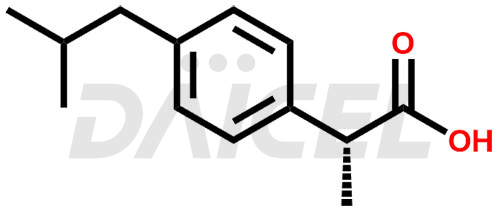
Le nom chimique de l’ibuprofène est l’acide α-méthyl-4-(2-méthylpropyl) benzène acétique. Sa formule chimique est C13H18O2, et son poids moléculaire est d'environ 206.28 g/mol.
L'ibuprofène inhibe les précurseurs des prostaglandines, tels que la cyclooxygénase, une enzyme permettant la synthèse des prostaglandines.
L'ibuprofène peut contenir des impuretés provenant des processus de fabrication1 ou du stockage. Les impuretés courantes de l'ibuprofène comprennent les impuretés des isomères de l'ibuprofène, les impuretés d'acide carboxylique associées, les impuretés organiques provenant des matières premières ou des intermédiaires, les impuretés inorganiques telles que les métaux lourds ou les sels et les solvants résiduels utilisés lors de la synthèse ou de la purification. Les autorités réglementaires fixent des limites aux niveaux d'impuretés pour garantir la sécurité et la qualité de l'ibuprofène. Les fabricants adhèrent à des mesures strictes de contrôle de qualité pour minimiser les impuretés et respecter les normes réglementaires pour le produit final.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour la préparation d'étalons d'impuretés d'ibuprofène, tels que l'Ibuprofen Ph. Eur. Impureté G, impureté inconnue de l'ibuprofène, 3-hydroxy-2,2-diméthylpropyl 2-(4-isobutylphényl)propanoate, esters d'ibuprofène 1,2-propylène glycol (mélange d'isomères régio et stéréo), ibuprofène 1,2,3-propanetriol esters (mélange d'isomères régio et stéréo), etc. Nous proposons des composés d'ibuprofène marqués au deutérium, notamment l'ibuprofène-D3, l'isomère S de l'ibuprofène-D3, l'ibuprofène-13CD3 et l'isomère R de l'ibuprofène-D3, essentiels pour la recherche bioanalytique et les études BA/BE. Nos impuretés disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. Nous pouvons synthétiser des impuretés ou des produits de dégradation inconnus de l’ibuprofène et des composés marqués. Chaque livraison dispose d'un rapport de caractérisation complet.
Si la présence d'impuretés dans l'ibuprofène se situe dans des limites acceptables, il n'y a aucune cause d'effets indésirables ni d'impact sur l'efficacité. Cependant, des niveaux d’impuretés plus élevés pourraient affecter la sécurité et l’efficacité du médicament.
Bien que les processus de fabrication et les mesures de contrôle de la qualité des différentes marques d'ibuprofène puissent varier, toutes les formulations doivent être conformes aux normes réglementaires relatives aux niveaux d'impuretés. Par conséquent, la présence d’impuretés doit se situer dans des limites acceptables quelle que soit la marque.
L'acétonitrile ou le méthanol sont les solvants couramment utilisés lors de l'analyse de nombreuses impuretés contenues dans l'ibuprofène.
Il est recommandé de conserver les impuretés de l'ibuprofène à une température ambiante contrôlée, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.