Charger plus
Vous avez vu 9 sur 11 articles
Daicel Pharma propose des options de livraison dans le monde entier pour une synthèse personnalisée des impuretés de l'hydroxychloroquine, y compris des impuretés telles que la bis-déséthylchloroquine, le N-oxyde de chloroquine, la déséthylchloroquine, la déséthylhydroxychloroquine (DHCQ), etc. Ces impuretés permettent d’évaluer la pureté et la sécurité d’un ingrédient pharmaceutique actif, l’hydroxychloroquine.
Hydroxychloroquine [CAS : 118/42/3], un composé aminoquinoléine, est une variante de la chloroquine. Il traite le lupus érythémateux, la polyarthrite rhumatoïde et les éruptions cutanées photosensibles, présentant des propriétés similaires à celles de la chloroquine en tant que médicament antipaludique, ciblant les formes érythrocytaires des parasites du paludisme. Parallèlement à son activité antipaludique, l’hydroxychloroquine agit comme agent antirhumatismal. Il possède des propriétés immunosuppressives et démontre une action anti-autophagie.
L'hydroxychloroquine cible les formes érythrocytaires des parasites du paludisme. Sa toxicité sélective contre les stades érythrocytaires de l'infection plasmodiale peut être due à sa concentration dans les érythrocytes parasités. De plus, en tant qu'agent antirhumatismal, l'hydroxychloroquine supprime le système immunitaire, provoquant une diminution du facteur rhumatoïde et des réactifs de la phase aiguë. Il présente également une affinité pour les globules blancs, stabilisant les membranes lysosomales et inhibant les enzymes impliquées dans la dégradation du cartilage, notamment la collagénase et les protéases. Notamment, Plaquenil est le nom de marque associé aux formulations de ce médicament.
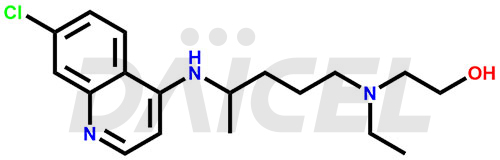
Le nom chimique de l’hydroxychloroquine est 2-[[4-[(7-Chloro-4-quinolinyl)amino]pentyl]éthylamino]éthanol. Sa formule chimique est C18H26CIN3O, et son poids moléculaire est d'environ 335.9 g/mol.
Le mécanisme d'action de l'hydroxychloroquine est inconnu.
Des impuretés d'hydroxychloroquine peuvent survenir lors du processus de fabrication, du stockage ou de la dégradation. Les impuretés peuvent résulter de produits secondaires de réaction, de réactions incomplètes ou d'interactions avec d'autres substances. Les méthodes analytiques telles que la HPLC, la LC-MS, la RMN et la spectroscopie IR permettent d'analyser et de quantifier ces impuretés. Les mesures de contrôle comprennent l'optimisation du processus de synthèse et des étapes de purification et la garantie de conditions de stockage appropriées pour minimiser la formation d'impuretés. Les études de stabilité évaluent le profil des impuretés au fil du temps et établissent des dates de péremption appropriées et des recommandations de stockage. Le respect des directives réglementaires, telles que celles fournies par l'ICH, est essentiel pour garantir la qualité et la sécurité des formulations d'hydroxychloroquine. Un contrôle efficace des impuretés joue un rôle essentiel dans le maintien de l’intégrité de l’hydroxychloroquine en tant que produit pharmaceutique.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour synthétiser les normes d'impuretés d'hydroxychloroquine telles que la bis-déséthylchloroquine, le N-oxyde de chloroquine, la déséthylchloroquine, la déséthylhydroxychloroquine (DHCQ), et plus encore. Nous proposons des étalons d'hydroxychloroquine marqués au deutérium, notamment l'hydroxychloroquine-D5, essentielle pour la recherche bioanalytique et les études BA/BE. Nos impuretés disposent d'un certificat d'analyse (CoA) détaillé qui fournit un rapport de caractérisation complet. Ce rapport comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.1,2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. Nous pouvons synthétiser des impuretés ou des produits de dégradation inconnus de l’hydroxychloroquine et des composés marqués. Chaque livraison dispose d'un rapport de caractérisation complet.
Les normes pharmacopées, telles que la Pharmacopée américaine (USP) ou la Pharmacopée européenne (EP), décrivent les exigences spécifiques en matière de tests d'impuretés pour l'hydroxychloroquine afin de garantir sa qualité et sa sécurité.
Les impuretés contenues dans l'hydroxychloroquine peuvent influencer sa stabilité dans des conditions de stockage spécifiques, telles que la température et l'humidité. Des directives de stockage appropriées aident à maintenir l’intégrité des médicaments.
Lors de l’analyse de nombreuses impuretés dans l’hydroxychloroquine, le méthanol est le solvant courant.
Il est recommandé de conserver les impuretés de l’hydroxychloroquine à une température ambiante contrôlée, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.