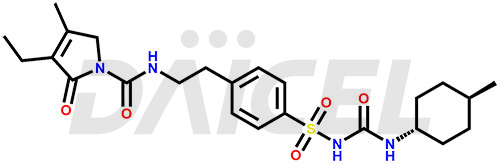
Glimépiride
Renseignements généraux
Impuretés du glimépiride et glimépiride
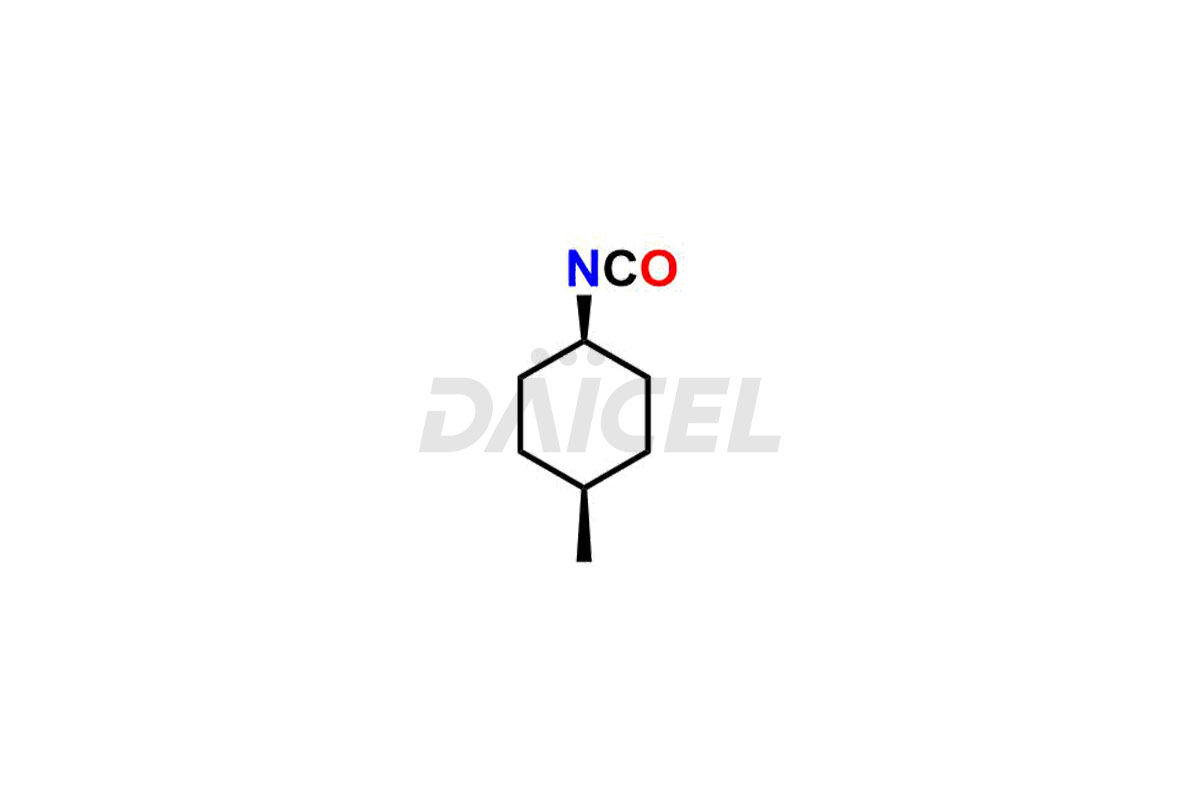
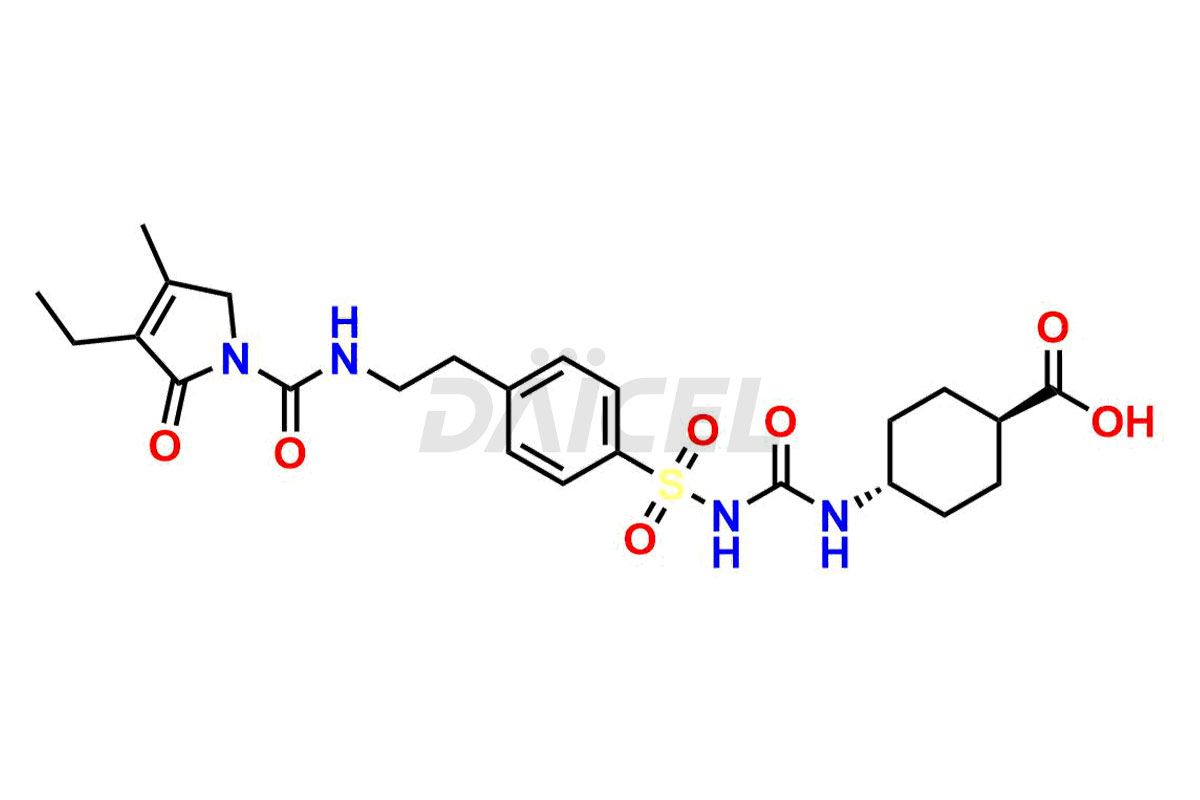
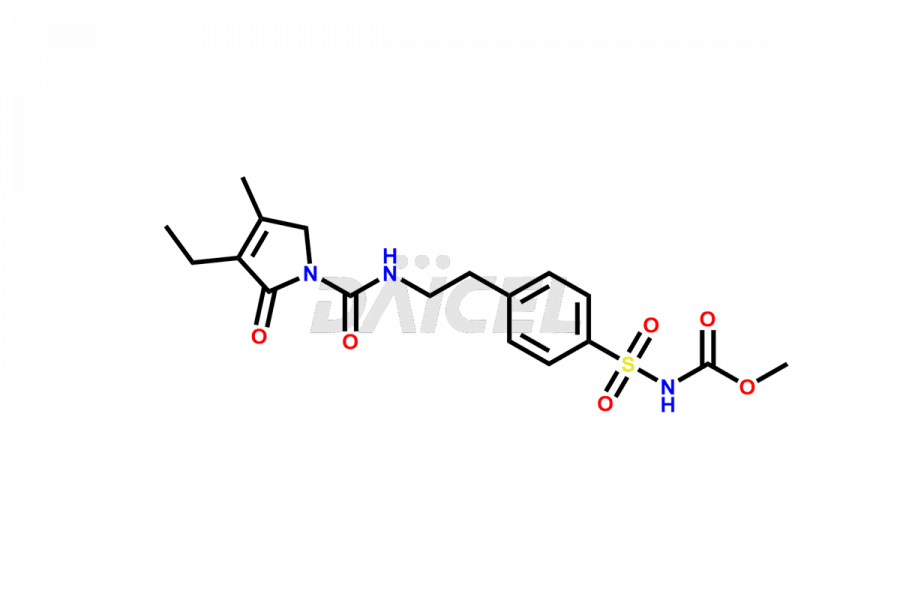
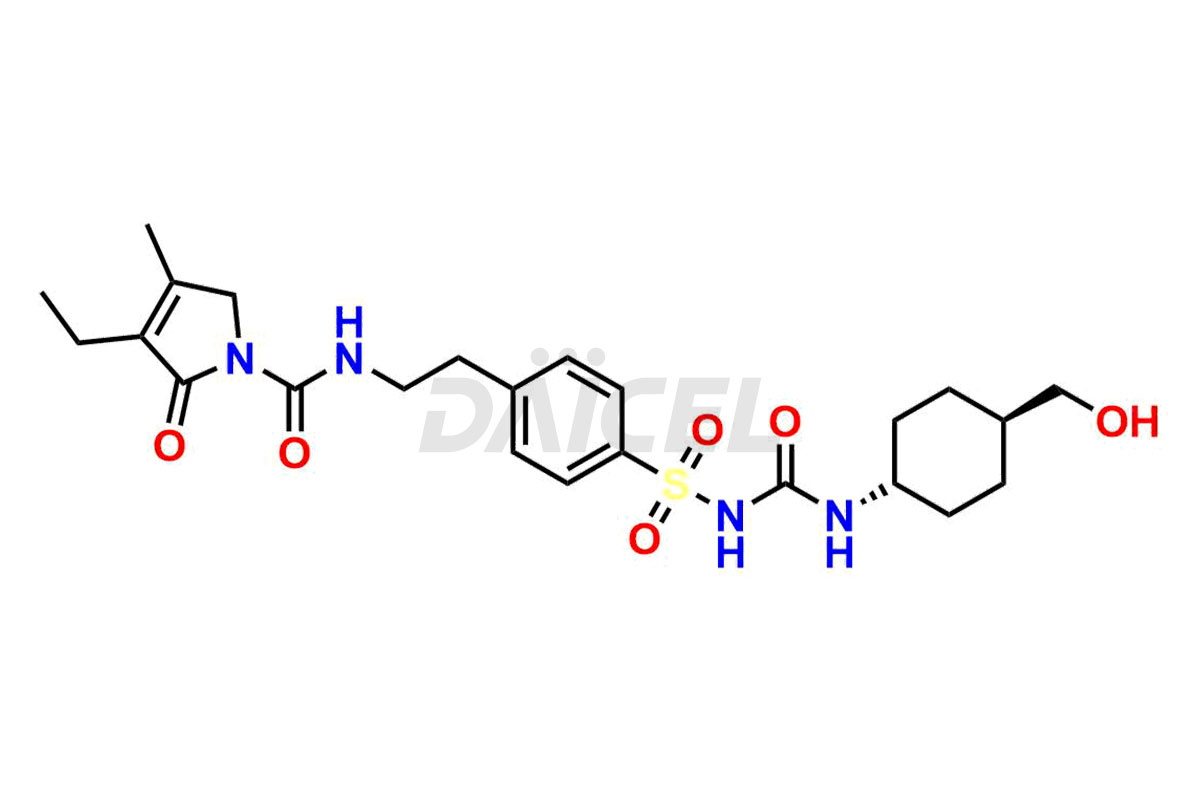
Daicel Pharma propose des options de livraison dans le monde entier pour une synthèse personnalisée des impuretés du glimépiride, y compris des impuretés telles que l'isomère Cis du MCI-glimépiride, le cyclohexyl carboxyl glimépiride et le trans-hydroxy glimépiride. Ces impuretés jouent un rôle essentiel dans l’évaluation de la pureté et de l’innocuité du glimépiride, un ingrédient pharmaceutique actif.
Glimépiride [CAS : 93479/97/1] est un médicament sulfonylurée de troisième génération à action prolongée. Il abaisse le taux de sucre dans le sang et stimule la sécrétion d'insuline. Grâce à sa durée d'action prolongée et à ses effets hypoglycémiants, le glimépiride est une option efficace pour gérer le diabète.
Glimépiride : utilisation et disponibilité commerciale
Approuvé par la FDA pour le traitement du diabète sucré de type 2, le glimépiride est un médicament sulfonylurée de deuxième génération. Il améliore le contrôle glycémique chez les adultes. Le glimépiride est utilisé dans les cas où la metformine n'est pas tolérée. Amaryl est la marque sous laquelle le glimépiride est disponible.
Structure et mécanisme d'action du glimépiride 
Le nom chimique du glimépiride est 3-éthyl-4-méthyl-N-(4-(N-((4-méthylcyclohexyl)carbamoyl)sulfamoyl)phénéthyl)-2-oxo-2,5-dihydro-1H-pyrrole-1. -carboxamide. Sa formule chimique est C24H34N4O5S, et son poids moléculaire est d'environ 490.6 g/mol.
Le glimépiride stimule la libération d'insuline par les cellules pancréatiques fonctionnelles.
Impuretés et synthèse du glimépiride
Des impuretés de glimépiride peuvent se former lors de la synthèse1, le stockage ou l'utilisation, résultant de divers facteurs tels que les réactions secondaires et la dégradation. Des méthodes analytiques telles que HPLC, LC-MS, RMN et IR permettent d'analyser et de quantifier ces impuretés. Les mesures de contrôle comprennent l’optimisation des conditions de synthèse, les étapes de purification et la mise en œuvre d’une technologie analytique avancée. Des conditions de stockage et un emballage appropriés sont essentiels pour minimiser la formation d'impuretés pendant le stockage. Les études de stabilité aident à évaluer les profils d'impuretés au fil du temps. Le respect des directives réglementaires garantit la qualité et la sécurité du Glimépiride.
Daicel Pharma adhère strictement aux normes cGMP et exploite une installation d'analyse pour synthétiser les normes d'impuretés du glimépiride. Nous proposons une gamme d'impuretés de glimépiride, telles que l'isomère Cis du MCI-glimépiride, le cyclohexyl carboxyl glimépiride et le trans-hydroxy glimépiride. Nos étalons d'impuretés disposent d'un certificat d'analyse (CoA) détaillé et d'un rapport de caractérisation complet. Le CoA englobe les données obtenues grâce à des techniques, notamment l'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Nous fournissons des données supplémentaires, telles que 13C-DEPT, sur demande. Nous pouvons synthétiser des impuretés ou des produits de dégradation inconnus du glimépiride. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Thennati, Rajamannar ; Rehani, Rajeev Budhdev ; Soni, Rohit Ravikant, Procédé de préparation du trans-3-éthyl-2,5-dihydro-4-méthyl-N-[2-[4-[[[[(4-méthyl cyclohexyl) amino]carbonyl]amino] sulfonyl]phényl]éthyl]-2-oxo-1H-pyrrole-1-carboxamide, Sun Pharmaceutical Industries Limited, Inde, US7132444B2, 7 novembre 2006
- Lehr, KH; Damm, P., Détermination simultanée du sulfonylurée glimépiride et de ses métabolites dans le sérum et l'urine humains par chromatographie liquide haute performance après dérivatisation pré-colonne, Journal of Chromatography, Biomedical Applications, Volume : 526, Numéro : 2, Pages : 497- 505, 1990
Foire aux Questions
Les impuretés du glimépiride sont-elles surveillées dans le temps ?
Oui, les impuretés du glimépiride sont régulièrement surveillées au cours des études de stabilité afin d'évaluer la qualité et la sécurité à long terme du médicament.
Comment sont identifiées les impuretés du Glimépiride ?
Les impuretés du glimépiride sont identifiées en comparant leurs caractéristiques chromatographiques ou spectrales avec celles d'impuretés connues ou d'étalons de référence.
Les impuretés du glimépiride peuvent-elles être éliminées ou réduites ?
Les fabricants s'efforcent de minimiser les impuretés lors de la synthèse et des techniques de purification peuvent être utilisées pour réduire les niveaux d'impuretés.
Comment conserver les impuretés du glimépiride en termes de température ?
Il est recommandé de conserver les impuretés du glimépiride à une température ambiante contrôlée, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.