Fulvestrant
Renseignements généraux
Impuretés du Fulvestrant et Fulvestrant
Daicel Pharma est spécialisée dans la synthèse d'impuretés pour le Fulvestrant, un ingrédient pharmaceutique actif. Nous proposons des impuretés telles que l'AN04035, l'énantiomère Fulvestrant R, l'impureté associée au Fulvestrant et l'énantiomère Fulvestrant S, qui jouent un rôle essentiel dans l'évaluation de la pureté et de la sécurité du Fulvestrant. Daicel Pharma propose également une synthèse personnalisée d'impuretés de Fulvestrant pour répondre aux besoins spécifiques des clients et offrir des options de livraison dans le monde entier.
Fulvestrant [CAS : 129453/61/8] est un antagoniste synthétique des récepteurs des œstrogènes qui traite le cancer du sein métastatique à récepteurs hormonaux positifs. Il s'agit des cas de cancer du sein à récepteurs d'œstrogènes positifs, localement avancés ou métastatiques.
Fulvestrant : utilisation et disponibilité commerciale
Le fulvestrant, vendu sous Faslodex, présente des avantages cliniques principalement chez les femmes ménopausées atteintes d'un cancer du sein HR-positif et HER2-négatif. Le fulvestrant traite le cancer du sein avancé, y compris les cas de tumeurs volumineuses, de métastases ganglionnaires étendues et d'invasion des tissus et organes environnants.
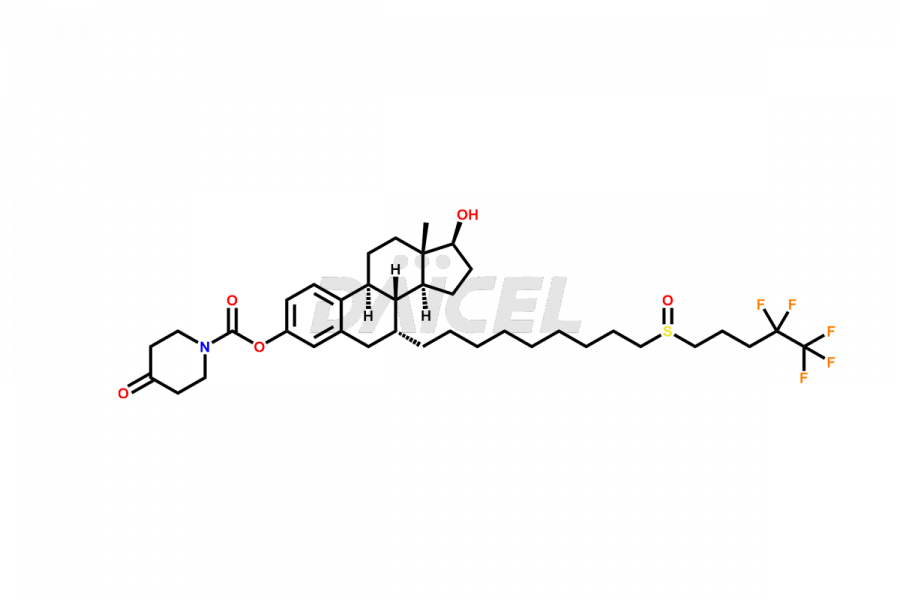
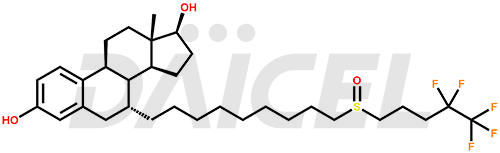
Structure du fulvestrant et mécanisme d'action 
Le nom chimique du Fulvestrant est (7α,17β)-7-[9-[(4,4,5,5,5-pentafluoropentyl)sulfinyl]nonyl]estra-1,3,5(10)-triène-3,17, XNUMX-diol. Sa formule chimique est C32H47F5O3S, et son poids moléculaire est d'environ 606.8 g/mol.
Le fulvestrant se lie aux récepteurs des œstrogènes et régule négativement la protéine ER dans les cellules cancéreuses du sein humain.
Impuretés et synthèse du fulvestrant
Les impuretés contenues dans le Fulvestrant sont des substances involontaires qui peuvent être présentes dans le produit médicamenteux, en dehors de l'ingrédient actif souhaité. Ils peuvent provenir de diverses sources, notamment des matières premières, des processus de synthèse ou de la dégradation du Fulvestrant au fil du temps. Des exemples d'impuretés présentes dans le Fulvestrant peuvent inclure des composés apparentés, des solvants résiduels, des produits de dégradation ou des impuretés introduites lors de la fabrication. Un contrôle et une surveillance efficaces des impuretés contenues dans le Fulvestrant sont essentiels pour garantir la qualité, la sécurité et l'efficacité du médicament.
Daicel Pharma, conformément aux normes cGMP, exploite une installation d'analyse où nous préparons des normes d'impuretés du Fulvestrant telles que AN04035, l'énantiomère Fulvestrant R, l'impureté associée au Fulvestrant et l'énantiomère Fulvestrant S. Nous proposons un certificat d'analyse (CoA) complet pour ces impuretés, fournissant un rapport de caractérisation détaillé. Le CoA comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.1,2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. Nous pouvons synthétiser des impuretés ou des produits de dégradation inconnus du Fulvestrant. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Fazioni, Cristian; Giolito, Andrea, Séparation des isomères du fulvestrant, WO2007044662A2, 19 avril 2007
- Venkata Narasimha Rao, Ganipisetty ; Gnanadev, G. ; Ravi, Bellam; Dhananjaya, D. ; Manoj, P. ; Indu, B. ; Nadh, R. Venkata, Chromatographie de convergence ultra performance basée sur un fluide supercritique (dioxyde de carbone) pour la séparation et la détermination des diastéréomères du fulvestrant, Méthodes analytiques, Volume : 5, Numéro : 18, Pages : 4832-4837, 2013
Foire aux Questions
Les impuretés du Fulvestrant sont-elles surveillées en permanence pendant son processus de fabrication ?
Les impuretés du Fulvestrant sont surveillées en permanence pendant son processus de fabrication. Les mesures de contrôle de la qualité, y compris les tests et analyses en cours de processus, garantissent le contrôle continu des niveaux d'impuretés.
Les impuretés du Fulvestrant peuvent-elles entraîner une variabilité de sa réponse thérapeutique ?
Les impuretés contenues dans le Fulvestrant peuvent potentiellement provoquer une variabilité de sa réponse thérapeutique. Ils peuvent interférer avec le mécanisme d’action du médicament ou modifier sa pharmacocinétique. Leur contrôle strict minimise cette variabilité pour garantir une réponse thérapeutique cohérente.
Existe-t-il des limites ou des seuils spécifiques pour les niveaux d'impuretés dans le Fulvestrant ?
Oui, les autorités réglementaires fournissent des limites ou des seuils spécifiques pour les niveaux d'impuretés dans le Fulvestrant. Ces limites sont établies sur la base de considérations de sécurité et sont incluses dans les directives réglementaires. Les fabricants doivent respecter ces limites pour garantir la qualité et la sécurité du Fulvestrant.
Comment conserver les impuretés du Fulvestrant en termes de température ?
Il est recommandé de conserver les impuretés du Fulvestrant à une température ambiante contrôlée, entre 2 et 8 °C (sensible à la lumière). Cependant, les impuretés du Fulvestrant telles que l'AN04035 sont stockées à -20 °C dans une atmosphère d'azote.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.