Foscarnet
Renseignements généraux
Impuretés du Foscarnet et Foscarnet
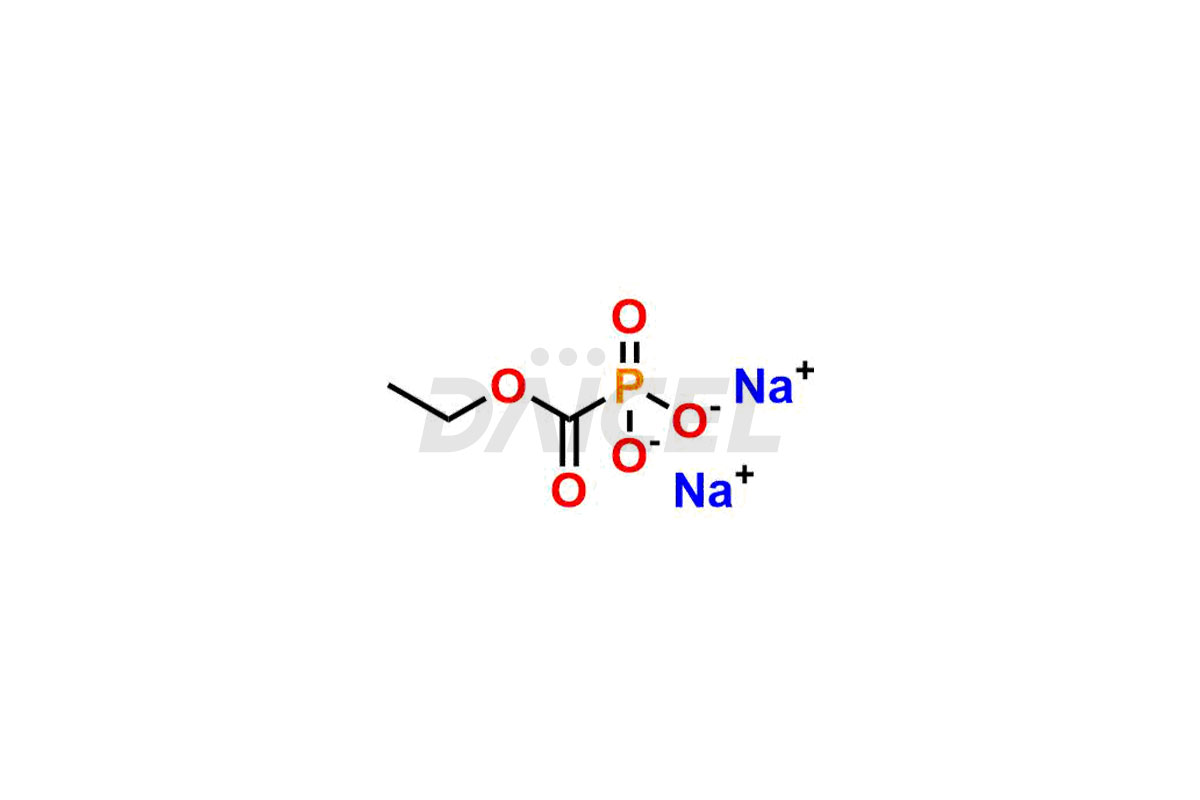
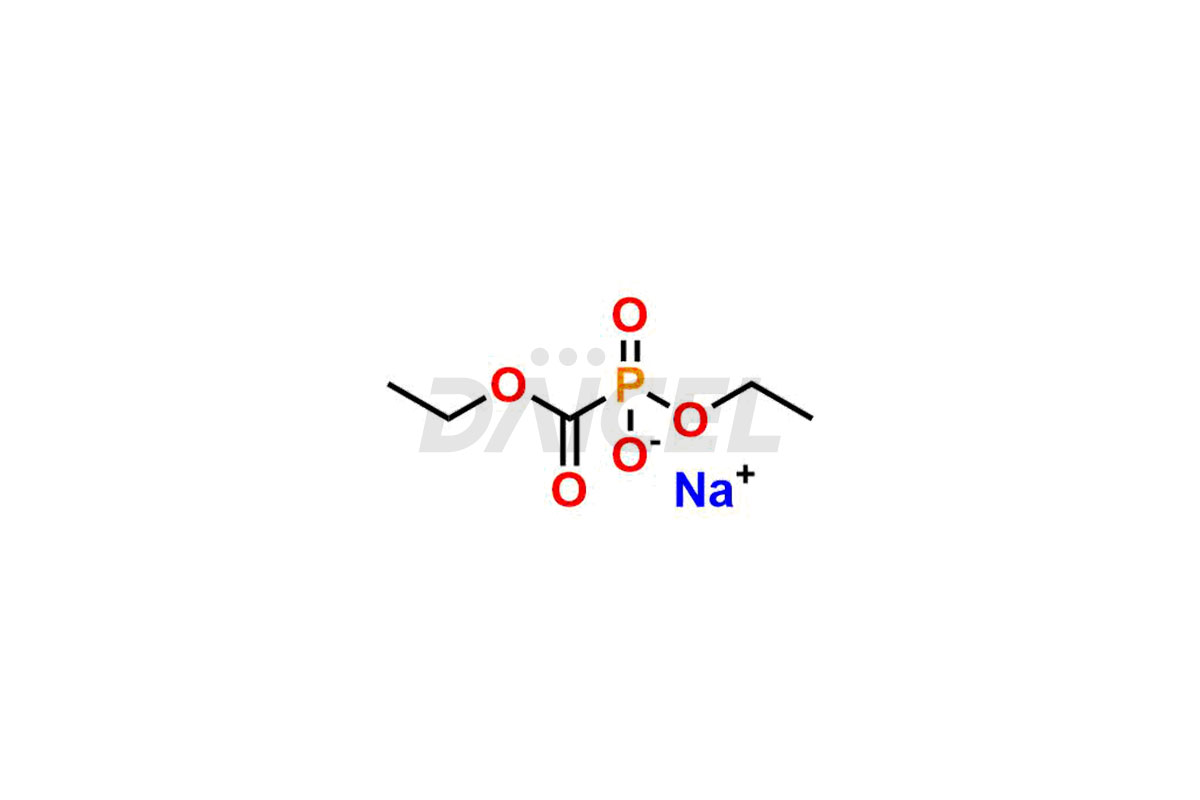
Daicel Pharma est spécialisée dans la synthèse d'impuretés pour le Foscarnet, un ingrédient pharmaceutique actif. Nous proposons des impuretés telles que le composé A associé au Foscarnet, le composé B associé au Foscarnet et le composé C associé au Foscarnet, qui jouent un rôle essentiel dans l'évaluation de la pureté et de la sécurité du Foscarnet. Daicel Pharma propose également une synthèse personnalisée des impuretés Foscarnet pour répondre aux besoins spécifiques des clients et offrir des options de livraison dans le monde entier.
Foscarnet [CAS : 4428/95/9] est un analogue organique synthétique du pyrophosphate inorganique qui présente une activité antivirale contre plusieurs virus. Il traite la rétinite à cytomégalovirus, une infection virale qui affecte la rétine de l'œil. En plus de son efficacité contre le cytomégalovirus, Foscarnet démontre également une activité contre les virus de l'herpès humain et le VIH, ce qui en fait un agent antiviral précieux pour traiter ces infections.
Foscarnet : utilisation et disponibilité commerciale
Foscarnet, commercialisé sous le nom de Foscavir, est un médicament antiviral approuvé par la FDA américaine pour traiter les infections virales. Il traite le cytomégalovirus (CMV) et la rétinite ophtalmique associée au CMV chez les patients atteints du SIDA qui ne tolèrent pas le ganciclovir. Foscarnet traite également les patients immunodéprimés atteints du virus de l'herpès simplex (HSV) qui présentent une résistance à l'acyclovir, le traitement standard contre le HSV. Lorsque le ganciclovir seul s'avère inefficace ou provoque des effets secondaires importants, les cliniciens peuvent opter pour Foscarnet en monothérapie ou en association avec d'autres médicaments.
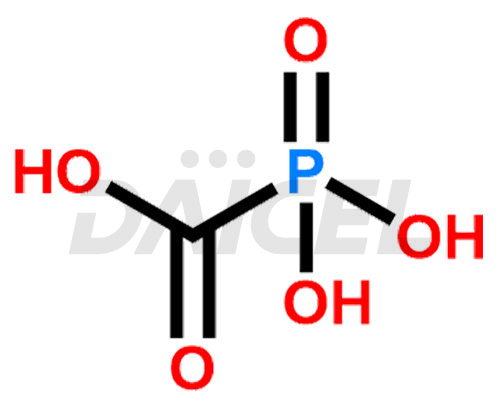
Structure de Foscarnet et mécanisme d'action 
Le nom chimique du Foscarnet est 1,1-oxyde d’acide 1-dihydroxy-phosphinecarboxylique. Sa formule chimique est CH3O5P, et son poids moléculaire est d'environ 126.01 g/mol.
Foscarnet empêche la réplication des virus de l'herpès en inhibant les sites de liaison du pyrophosphate sur les ADN polymérases spécifiques du virus.
Impuretés Foscarnet et synthèse
Les impuretés contenues dans le Foscarnet font référence à des substances indésirables contenues dans le produit médicamenteux qui ne sont pas l'ingrédient pharmaceutique actif (API) prévu. Ils peuvent survenir lors du processus de fabrication ou du stockage du Foscarnet. Les impuretés courantes dans le Foscarnet peuvent inclure des composés apparentés, des produits de dégradation, des solvants résiduels ou des sous-produits de synthèse. Il est crucial de contrôler et de surveiller les impuretés du Foscarnet pour garantir la sécurité, l'efficacité et la qualité du médicament.
Daicel Pharma, conformément aux normes cGMP, exploite une installation d'analyse où nous préparons des normes d'impuretés Foscarnet telles que le composé associé au Foscarnet A, le composé associé au Foscarnet B et le composé associé au Foscarnet C. Nous proposons un certificat d'analyse (CoA) complet pour ces impuretés, fournir un rapport de caractérisation détaillé. Le CoA comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.1,2. Sur demande, nous fournissons des données supplémentaires comme 13C-DEPT. Nous pouvons synthétiser des impuretés Foscarnet inconnues ou des produits de dégradation. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Pettersson, KJ; Nordgren, T. ; Westerlund, D., Détermination du phosphonoformate (Foscarnet) dans les fluides biologiques par chromatographie liquide en phase inverse par paires d'ions, Journal of Chromatography, Biomedical Applications, Volume : 488, Numéro : 2, Pages : 447-55, 1989
- García, Javier; Marquez, Apolonia; Ruiz, Rosa ; López, Luis F. ; Claro, Carmen ; Lucero, Maria Jesus, Détermination du foscarnet (phosphonoformate trisodique) dans les préparations pharmaceutiques par chromatographie liquide haute performance avec détection ultraviolette, Chromatographie biomédicale, Volume : 20, Numéro : 10, Pages : 1024-1027, 2006
Foire aux Questions
Les impuretés du Foscarnet peuvent-elles avoir un impact sur la stabilité du médicament ?
Oui, les impuretés présentes dans le Foscarnet peuvent potentiellement affecter sa stabilité. Certains d’entre eux peuvent contribuer à des réactions de dégradation pouvant compromettre la stabilité et la durée de conservation du médicament. Il est donc nécessaire de les contrôler pour assurer la stabilité à long terme du Foscarnet.
Existe-t-il des tests spécifiques effectués pour évaluer les impuretés Foscarnet ?
Des tests et des méthodes spécifiques sont utilisés pour évaluer les impuretés du Foscarnet lors des tests de contrôle qualité. Ils peuvent inclure l'analyse de substances associées, des tests de solvants résiduels, une évaluation des produits de dégradation, etc. Ces tests permettent de garantir que les niveaux d'impuretés se situent dans des limites acceptables.
Quel solvant aide à analyser les impuretés du Foscarnet ?
L'eau est le solvant utilisé lors de l'analyse de nombreuses impuretés dans le Foscarnet.
Comment stocker les impuretés du Foscarnet en termes de température ?
Il est recommandé de conserver les impuretés du Foscarnet à une température ambiante contrôlée, entre 2 et 8 ⁰C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.