Charger plus
Vous avez vu 9 sur 12 articles
Daicel Pharma est spécialisée dans la synthèse d'impuretés pour la fluphénazine, un ingrédient pharmaceutique actif. Nous proposons des impuretés telles que Fluphénazine Impureté-C, Fluphénazine Impureté-D, 7-Hydroxy Fluphénazine, 7-Bromo fluphénazine, Fluphénazine EP Impureté-A, Fluphénazine Impureté-B, etc., qui jouent un rôle essentiel dans l'évaluation de la pureté, et la sécurité de la fluphénazine. Daicel Pharma propose également une synthèse personnalisée des impuretés de fluphénazine pour répondre aux besoins spécifiques des clients et offrir des options de livraison dans le monde entier.
Fluphénazine [CAS : 69/23/8] est un antipsychotique phénothiazine doté de propriétés antagonistes dopaminergiques. Il bloque les récepteurs postsynaptiques de la dopamine D2 et réduit les hallucinations associées à la schizophrénie. Ses utilisations sont similaires à celles de la chlorpromazine.
La fluphénazine, disponible sous diverses marques telles que Permitil, Prolixin, Prolixin Decanoate et Prolixin Enanthate, est un antipsychotique de première génération principalement utilisé pour gérer les symptômes de psychose chez les personnes atteintes de schizophrénie. Il est particulièrement bénéfique pour les patients qui ont des difficultés à tolérer les médicaments oraux ou lorsque l’observance des médicaments devient une préoccupation pour les prestataires de soins de santé.
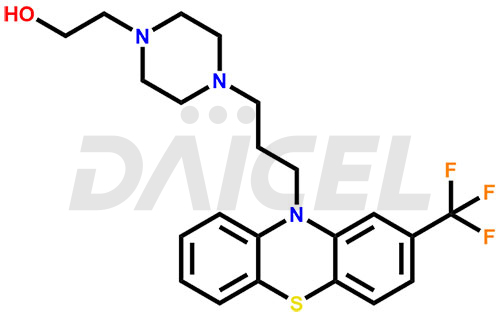
Le nom chimique de la fluphénazine est 4-[3-[2-(Trifluorométhyl)-10H-phénothiazine-10-yl]propyl]-1-pipérazineéthanol. Sa formule chimique est C22H26F3N3OS, et son poids moléculaire est d’environ 437.5 g/mol.
La fluphénazine bloque les récepteurs de la dopamine dans le système limbique, le système cortical et les noyaux gris centraux.
La fluphénazine est un médicament antipsychotique phénothiazine qui peut contenir des impuretés. Ils peuvent survenir pendant le processus de fabrication1 ou des conditions de stockage. Les impuretés courantes de la fluphénazine comprennent des composés apparentés ou des produits de dégradation. Ils peuvent avoir un impact sur la stabilité, l’efficacité et la sécurité du médicament. Par conséquent, les fabricants de produits pharmaceutiques doivent surveiller et contrôler les niveaux d’impuretés pour garantir la qualité des produits Fluphénazine.
Daicel Pharma, conformément aux normes cGMP, exploite une installation d'analyse où nous préparons des étalons d'impuretés de fluphénazine telles que Fluphénazine Impureté-C, Fluphénazine Impureté-D, 7-Hydroxy Fluphénazine, 7-Bromo fluphénazine, Fluphénazine EP Impureté-A, Fluphénazine Impureté-B. , et ainsi de suite. Nous proposons un certificat d'analyse (CoA) complet pour ces impuretés, fournissant un rapport de caractérisation détaillé. Le CoA comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires telles que 13C-DEPT. Nous pouvons synthétiser des impuretés inconnues de la fluphénazine, des produits de dégradation et des composés marqués pour évaluer l'efficacité de la fluphénazine générique. Pour la recherche bioanalytique, y compris les études BA/BE, nous proposons le chlorhydrate de Fluphénazine-D6, un composé de fluphénazine marqué deutéré. Chaque livraison dispose d'un rapport de caractérisation complet.
Les fabricants pharmaceutiques de fluphénazine mettent en œuvre des mesures de contrôle de qualité rigoureuses pour surveiller et contrôler les niveaux d’impuretés. Ces mesures comprennent l'utilisation de processus de fabrication appropriés, la réalisation de tests et d'analyses approfondis et le respect des directives et spécifications réglementaires concernant les limites d'impuretés.
Les impuretés contenues dans la fluphénazine peuvent provenir de diverses sources, notamment des matières premières, des réactifs lors de la synthèse, de la dégradation de l'API au fil du temps ou des sous-produits formés au cours du processus de fabrication. Les fabricants doivent identifier et traiter ces sources potentielles pour maintenir la pureté de la fluphénazine.
Les impuretés contenues dans la fluphénazine sont régulièrement testées et surveillées tout au long du processus de fabrication et de la durée de conservation du produit. Les fabricants effectuent des analyses de routine et des études de stabilité pour évaluer les niveaux d'impuretés et garantir la conformité aux exigences réglementaires. Ces tests aident à maintenir la qualité et l’intégrité de la fluphénazine.
Il est recommandé de conserver les impuretés de fluphénazine à une température ambiante contrôlée, entre 2 et 8 °C.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.