Fésotérodine
Renseignements généraux
Impuretés de fésotérodine et fésotérodine
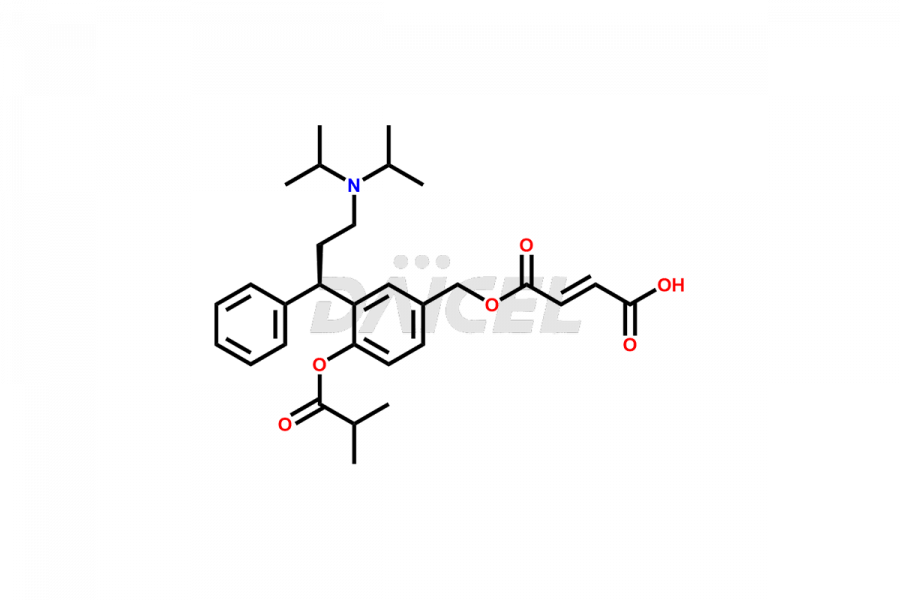
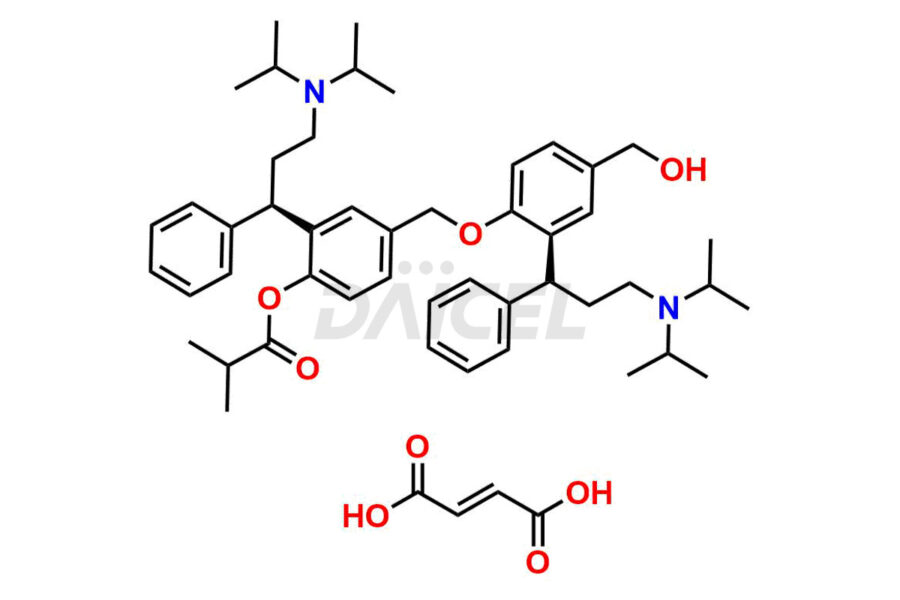
Daicel Pharma est spécialisée dans la synthèse d'impuretés pour la fésotérodine, un ingrédient pharmaceutique actif. Nous proposons des impuretés cruciales de fésotérodine telles que le fumarate de dimère de fésotérodine, le monoester de dimère de fésotérodine et l'impureté P de fésotérodine, qui jouent un rôle essentiel dans l'évaluation de la pureté et de la sécurité de la fésotérodine. Daicel Pharma propose également une synthèse personnalisée d'impuretés de fésotérodine pour répondre aux besoins spécifiques des clients, et nous proposons des options de livraison dans le monde entier.
En tant que médicament pour traiter l'incontinence urinaire et le syndrome de la vessie hyperactive, la fésotérodine [CAS : 286930/02/7] possède des propriétés relaxantes musculaires et antispasmodiques urinaires. Il fonctionne comme un antagoniste compétitif des récepteurs muscariniques et un agent anticholinergique et antispasmodique.
Fésotérodine : utilisation et disponibilité commerciale
La fésotérodine, vendue sous la marque Toviaz, est destinée aux adultes présentant des symptômes d'hyperactivité vésicale, tels que l'incontinence urinaire, l'urgence et la fréquence urinaire. Cela évite également un manque soudain de contrôle sur la miction chez les patients.
Structure de la fésotérodine et mécanisme d'action 
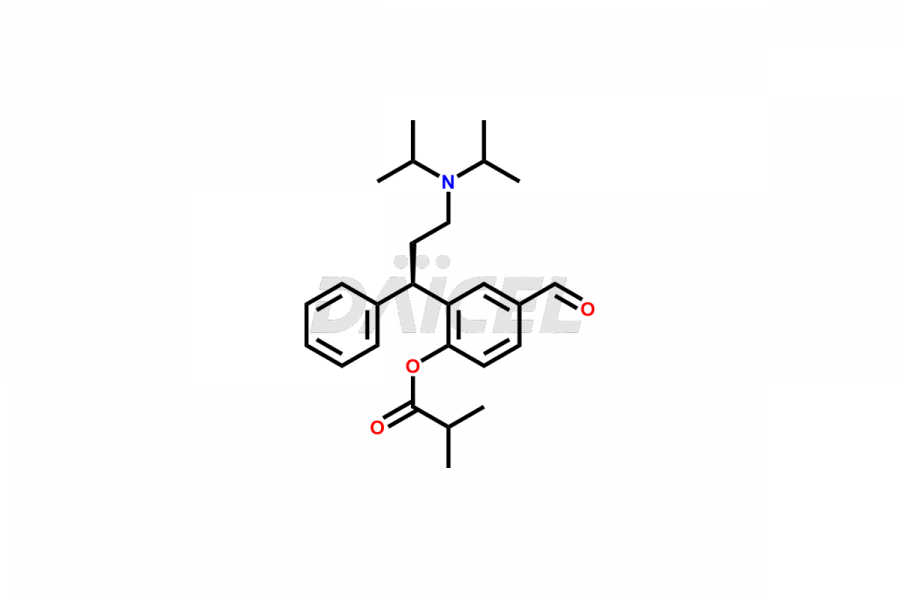
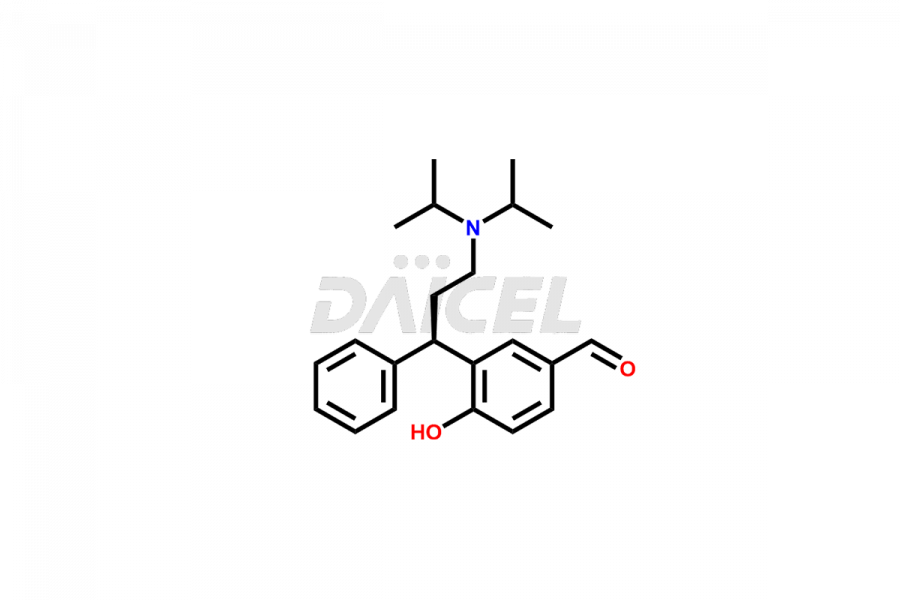
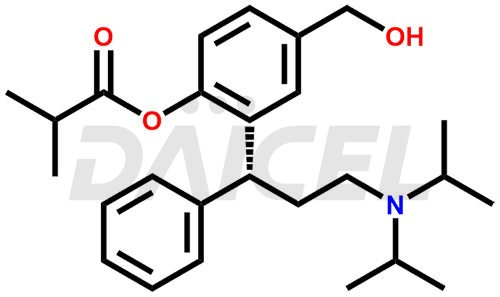
Le nom chimique de la fésotérodine est le (R)-2-(3-Diisopropylamino-1-phénylpropyl)-4-hydroxyméthylphénylisobutyrate. Sa formule chimique est C26H37NON3, et son poids moléculaire est d'environ 411.6 g/mol.
La fésotérodine hydrolyse son métabolite actif, la 5-hydroxyméthyl toltérodine, qui empêche les contractions de la vessie provoquées par l'acétylcholine. Il détend les muscles lisses de la vessie et réduit la perte involontaire d'urine.
Impuretés et synthèse de la fésotérodine
Les impuretés contenues dans la fésotérodine font référence à des substances involontaires qui peuvent être présentes aux côtés de l'ingrédient pharmaceutique actif. Ils peuvent survenir pendant le processus de fabrication1, le stockage ou en raison d'interactions avec d'autres composants. Des méthodes analytiques comme la chromatographie et la spectroscopie permettent d'identifier et de quantifier ces impuretés. Des mesures strictes de contrôle de qualité pendant la production aident à minimiser la formation d’impuretés et à garantir la sécurité et l’efficacité du produit. Les directives réglementaires fournissent des limites et des spécifications pour les niveaux acceptables d'impuretés dans la fésotérodine. Une surveillance et une analyse continues aident à maintenir la qualité et la pureté de la fésotérodine, garantissant ainsi son efficacité en tant que médicament.
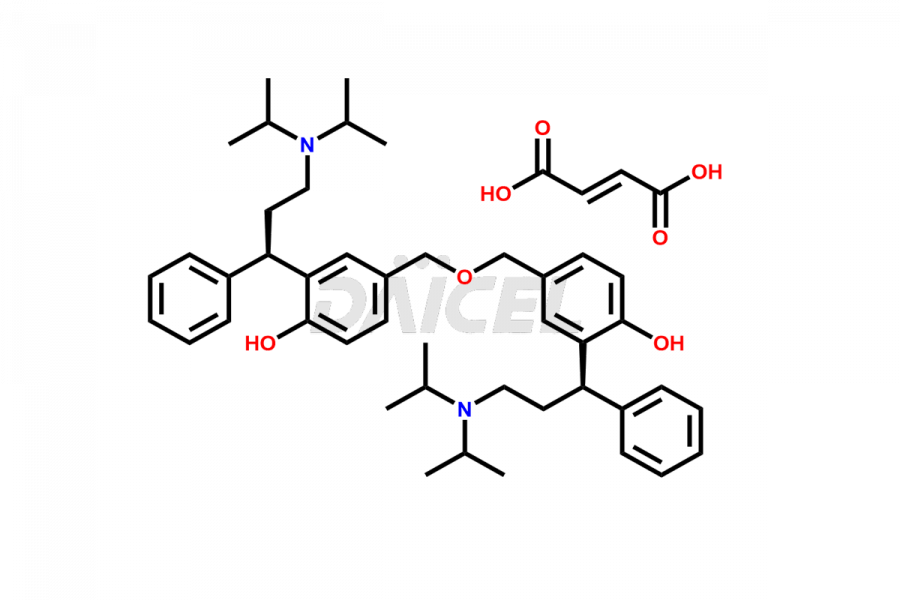
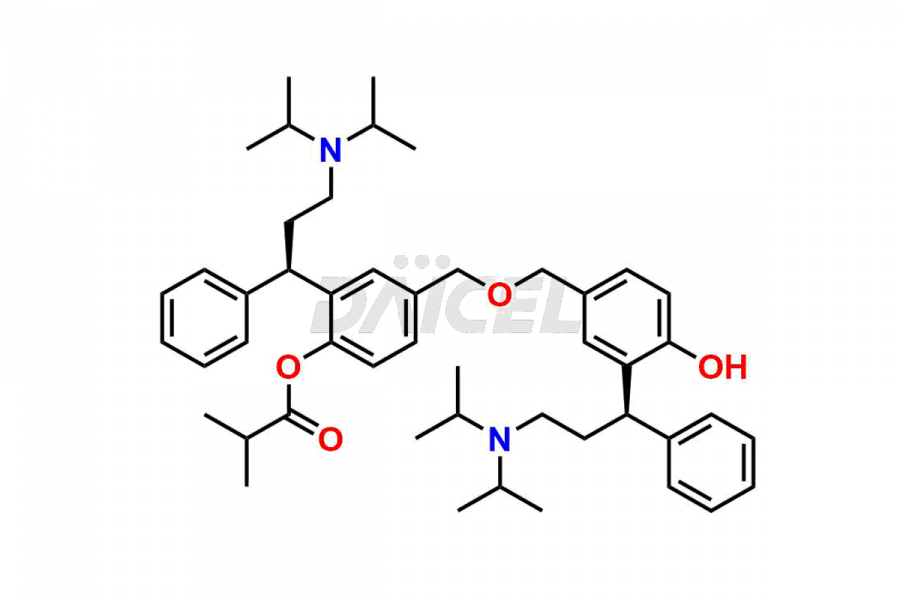
Daicel Pharma, conformément aux normes cGMP, exploite une installation d'analyse où nous préparons des étalons d'impuretés de fésotérodine comme le fumarate de diol diol de fésotérodine, le monoester de dimère de fésotérodine et l'impureté P de fésotérodine. Nous proposons un certificat d'analyse (CoA) complet pour ces impuretés, fournissant un rapport de caractérisation détaillé. Le CoA comprend des données obtenues grâce à des techniques d'analyse de pureté 1H RMN, 13C RMN, IR, MASS et HPLC.2. Sur demande, nous fournissons des données supplémentaires telles que 13C-DEPT. Nous pouvons synthétiser des impuretés ou des produits de dégradation inconnus de la fésotérodine. Chaque livraison est accompagnée d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Meese, Claus, Sels stables de nouveaux dérivés de 3,3-diphénylpropylamines, Schwarz Pharma A.-G., Allemagne, EP1230209B1, 12 janvier 2005
- Sangoi, Maximiliano S. ; Steppe, Martin, Détermination de la fésotérodine dans les formulations pharmaceutiques en utilisant la spectrométrie de masse par chromatographie liquide-tandem, European Journal of Mass Spectrometry, Volume : 16, Numéro : 6, Pages : 653-661, 2010
Foire aux Questions
Comment les impuretés sont-elles contrôlées lors de la fabrication de la Fesoterodine ?
Des mesures strictes de contrôle de qualité, y compris le respect des bonnes pratiques de fabrication (BPF), sont mises en œuvre pendant le processus de fabrication de la fésotérodine pour minimiser la formation d'impuretés et garantir la qualité et la sécurité du produit.
À quelle fréquence les formulations de fésotérodine sont-elles testées pour détecter les impuretés ?
Les formulations de fésotérodine sont soumises à des tests réguliers tout au long du processus de fabrication et lors des études de stabilité pour surveiller les niveaux d'impuretés et garantir la conformité aux exigences réglementaires.
Quels sont les risques potentiels liés à des niveaux élevés d’impuretés de fésotérodine ?
Les niveaux élevés d'impuretés de fésotérodine peuvent présenter des risques tels qu'une efficacité réduite du médicament, une toxicité accrue, des effets indésirables potentiels et une sécurité compromise des patients.
Comment les impuretés de fésotérodine doivent-elles être stockées en termes de température ?
Pour un stockage approprié des impuretés de fésotérodine, il est conseillé de les conserver à une température ambiante contrôlée, comprise entre 2 et 8 °C. Cependant, le stockage d'impuretés spécifiques comme l'impureté P de fésotérodine doit se faire à des températures inférieures à -20 °C, comme indiqué dans le certificat d'analyse (COA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.