Favipiravir
Renseignements généraux
Impuretés du favipiravir et favipiravir
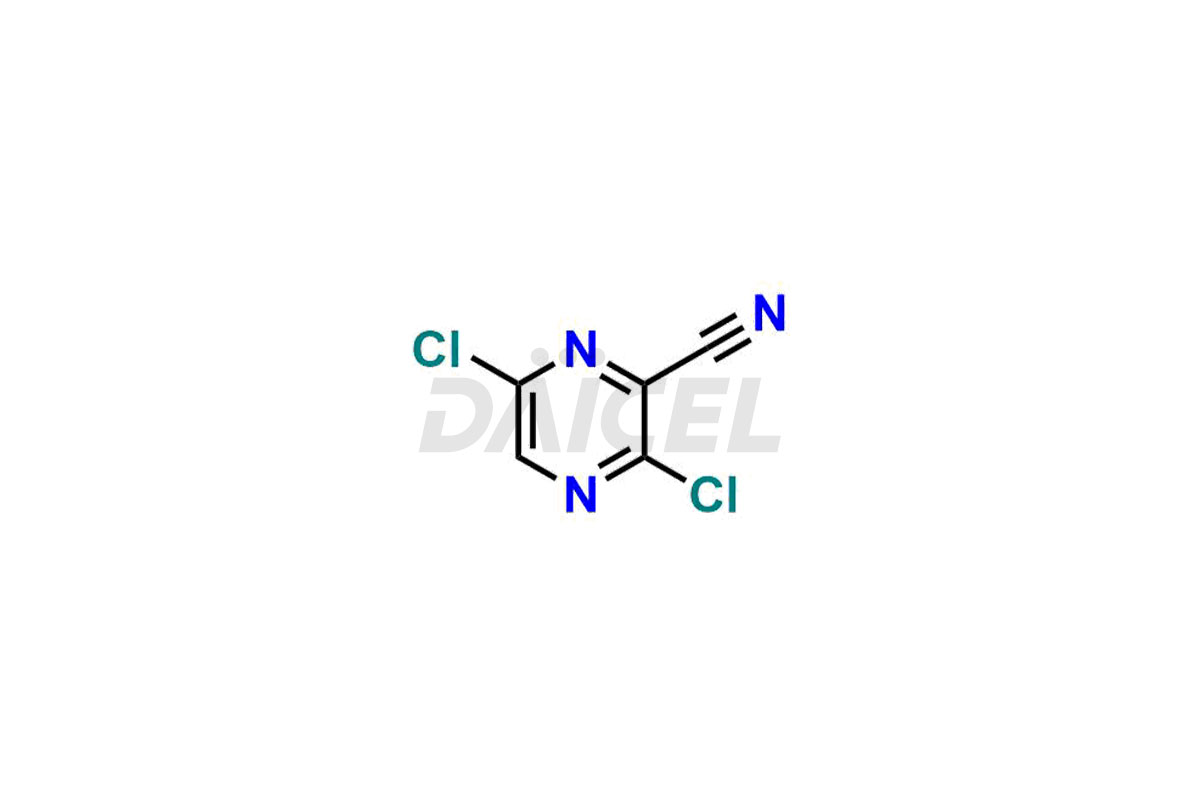
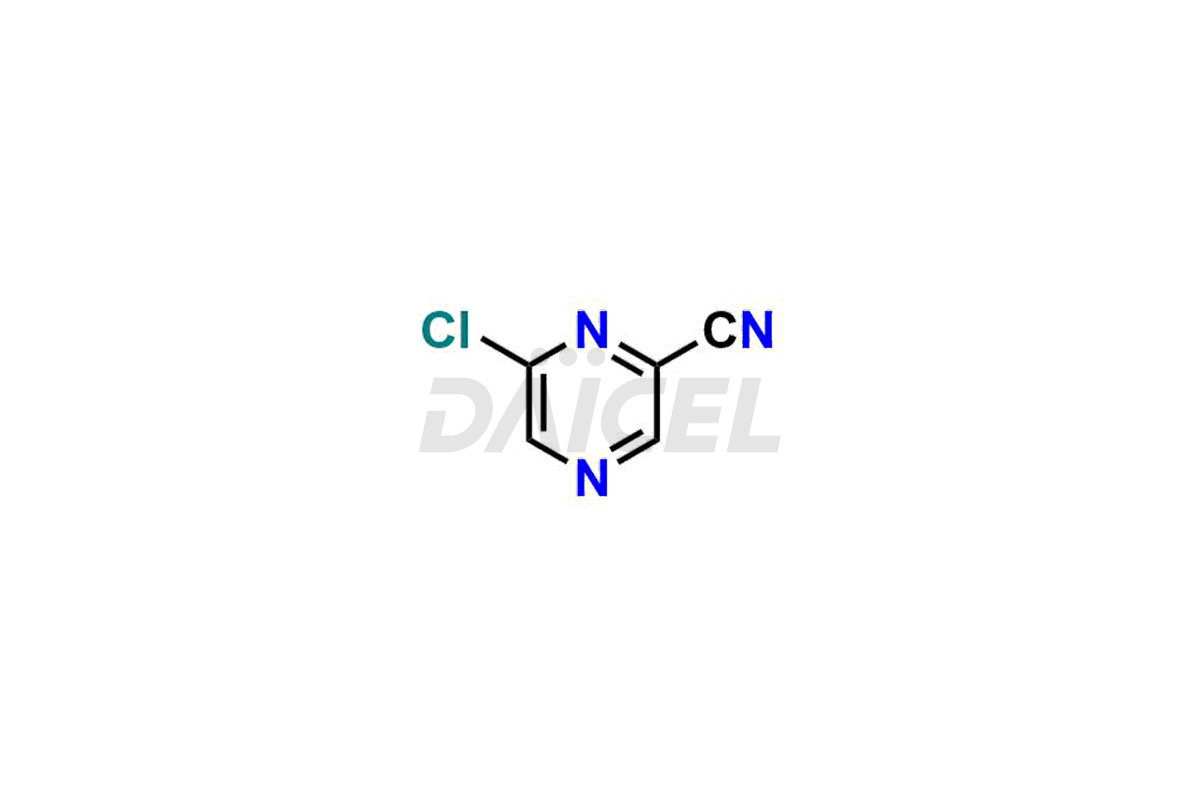
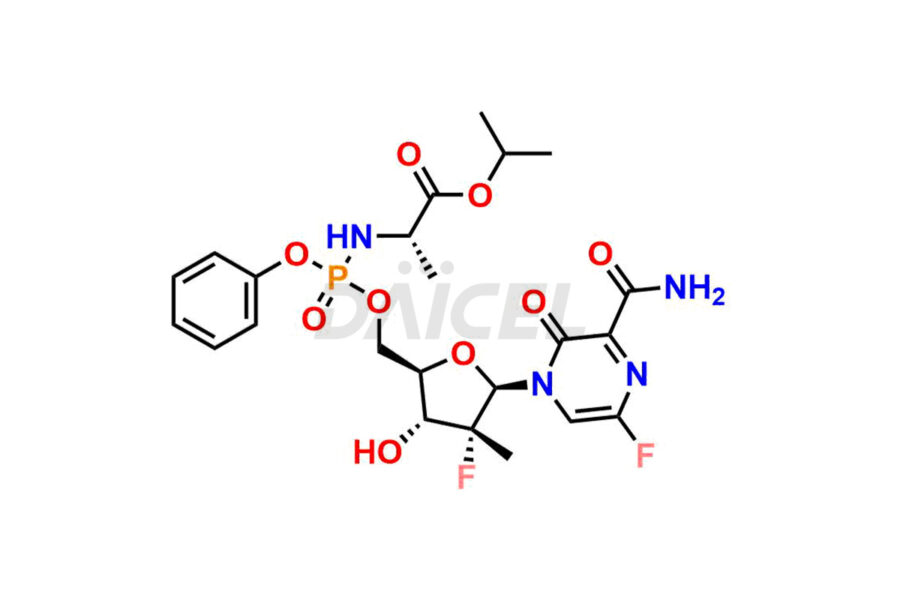
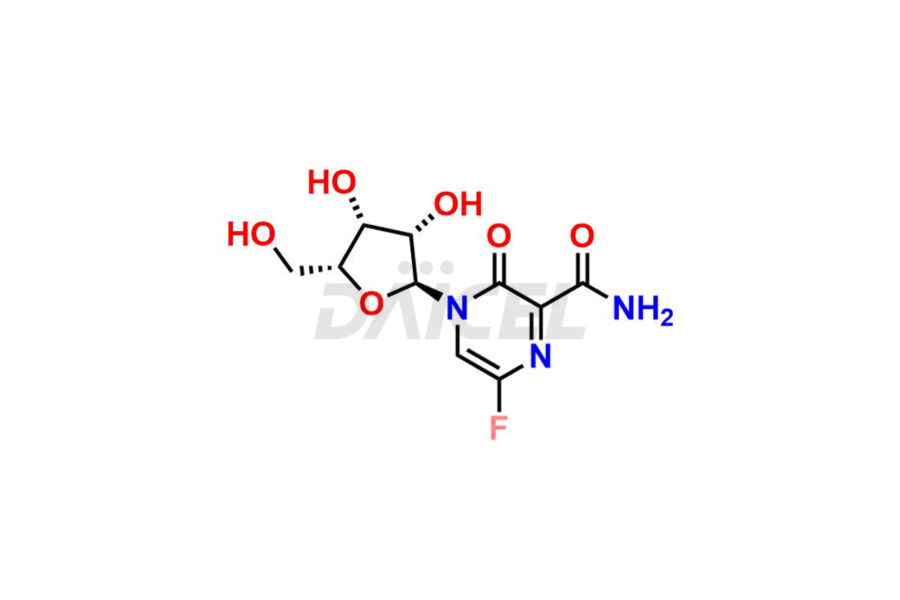
Daicel Pharma propose des impuretés de haute qualité pour le Favipiravir, un ingrédient pharmaceutique actif. Ces impuretés, notamment le 3-hydroxypyrazine-2-carboxamide, le 3,6-dichloropyrazine-2-carbonitrile, le 6-bromo-3-hydroxypyrazine-2-carboxamide, le 6-Chloro-3-hydroxypyrazine-2-carboxamide, le 6-Chloroypyrazine- Le 2-carbonitrile, le Favipiravir fluoro Ribofuranose, le Favipiravir Ribofuranose et le métabolite Favipiravir Ribofuranose jouent un rôle essentiel dans l'évaluation de la pureté, de la fiabilité et de l'innocuité du Favipiravir. Daicel Pharma propose également une synthèse personnalisée des impuretés du Favipiravir pour répondre aux exigences des clients, avec des options de livraison disponibles dans le monde entier.
Favipiravir [CAS : 259793/96/9] est un médicament antiviral qui est un dérivé de la pyrazine carboxamide. Il présente une activité contre les virus à ARN en inhibant sélectivement l'ARN polymérase ARN-dépendante des virus à ARN. Le favipiravir traite la grippe et est un agent antiviral et un inhibiteur de l'ARN polymérase dirigé par l'ARN. De plus, cela aide également à lutter contre les coronavirus.
Favipiravir : utilisation et disponibilité commerciale
Le favipiravir, connu sous le nom de marque Avigan, a été initialement approuvé au Japon en 2014 pour traiter les cas de grippe qui ne répondaient pas aux thérapies conventionnelles. Son efficacité dans le ciblage de diverses souches de grippe a incité à enquêter sur son utilisation potentielle contre d’autres infections virales, notamment Ebola et COVID-19. Le favipiravir agit comme un analogue de la purine, remplaçant la guanine ou l'adénine lors de la réplication virale, entravant ainsi le processus de réplication. Il peut traiter des infections potentiellement mortelles telles qu’Ebola, la fièvre de Lassa et la rage, établissant ainsi sa valeur thérapeutique dans ces maladies.
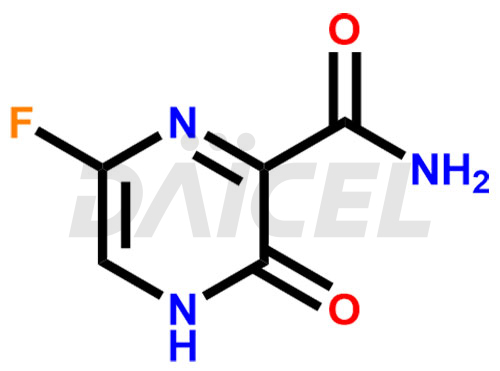
Structure et mécanisme d'action du favipiravir 
Le nom chimique du Favipiravir est 6-Fluoro-3,4-dihydro-3-oxo-2-pyrazinecarboxamide. Sa formule chimique est C5H4FN3O2, et son poids moléculaire est d'environ 157.10 g/mol.
Le favipiravir inhibe sélectivement l'ARN polymérase ARN-dépendante du virus de la grippe.
Impuretés et synthèse du favipiravir
Les impuretés contenues dans le Favipiravir font référence à des substances ou sous-produits inattendus présents dans le médicament. Ils peuvent survenir lors de la synthèse1, les processus de fabrication ou de stockage. Ils englobent les composés associés, les produits de dégradation, les solvants résiduels ou autres impuretés introduites lors de la production ou de la manipulation. Ils peuvent avoir un impact sur la pureté, la stabilité et la qualité globale du Favipiravir. Des directives réglementaires strictes et des mesures de contrôle de qualité aident à surveiller et à contrôler les niveaux d'impuretés afin de garantir la sécurité et l'efficacité des médicaments Favipiravir. Il est essentiel de les minimiser et de les gérer pour maintenir l’intégrité et la valeur thérapeutique du Favipiravir.
Daicel Pharma propose un certificat d'analyse (CoA) complet pour les normes d'impuretés du Favipiravir, notamment le 3-hydroxypyrazine-2-carboxamide, le 3,6-dichloropyrazine-2-carbonitrile, le 6-bromo-3-hydroxypyrazine-2-carboxamide, le 6-Chloro. -3-hydroxypyrazine-2-carboxamide, 6-Chloroypyrazine-2-carbonitrile, Favipiravir fluoro Ribofuranose, Favipiravir Ribofuranose et métabolite Favipiravir Ribofuranose. Ils sont générés à partir d’une installation d’analyse conforme aux normes cGMP. Le CoA fournit un rapport de caractérisation détaillé avec des données obtenues grâce à des techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et l'analyse de pureté HPLC.2. Nous fournissons des données supplémentaires comme 13C-DEPT sur demande. Daicel Pharma synthétise des impuretés ou des produits de dégradation inconnus du Favipiravir. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Furuta, Yousuke ; Egawa, Hiroyuki, Dérivés de carboxamide hétérocycliques azotés ou sels de ceux-ci comme agents antiviraux, Toyama Chemical Co., Ltd., Japon, EP1112743B1, 24 octobre 2007 (https://patents.google.com/patent/EP1112743B1/en)
- Bulduk, Ibrahim, Méthode HPLC-UV pour la quantification du favipiravir dans les formulations pharmaceutiques, Acta Chromatographica, Volume : 33, Numéro : 3, Pages : 209-215, 2021
Foire aux Questions
Comment les impuretés du favipiravir dans les formulations médicamenteuses sont-elles caractérisées ?
Diverses techniques de caractérisation physicochimique, telles que la détermination du point de fusion, les études de solubilité et l'analyse spectroscopique, aident à caractériser les impuretés contenues dans les formulations de Favipiravir.
Les impuretés du favipiravir dans les formulations médicamenteuses peuvent-elles entraîner des modifications des effets pharmacodynamiques du médicament ?
Certaines impuretés contenues dans les formulations de Favipiravir peuvent altérer les effets pharmacodynamiques du médicament, affectant ainsi son mécanisme d'action ou ses résultats thérapeutiques.
Comment les impuretés du Favipiravir sont-elles contrôlées pendant le stockage et le transport ?
Des conditions de stockage appropriées, telles que le contrôle de la température et de l'humidité, ainsi que des matériaux d'emballage appropriés contribuent à minimiser la formation ou la dégradation d'impuretés dans le Favipiravir pendant le stockage et le transport.
Comment conserver les impuretés du Favipiravir en termes de température ?
Les impuretés du favipiravir sont conservées à une température ambiante contrôlée, entre 2 et 8 °C, ou conformément aux spécifications du certificat d'analyse (CoA).
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.