Doxazosine
Renseignements généraux
Impuretés de doxazosine et doxazosine
Daicel Pharma se spécialise dans l'offre d'impuretés de haute qualité pour la doxazosine, un ingrédient pharmaceutique actif. L'impureté, le composé associé au mésylate de doxazosine, joue un rôle essentiel dans l'évaluation de la pureté, de la fiabilité et de la sécurité de la doxazosine. Daicel Pharma propose également une synthèse personnalisée d'impuretés de doxazosine pour répondre aux exigences des clients, avec des options de livraison disponibles dans le monde entier.
Doxazosine [CAS : 74191/85/8] présente des propriétés antihypertensives et antinéoplasiques. Le composé quinazoline inhibe sélectivement les récepteurs adrénergiques alpha-1. Il traite l'hypertension et l'hypertrophie bénigne de la prostate comme un alpha-bloquant non sélectif.
Doxazosine : utilisation et disponibilité commerciale
La doxazosine est un médicament qui offre des avantages thérapeutiques pour plusieurs affections. Dérivé de la quinazoline, il fonctionne comme un antagoniste alpha1 compétitif. Il gère l'hyperplasie bénigne de la prostate, les calculs urétéraux et l'hypertension. Les symptômes associés à l'hypertrophie bénigne de la prostate, notamment la fréquence urinaire, l'urgence et la nycturie, sont soulagés par la doxazosine. Il peut être prescrit seul pour contrôler l’hypertension ou avec d’autres agents antihypertenseurs. La doxazosine est disponible sous les marques Cardura et Cardura XL.
Structure et mécanisme d'action de la doxazosine 
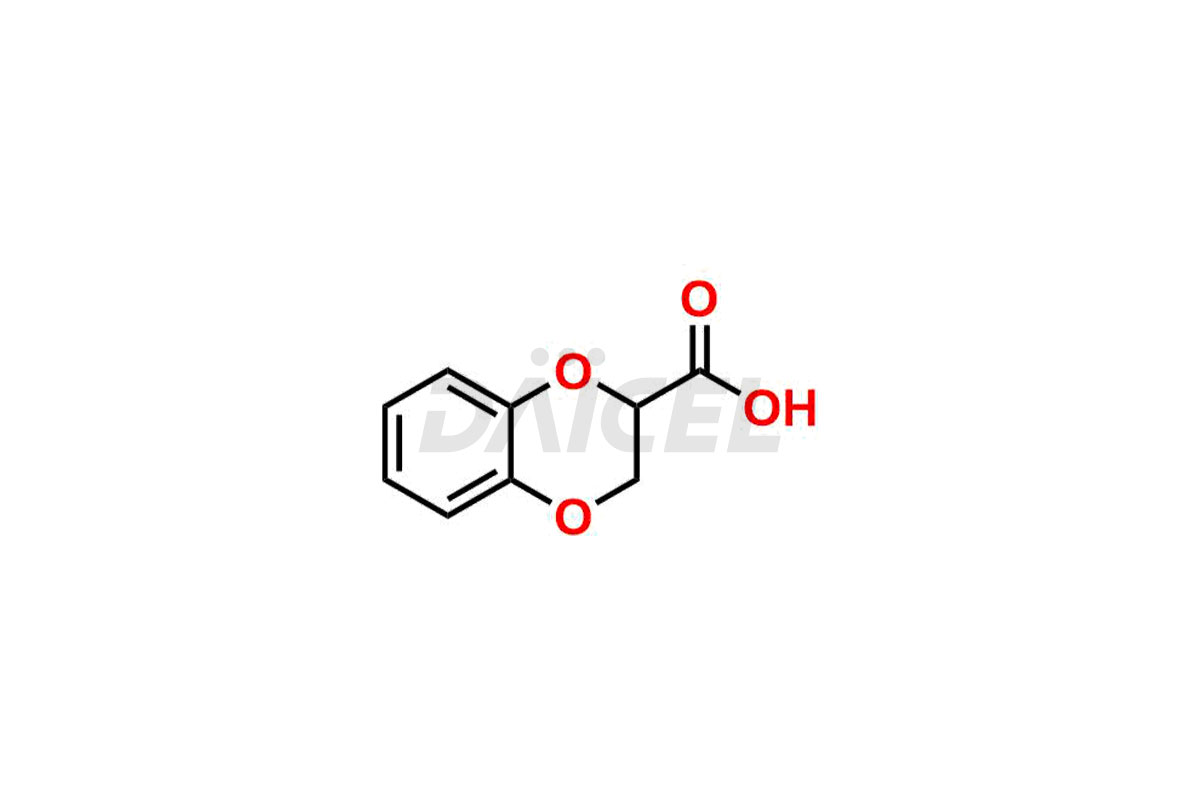
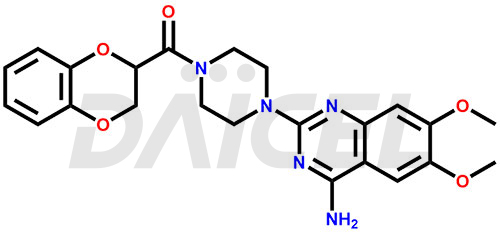
Le nom chimique de la doxazosine est [4-(4-Amino-6,7-diméthoxy-2-quinazolinyl)-1-pipérazinyl](2,3-dihydro-1,4-benzodioxin-2-yl)méthanone. Sa formule chimique est C23H25N5O5, et son poids moléculaire est d'environ 451.5 g/mol.
La doxazosine s'oppose de manière compétitive aux effets vasopresseurs de la phényléphrine, un agoniste alpha1. Il s'oppose également à l'effet vasopresseur systolique de la noradrénaline.
Impuretés et synthèse de la doxazosine
Les impuretés de doxazosine font référence aux sous-produits ou substances apparentées qui peuvent être présents dans le médicament doxazosine. La synthèse des impuretés de Doxazosine implique la préparation de ces composés involontaires au cours du processus de fabrication1. L'analyse et le contrôle des impuretés de la doxazosine sont cruciaux pour garantir la qualité, la sécurité et l'efficacité du médicament. Diverses techniques analytiques, comme la chromatographie liquide haute performance (HPLC), permettent d'identifier et de quantifier ces impuretés. Des mesures strictes de contrôle de qualité aident à limiter la présence d'impuretés de doxazosine dans des limites acceptables, en respectant les directives réglementaires et en garantissant la pureté de la doxazosine.
Daicel Pharma propose un certificat d'analyse (CoA) complet pour l'étalon d'impuretés de doxazosine, tel que le composé associé au mésylate de doxazosine. Ils sont générés à partir d’une installation d’analyse conforme aux normes cGMP. Le CoA fournit un rapport de caractérisation détaillé avec des données obtenues grâce à des techniques telles que la RMN 1H, la RMN 13C, l'IR, la MASS et la pureté HPLC.2 analyse. Nous fournissons des données supplémentaires comme 13C-DEPT sur demande. Daicel Pharma synthétise des impuretés ou des produits de dégradation inconnus de la doxazosine, ainsi que des composés marqués, pour évaluer l'efficacité de la doxazosine générique. En outre, la Doxazosine-D8, un étalon de doxazosine marquée au deutérium, est disponible pour la recherche bioanalytique, y compris les études BA/BE. Chaque livraison dispose d'un rapport de caractérisation complet.
Bibliographie
FAQ
Bibliographie
- Campbell, Simon Fraser, Antihypertensive 4-amino-2-[4-(1,4-benzodioxan-2-carbonyl) pipérazin-1-yl ou homopipérazin-1-yl]quinazolines, Pfizer Corp., Panama, US4188390A, 12 février , 1980
- Cowlishaw, MG ; Sharman, JR, Détermination de la doxazosine par chromatographie liquide haute performance utilisant la détection par fluorescence, Journal of Chromatography, Biomedical Applications, Volume : 344, Pages : 403-7, 1985
Foire aux Questions
Quelles sont les sources potentielles d’impuretés contenues dans la doxazosine ?
Les sources potentielles d'impuretés contenues dans la doxazosine comprennent les matières premières, les réactifs, les solvants et les intermédiaires de réaction utilisés dans le processus de fabrication.
Les impuretés de doxazosine peuvent-elles affecter l’efficacité du médicament ?
Selon leur nature et leur concentration, les impuretés contenues dans la doxazosine peuvent affecter l'efficacité, la stabilité et la sécurité du médicament.
Quelles étapes permettent d’assurer le contrôle des impuretés de la doxazosine pendant le développement du médicament ?
Au cours du développement du médicament, des études approfondies aident à identifier et à caractériser les impuretés présentes dans la doxazosine, à établir des limites acceptables et à mettre en œuvre des stratégies de contrôle appropriées.
Quelles sont les conditions de température nécessaires pour stocker les impuretés de doxazosine ?
La température recommandée pour stocker les impuretés dans la doxazosine est une température ambiante contrôlée, généralement comprise entre 2 et 8 °C. Alternativement, la température spécifique indiquée sur le certificat d'analyse (CoA) est requise pour un stockage correct.
Remarque : Les produits protégés par des brevets valides d'un fabricant ne sont pas proposés à la vente dans les pays bénéficiant d'une protection par brevet. La vente de tels produits constitue une contrefaçon de brevet et sa responsabilité est aux risques et périls de l'acheteur.